Thionylfluorid
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
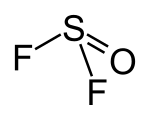
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Thionylfluorid | ||||||||||||||||||
| Andere Namen |
Thionyldifluorid | ||||||||||||||||||
| Summenformel | F2OS | ||||||||||||||||||
| Kurzbeschreibung |
farbloses Gas[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 86,06 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
gasförmig | ||||||||||||||||||
| Dichte |
1,780 g·cm−3 (−100 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
−43,7 °C[1] | ||||||||||||||||||
| Löslichkeit |
langsame Hydrolyse in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Thionylfluorid ist eine chemische Verbindung aus der Gruppe der Thionylhalogenide.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Thionylfluorid kann durch Reaktion von Thionylchlorid mit Fluorwasserstoff oder Natriumfluorid gewonnen werden.[1]
Die einfachste Darstellung im Labor verläuft über die Umsetzung von Thionylchlorid mit Antimon(III)-fluorid in Gegenwart von Antimon(V)-chlorid als Katalysator[3]:
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Thionylfluorid ist ein farbloses Gas, das thermisch bis Rotglut beständig ist. Unedle Metalle wie zum Beispiel Magnesium, Nickel, Quecksilber und Aluminium werden bei trockener Atmosphäre bis 125 °C nicht angegriffen. Während Glas ab 400 °C angegriffen wird, tritt mit Eisen bei dieser Temperatur keine Reaktion ein.[3] Es wird von eiskaltem Wasser nur langsam hydrolysiert[1] und raucht bei Kontakt mit feuchter Luft leicht.[3] Im festen Zustand hat es eine monokline Kristallstruktur mit der Raumgruppe P21/c (Raumgruppen-Nr. 14).[4] Mit Fluor reagiert es zu Thionyltetrafluorid F4SO.[5] Es ist gut löslich in Diethylether und Benzol.[3]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 187.
- ↑ Eintrag zu Thionylfluorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Juli 2016. (JavaScript erforderlich)
- ↑ a b c d W. C. Smith and E. L. Muetterties: Thionyl fluoride. In: Eugene G. Rochow (Hrsg.): Inorganic Syntheses. Band 6. McGraw-Hill Book Company, Inc., 1960, S. 162–163 (englisch).
- ↑ Jean d’Ans, Ellen Lax, Roger Blachnik: Taschenbuch für Chemiker und Physiker. Springer DE, 1998, ISBN 3-642-58842-5, S. 712 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Catherine E. Housecroft: Inorganic Chemistry. Pearson Education, 2005, ISBN 0-13-039913-2, S. 450 (eingeschränkte Vorschau in der Google-Buchsuche).




![{\displaystyle {\ce {3 SOCl2 + 2 SbF3 ->[SbCl_5][]3 SOF2 + 2 SbCl3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a1c2d5ebe96edb8f2850ce7dac7420ae90bf7eb1)