Thujone
Thujone (Absinthol, Tanaceton) sind farblose Flüssigkeiten und bilden eine Gruppe bicyclischer Monoterpen-Ketone mit mentholartigem Geruch. Als Bestandteil ihrer ätherischen Öle sind Thujone unter anderem in Thuja, Thymian, Wermut,[1] Rainfarn, Rosmarin, Beifuß und im Echten Salbei enthalten.
Die Struktur wurde im Jahr 1900 von Friedrich Wilhelm Semmler aufgeklärt.
Vertreter
[Bearbeiten | Quelltext bearbeiten]Bei den Thujonen handelt es sich um die Stereoisomere des 1-Isopropyl-4-methylbicyclo[3.1.0]hexan-3-ons.
| Thujone | ||||||||
| Name | (+)-α-Thujon | (−)-α-Thujon | (+)-β-Thujon | (−)-β-Thujon | ||||
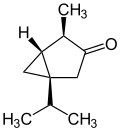
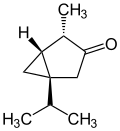
| Strukturformel | 
|
|
|

| ||||
| IUPAC-Name | (1R,4S,5S)-4-Methyl- 1-(propan-2-yl)- bicyclo[3.1.0]hexan-3-on |
(1S,4R,5R)-4-Methyl- 1-(propan-2-yl)- bicyclo[3.1.0]hexan-3-on |
(1S,4S,5R)-4-Methyl- 1-(propan-2-yl)- bicyclo[3.1.0]hexan-3-on |
(1R,4R,5S)-4-Methyl- 1-(propan-2-yl)- bicyclo[3.1.0]hexan-3-on | ||||
| Andere Namen |
1-Isopropyl-4-methylbicyclo[3.1.0]hexan-3-on | |||||||
| CAS-Nummer | 546-80-5 | 471-15-8 | ||||||
| 1125-12-8 | ||||||||
| PubChem | 12304612 | 261491 | 91456 | 6553876 | ||||
| Summenformel | C10H16O | |||||||
| Molare Masse | 152,24 g·mol−1 | |||||||
| Aggregatzustand | flüssig | |||||||
| Kurzbeschreibung | hellgelbe Flüssigkeit[2] | |||||||
| Siedepunkt | 201 °C[3] | |||||||
| Dichte | 0,91 g·cm−3 (20 °C)[3] | |||||||
| Löslichkeit |
sehr schlecht in Wasser[3] | |||||||
| GHS- Kennzeichnung[2] |
|
|
|
| ||||
| H- und P-Sätze | siehe oben | 302 | siehe oben | siehe oben | ||||
| siehe oben | keine EUH-Sätze | siehe oben | siehe oben | |||||
| siehe oben | keine P-Sätze | siehe oben | siehe oben | |||||
| LD50 | 500 mg·kg−1 (Ratte, oral)[2] | |||||||
Vorkommen
[Bearbeiten | Quelltext bearbeiten]

In der Wermutpflanze (Artemisia absinthium) kommen α- und β-Thujone vor.[5] Bei der Herstellung von Absinth werden Thujone aus den Blättern des Wermutkrauts (Folia absinthii) oder der ganzen Pflanze (Herba absinthii) extrahiert. Thujone finden sich daneben auch in vielen anderen Artemisien und z. B. auch mit einem Anteil von bis zu 60 % in den ätherischen Ölen des Echten Salbeis (Salvia officinalis) und ebenfalls in der getrockneten Form des weißen Salbeis (Salvia apiana), welcher u. a. zum Räuchern verwendet wird. Thujaöl enthält 40 % (−)-α-Thujon, Rainfarnöl 58 % (+)-β-Thujon.[6]
Wirkungen
[Bearbeiten | Quelltext bearbeiten]Thujone sind Nervengifte, die in höherer Dosierung Verwirrtheit und epileptische Krämpfe (Konvulsionen) hervorrufen können. Auch andere Symptome, wie Schwindel, Halluzinationen und Wahnvorstellungen, die nach Einnahme thujonhaltiger alkoholischer Getränke beobachtet werden konnten, wurden diesen Wirkstoffen zugeschrieben. Ebenso werden diese Getränke, insbesondere der Absinth, wegen einer angeblichen euphorisierenden und aphrodisierenden Wirkung beworben. Da der zulässige Thujongehalt in alkoholischen Getränken auf maximal 35 mg je kg begrenzt wurde und auch bei historischen Absinthen keine höheren Werte nachgewiesen werden konnten, wird die Wirkung des Absinthkonsums heutzutage eher dem Alkohol zugeschrieben.[7] Die Symptome des chronischen Absinthkonsums (Absinthismus) sind identisch mit denen eines Alkoholismus.[8] Eine Studie[9] im Jahr 2008 wies in Proben aus der Zeit vor dem Verbot nur Konzentrationen von durchschnittlich 25 mg/l nach. Eine psychotrope Wirkung ist bei diesen Werten äußerst unwahrscheinlich.
Für die beschriebenen konvulsiven Wirkungen der Thujone werden insbesondere GABAA-Rezeptoren verantwortlich gemacht. Als Antagonisten und Modulatoren dieser Rezeptoren hemmen Thujone die antikonvulsive Wirkung der γ-Aminobuttersäure (GABA), wenngleich mit schwacher Potenz.[10] Als GABAA-Rezeptor Antagonisten ähneln sie in ihrer Wirkung den Pflanzengiften Bicucullin der Herzblumen und dem Picrotoxin der Scheinmyrte. Auch eine Desensibilisierung von 5-HT3-Rezeptoren kann an den beobachteten Effekten beteiligt sein.[11] Ein möglicher gemeinsamer Wirkmechanismus mit dem Cannabis-Wirkstoff Tetrahydrocannabinol über eine Aktivierung von Cannabinoid-Rezeptoren, der auf Grund entfernter Analogien der Molekülstruktur und klinischen Wirkungen vermutet wurde,[12] konnte hingegen nicht bestätigt werden.[13] Für den bitteren Geschmack der Thujone wird eine Aktivierung des Geschmacksrezeptors TAS2R14 verantwortlich gemacht.[14]
Analytik
[Bearbeiten | Quelltext bearbeiten]Die zuverlässige qualitative und quantitative Bestimmung in verschiedenen Untersuchungsmaterialien gelingt nach hinreichender Probenvorbereitung durch Koppelung der Gaschromatographie oder der HPLC mit der Massenspektrometrie.[15][16][17] Auch für Metabolismusstudien werden diese Verfahren eingesetzt.[18]
Gesetzliche Vorschriften
[Bearbeiten | Quelltext bearbeiten]Durch die ehemalige Aromenverordnung[19] wird der Thujongehalt in Lebensmitteln begrenzt. In Getränken und anderen Lebensmitteln dürfen maximal 0,5 mg/kg enthalten sein. Lebensmittel, die Salbeizubereitungen enthalten, dürfen höchstens 25 mg/kg Thujone enthalten. Die Grenze in alkoholhaltigen Getränken (Sonderregelung) hängt von dem Alkoholgehalt der Spirituose ab:
Branntweine:
- maximal 5 mg/kg bei einem Alkoholgehalt bis zu 25 Vol.-%
- maximal 10 mg/kg bei einem Alkoholgehalt über 25 Vol.-%
Bitter-Spirituosen:
- maximal 35 mg/kg bei einem Alkoholgehalt über 25 Vol.-%
Außerhalb von Lebensmitteln fällt Thujon unter die Definition von § 2 Abs. 1 des AMG, sobald es für die Anwendung an Mensch oder Tier bestimmt ist. Somit ist Herstellung und Verkauf einer Substanz nach dem AMG reguliert, unabhängig davon in welcher Form die Substanz vorliegt, wenn sie in Bestimmung § 2 Abs. 1 erfüllt.[20][21] Der Verkauf und die Herstellung von Arzneimitteln ohne Genehmigung ist strafbar nach AMG § 2 Abs. 1 Nr. 5 a. F., § 2 Abs. 1 Nr. 2a n. F., § 5, § 95 Abs. 1 Nr. 1. Dies wurde in einem Urteil des Bundesgerichtshofs zu der frei verfügbaren Chemikalie γ-Butyrolacton (GBL) bestätigt, welche nach dem AMG als Arzneimittel eingestuft wird, sobald sie für den Konsum bzw. Gebrauch an Mensch oder Tier bestimmt ist.[22][23]
Die deutsche Tabakverordnung verbietet den Zusatz von Thujon zu Tabakprodukten.
In der Europäischen Union gelten nach Anhang III der Verordnung (EG) Nr. 1334/2008 folgende Grenzwerte für Thujon:[24]
- 0,5 mg/kg in mit Artemisia spp. hergestellten alkoholfreien Getränken
- 10 mg/kg in alkoholischen Getränken, die nicht mit Artemisia spp. hergestellt werden
- 35 mg/kg in mit Artemisia spp. hergestellten alkoholischen Getränken
In den USA ist der Zusatz von Thujon zu Nahrungsmitteln nicht gestattet.[25] Nahrungsmittel und Getränke mit Artemisia sp. Abendländischer Lebensbaum, Eichenmoos, Rainfarn, oder Gemeine Schafgarbe müssen unter 10 mg/l Thujon enthalten.[26][27] Andere Pflanzen mit Thujon sind nicht reguliert, z. B. sind Salbei und Salbeiöl (mit bis zu 50 % Thujon) als Generally Recognized As Safe (GRAS, unbedenklicher Stoff) klassifiziert.[28]
In Kanada werden alkoholische Getränke von den Provinzen reguliert. In Alberta, Ontario, British Columbia und Nova Scotia sind bis zu 10 mg/kg Thujon erlaubt, in Quebec 15 mg/kg, in Manitoba 6–8 mg/L.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Otto Vostrowsky, Thorolf Brosche, Helmut Ihm, Robert Zintl, Karl Knobloch: Über die Komponenten des ätherischen Öls aus Artemisia absinthium L.. In: Zeitschrift für Naturforschung C. 36, 1981, S. 369–377 (PDF, freier Volltext).
- ↑ a b c Datenblatt (−)-α-Thujone bei Sigma-Aldrich, abgerufen am 19. Mai 2017 (PDF).
- ↑ a b c d David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 85. Auflage. (Internet-Version: 2005), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-532.
- ↑ a b Erowid
- ↑ Datenblatt α- und β-Thujon (Isomerengemisch) (PDF) bei Carl Roth, abgerufen am 14. Dezember 2010.
- ↑ Eintrag zu Thujone. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. April 2014.
- ↑ R. W. Olsen: Absinthe and γ-aminobutyric acid receptors. In: Proc. Natl. Acad. Sci. U.S.A. Band 97, 2000, S. 4417–4418.
- ↑ S. A. Padosch, D. W. Lachenmeier, L. U. Kröner: Absinthism: a fictitious 19th century syndrome with present impact. In: Subst. Abuse Treat. Prev. Policy. Band 1, 2006, S. 14.
- ↑ D. Lachenmeier, D. Nathan-Maister, T. Breaux, E.-M. Sohnius, K. Schoeberl, T. Kuballa: Chemical Composition of Vintage Preban Absinthe with Special Reference to Thujone, Fenchone, Pinocamphone, Methanol, Copper, and Antimony Concentrations. In: J. Agric. Food Chem. 56 (9), 2008, S. 3073–3081.
- ↑ K. M. Hold, N. S. Sirisoma, T. Ikeda, T. Narahashi, J. E. Casida: α-thujone (the active component of absinthe): γ-aminobutyric acid type A receptor modulation and metabolic detoxification. In: Proc. Natl. Acad. Sci. U.S.A. Band 97, 2000, S. 3826–3831.
- ↑ T. Deiml, R. Haseneder, W. Zieglgänsberger, G. Rammes, B. Eisensamer, R. Rupprecht, G. Hapfelmeier: α-Thujone reduces 5-HT3 receptor activity by an effect on the agonist-reduced desensitization. In: Neuropharmacology. Band 46, 2004, S. 192–201.
- ↑ J. del Castillo, M. Anderson, G. M. Rubottom: Marijuana, absinthe and the central nervous system. In: Nature. Band 253, 1975, S. 365–366.
- ↑ J. P. Meschler, A. C. Howlett: Thujone exhibits low affinity for cannabinoid receptors but fails to evoke cannabimimetic responses. In: Pharmacol Biochem Behav. Band 62, 1999, S. 473–480.
- ↑ M. Behrens, A. Brockhoff, C. Kuhn, B. Bufe, M. Winnig, W. Meyerhof: The human taste receptor hTAS2R14 responds to a variety of different bitter compounds. In: Biochem. Biophys. Res. Commun. Band 319, 2004, S. 479–485. PMID 15178431.
- ↑ B. Bach, M. Cleroux, M. Saillen, P. Schönenberger, S. Burgos, J. Ducruet, A. Vallat: A new chemical tool for absinthe producers, quantification of α/β-thujone and the bitter components in Artemisia absinthium. In: Food Chem. 213, 15. Dez 2016, S. 813–817. PMID 27451252
- ↑ J. D. Williams, J. A. Yazarians, C. C. Almeyda, K. A. Anderson, G. R. Boyce: Detection of the Previously Unobserved Stereoisomers of Thujone in the Essential Oil and Consumable Products of Sage (Salvia officinalis L.) Using Headspace Solid-Phase Microextraction-Gas Chromatography-Mass Spectrometry. In: J Agric Food Chem. 64(21), 1. Jun 2016, S. 4319–4326. PMID 27181395
- ↑ H. Hu, X. Zheng, H. Hu, R. Wang, Y. Wu: Study on gas chromatography-mass spectrometry fingerprint of Acanthopanax brachypus. In: J Chromatogr Sci. 52(8), Sep 2014, S. 759–765. PMID 24076562
- ↑ K. Abass, P. Reponen, S. Mattila, O. Pelkonen: Metabolism of α-thujone in human hepatic preparations in vitro. In: Xenobiotica. 41(2), Feb 2011, S. 101–111. PMID 21087116
- ↑ AromV Aromenverordnung. Abgerufen am 19. Januar 2024.
- ↑ Erwin Deutsch, Rudolf Ratzel, Hans-Dieter Lippert: Kommentar zum Arzneimittelgesetz (AMG). 3. Auflage. Gabler Wissenschaftsverlage, 2010, ISBN 978-3-642-01454-3, S. 64–66 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ ArzneimittelG § 2 Abs. 1 Nr. 5 a. F., § 2 Abs. 1 Nr. 2a n. F., § 5, § 95 Abs. 1 Nr. 1. Abgerufen am 16. Mai 2012.
- ↑ Martin Kämpf: Strafrecht: Handel mit Gamma-Butyrolacton (GBL, liquid ecstasy) zu Konsumzwecken. 25. Juli 2011.
- ↑ Das unerlaubte Inverkehrbringen von Gamma-Butyrolacton (GBL) zu Konsumzwecken ist nach dem Arzneimittelgesetz strafbar. BGH-Urteil vom 8. Dezember 2009, 1 StR 277/09, LG Nürnberg-Fürth bei Lexetius.com/2009,3836.
- ↑ Verordnung (EG) Nr. 1334/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 (PDF)
- ↑ Laurie C. Dolan, Ray A. Matulka, George A. Burdock: Naturally Occurring Food Toxins. In: Toxins. Band 2, Nr. 9, 2010, S. 2289–2332, doi:10.3390/toxins2092289, PMID 22069686, PMC 3153292 (freier Volltext).
- ↑ FDA Regulation 21 CFR 172.510 – Food Additives Permitted for Direct Addition to Food for Human Consumption. Food and Drug Administration (2003). Abgerufen am 28. Oktober 2006.
- ↑ Department of the Treasury Alcohol and Tobacco Tax and Trade Bureau Industry Circular 2007-5 ( vom 9. Februar 2014 im Internet Archive) Abgerufen am 17. Oktober 2007 (oder am 5. Mai 2009?).
- ↑ Substances generally recognized as safe. ( vom 30. November 2005 im Internet Archive) Food and Drug Administration (2003). Abgerufen am 28. Oktober 2006.

