Trialkylborane
| Trialkylborane |
|---|
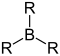 Allgemeine Formel (R = Alkyl) |
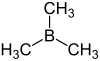 Trimethylboran |
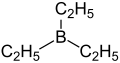 Triethylboran |
Trialkylborane (BR3) sind meist unbeständige, luftempfindliche Verbindungen. Häufig werden sie deshalb unmittelbar nach der Herstellung weiter verarbeitet.[1]
Herstellung
[Bearbeiten | Quelltext bearbeiten]Es gibt mehrere Methoden zur Synthese von Trialkylboranen:
- aus Borwasserstoff (BH3) und Alkenen,[2]
- aus Bortrihalogeniden – z. B. Bortrifluorid (BF3) – mit Grignard-Verbindungen,[3]
- aus Trialkylderivaten des Boroxins[4] und
- aus Trialkylaluminiumverbindungen.[4]
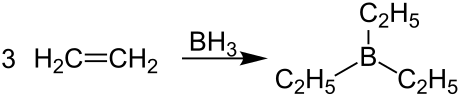
Die atomeffizienteste Methode ist dabei die Addition von Borwasserstoff an die C=C-Doppelbindung von Alkenen. So reagiert BH3 z. B. mit Ethen zu Triethylboran:[1]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Im Gegensatz zu Diboran (B2H6) liegen die Trialkylborane in monomerer Form vor, weil eine Dimerisierung über Zweielektronen-Dreizentren-Bindungen aus sterischen Gründen verhindert wird.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Die Oxidation der Trialkylborane mit Wasserstoffperoxid (H2O2) führt zu Alkoholen. So wird z. B. Triethylboran zu Triethylborat oxidiert und anschließend unter Einwirkung von Natronlauge zu Ethanol hydrolysiert:[1]

Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Joachim Buddrus, Bernd Schmidt: Grundlagen der Organischen Chemie, 5. Auflage, de Gruyter Verlag, Berlin, 2015, S. 176–178, ISBN 978-3-11-030559-3.
- ↑ Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 237, ISBN 3-342-00280-8.
- ↑ a b Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 548, ISBN 3-342-00280-8.
- ↑ a b Otto-Albrecht Neumüller (Herausgeber): Römpps Chemie Lexikon, 8. Auflage, Frank’sche Verlagshandlung, Stuttgart 1983, ISBN 3-440-04513-7, S. 497.