Tribromacetaldehyd
Zur Navigation springen
Zur Suche springen
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
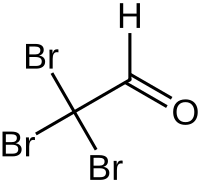
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tribromacetaldehyd | ||||||||||||||||||
| Andere Namen |
Bromal | ||||||||||||||||||
| Summenformel | C2HBr3O | ||||||||||||||||||
| Kurzbeschreibung |
gelbe bis braune Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 280,74 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
2,665 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Siedepunkt |
174 °C[1] | ||||||||||||||||||
| Löslichkeit |
löslich in Wasser, Ethanol und Aceton[2] | ||||||||||||||||||
| Brechungsindex |
1,584 (20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Tribromacetaldehyd ist eine anorganische chemische Verbindung aus der Gruppe der Aldehyde.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Tribromacetaldehyd kann durch Reaktion von Brom mit Ethanol oder Chloral gewonnen werden.[2]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Tribromacetaldehyd ist eine gelbliche bis braune Flüssigkeit, die in Wasser löslich ist und dabei Bromalhydrat bildet.[1][2] Sie wird durch Alkalien in Ameisensäure und Bromoform zerlegt.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Tribromacetaldehyd wird für organische Synthesen (zum Beispiel von Tribromethanol[4]) verwendet.[2]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Datenblatt Tribromoacetaldehyde, 97% bei Sigma-Aldrich, abgerufen am 10. November 2021 (PDF).
- ↑ a b c d Eintrag zu Tribromoacetaldehyde in der Hazardous Substances Data Bank (via PubChem), abgerufen am 23. Juli 2015.
- ↑ F.K. Beilstein: Handbuch der organischen Chemie. 1928, ISBN 5-88502-336-0, S. 935 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Lehrbuch der Anaesthesiologie. Springer-Verlag, 2013, ISBN 978-3-662-01556-8, S. 24 (eingeschränkte Vorschau in der Google-Buchsuche).

