Triphenylgermaniumhydrid
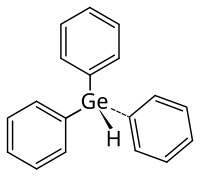
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Triphenylgermaniumhydrid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C18H16Ge | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 320,496 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
127–128 °C (0,01 hPa)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Triphenylgermaniumhydrid ist eine chemische Verbindung aus der Gruppe der germaniumorganischen Verbindungen.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Triphenylgermaniumhydrid kann durch Reaktion von Triphenylgermaniumchlorid und Zinkstaub in Ethanol oder durch Reaktion von Triphenylgermaniumchlorid oder Triphenylgermaniumbromid mit Lithiumaluminiumhydrid oder Natriumborhydrid gewonnen werden.[2]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Triphenylgermaniumhydrid ist ein weißer kristalliner Feststoff.[1] Die Verbindung ist dimorph, die stabilere α-Form schmilzt bei 41–45 °C,[3][4] die β-Form bei 27 °C.[2] Mit einer Reihe von Vinylderivaten reagiert es ohne Katalysator.[5] Die Pyrolyse bei 300 °C ergibt Tetraphenylgermanium und Diphenylgermaniumdihydrid.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Triphenylgermaniumhydrid kann als Polymerisationshemmer verwendet werden.[2]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Datenblatt Triphenylgermanium hydride, bei Sigma-Aldrich, abgerufen am 7. Oktober 2017 (PDF).
- ↑ a b c d Jane E. Macintyre: Dictionary of Organometallic Compounds. CRC Press, 1994, ISBN 978-0-412-43060-2, S. 1742 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Richard W. Weiss: Compounds of Germanium, Tin, and Lead, including Biological Activity and Commercial Application Covering the Literature from 1937 to 1964. Springer Science & Business Media, 2013, ISBN 978-3-642-51889-8, S. 52 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ John E. Drake, Christa Siebert: Ge Organogermanium Compounds Part 4: Compounds with Germanium-Hydrogen Bonds. Springer Science & Business Media, 2013, ISBN 978-3-662-06324-8, S. 100 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ B. L. Shaw: Inorganic Hydrides The Commonwealth and International Library: Chemistry Division. Elsevier, 2013, ISBN 978-1-4831-6032-0, S. 49 (eingeschränkte Vorschau in der Google-Buchsuche).

![{\displaystyle \mathrm {4\ Ge(C_{6}H_{5})_{3}Br+Li[AlH_{4}]\longrightarrow 4\ Ge(C_{6}H_{5})_{3}H+LiBr+AlBr_{3}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/10f8805308f905fd98e010da2c4d6ddea7d1de94)
