Neuroleptikum

Ein Neuroleptikum (Mehrzahl Neuroleptika; von altgriechisch νεῦρον neũron, deutsch ‚Nerv‘, λῆψις lepsis, deutsch ‚ergreifen‘)[1] oder Antipsychotikum ist ein Arzneistoff aus der Gruppe der Psychopharmaka, die eine dämpfende (sedierende) und antipsychotische (den Realitätsverlust bekämpfende) Wirkung besitzen.[2]
Einsatzbereiche
[Bearbeiten | Quelltext bearbeiten]Hauptsächlich werden Neuroleptika zur Behandlung von Wahnvorstellungen und Halluzinationen eingesetzt, wie sie etwa im Rahmen einer Schizophrenie oder Manie auftreten können.[3]
Zusätzlich werden sie auch als Beruhigungsmittel verwendet, etwa bei Unruhe, Ängsten oder Erregungszuständen.[4] In diesem Zusammenhang werden sie häufig in Altenheimen eingesetzt.[5][6] In neuerer Zeit werden Neuroleptika zunehmend bei folgenden psychischen Erkrankungen verwendet:
- bei Tourette-Syndrom[7] und Zwangserkrankungen[8]
- Depressionen[9] oder Persönlichkeitsstörungen[10]
- ADHS bei Kindern[11] und Fetalem Alkoholsyndrom
- bei Autismus gegen Reizbarkeit und selbstverletzendes Verhalten[12]
Geschichte
[Bearbeiten | Quelltext bearbeiten]Anfänge
[Bearbeiten | Quelltext bearbeiten]Ausgangspunkt der Entwicklung von Neuroleptika war die deutsche Farbstoffindustrie Ende des 19. Jahrhunderts. Damals stellte die Firma BASF chemische Farbstoffe her, die bald auch in der Histologie Verwendung fanden. Bei bestimmten Farbstoffen stellte man eine antibiotische Wirksamkeit fest, beispielsweise wirkte der Stoff Methylenblau, ein Phenothiazin-Derivat, gegen Malaria. Bei Anwendung der Phenothiazinderivate wie Promethazin stellte man eine sedierende und antihistaminerge Wirkung fest. Dies sollte bei kriegsbedingten Schock- und Stressreaktionen und bei Operationen von Vorteil sein. Die zusätzlichen vegetativen (sympathico- und vagolytischen) Eigenschaften wurden als „künstlicher Winterschlaf“ bezeichnet und sollten bei größeren Operationen hilfreich sein. Zusammen mit Opiaten wurde damals von Neuroleptanästhesie gesprochen.
Das erste Neuroleptikum Chlorpromazin
[Bearbeiten | Quelltext bearbeiten]
Der erste Wirkstoff, der als antipsychotisch wirksames Medikament vermarktet wurde, ist das Chlorpromazin.[13] Es wurde im Jahr 1950 erstmals in Frankreich bei Forschungen zu antihistaminisch wirksamen Substanzen vom Chemiker Paul Charpentier bei der Firma Rhône-Poulenc synthetisiert. Seine antipsychotische Wirkung wurde zu diesem Zeitpunkt allerdings noch nicht erkannt. Im Jahre 1952 erprobte der französische Chirurg Henri Marie Laborit auf der Suche nach einem wirksamen Anästhetikum mehrere Antihistaminika. Er bemerkte, dass diese Stoffe eine sedierende und angstlösende Wirkung zu haben schienen, allen voran das Chlorpromazin.
Zwischen April 1951 und März 1952 wurden 4000 Proben an über 100 Forscher in 9 Länder verschickt. Am 13. Oktober 1951 erschien der erste Artikel, in dem Chlorpromazin öffentlich erwähnt wurde. Laborit berichtete über seine Erfolge mit der neuen Substanz bei der Anästhesie. Die beiden französischen Psychiater Jean Delay und Pierre Deniker gaben am 26. Mai 1952 bekannt, dass sie eine beruhigende Wirkung bei Patienten mit Manie gesehen hätten. Sowohl die Effekte in der Anästhesie als auch die psychotropen Wirkungen bezeichneten sie als Neurolepsie, was sich auf den neuronalen Einfluss der Medikamente bezog und zur Bezeichnung der neuen Stoffklasse führte.[14] Während Chlorpromazin am Anfang noch gegen viele verschiedene Störungen eingesetzt wurde, zeigte sich später als wichtigste Indikation eine spezifische Wirkung gegen psychomotorische Unruhe, vor allem bei der Schizophrenie.
Ab 1953 wurde das Chlorpromazin als Megaphen (Deutschland 1. Juli 1953) oder Largactil in Europa vermarktet, 1955 kam es in den USA unter dem Namen Thorazine auf den Markt. Die heute gebräuchliche Bezeichnung „Neuroleptikum“ wurde 1955 von Delay und Deniker eingeführt. Sie hatten beobachtet, dass Reserpin und Chlorpromazin sehr ähnliche extrapyramidale Nebenwirkungen haben.[15] Das neue Medikament wurde in den USA als „chemische Lobotomie“ beworben,[16][17][18] ähnlich wie später die medikamentöse „Lobotomie“ mit dem Medikament Reorganin (Guajacolglycerinaether) der Firma Dr. Christian Brunnengräber in Lübeck.[19]
Einfluss auf die Behandlung psychischer Störungen
[Bearbeiten | Quelltext bearbeiten]
Neuroleptika revolutionierten[17] die Behandlung von psychotischen Störungen.[20] Vor Einführung der Neuroleptika stand Menschen, die an einer akuten Psychose litten, keine symptomatische Behandlungsmethode zur Verfügung. Sie wurden gegen ihren Willen mit kalten Duschen übergossen oder angekettet,[21] im Mittelalter auch ausgepeitscht oder gar auf dem Scheiterhaufen verbrannt.[22] Aber auch bis hinein in die zweite Hälfte des 20. Jahrhunderts stand vielen keine adäquate Behandlungsmöglichkeit zur Verfügung. Oft mussten Erkrankte aufgrund fehlender Selbständigkeit oder drohender Eigen- und Fremdgefährdung in eine psychiatrische Klinik eingeliefert und solange dort behalten werden, bis die Symptome mit der Zeit abklangen. Als Behandlungsmöglichkeiten standen dort lediglich Schutzmaßnahmen wie Freiheitsentzug oder medikamentöse Sedierung zur Verfügung, um die Patienten daran zu hindern, sich selbst oder Dritte in ihrem wahnhaften Zustand zu schädigen. In den USA wurde, um Erkrankte ruhig zu stellen, bis zur Mitte des 20. Jahrhunderts die Lobotomie angewandt; eine neurochirurgische Operation, bei der die Nervenbahnen zwischen Thalamus und Frontallappen getrennt sowie Teile der grauen Substanz entnommen werden.
Mit Einführung der Neuroleptika konnten die Symptome der Patienten erstmals gezielter bekämpft werden, was die Dauer des krankhaften Zustandes und damit auch die nötige Aufenthaltsdauer in den Kliniken reduzierte. Die Verwendung von Neuroleptika setzte sich vor allem in Europa schnell durch. In den USA waren noch längere Zeit andere Behandlungsmethoden wie Lobotomie und Psychoanalyse gebräuchlich. Heute ist die Gabe von Neuroleptika in den Industrieländern die Standardmethode bei behandlungsbedürftigen Psychosen.[23]
Konzepte der neuroleptischen Schwelle und Potenz
[Bearbeiten | Quelltext bearbeiten]Die klassischen Neuroleptika verursachten neben der erwünschten antipsychotischen Wirkung eine Reihe von Nebenwirkungen, darunter das sogenannte extrapyramidale Syndrom. Dabei handelt es sich um Störungen der Bewegungsabläufe, die sich beispielsweise in Form einer Sitzunruhe oder einer Muskelstarrheit ähnlich wie bei Parkinson-Erkrankten äußern. Der Psychiater Hans-Joachim Haase war auf der Suche nach der optimalen Dosierung von Neuroleptika zu der Überzeugung gelangt, dass eine Substanz umso stärker antipsychotisch wirke, je größer diese extrapyramidalmotorischen Nebenwirkungen seien. Er führte 1961 die Begriffe „neuroleptische Schwelle“ und „neuroleptische Potenz“ ein.[24]
Die neuroleptische Schwelle definierte Haase als die minimale Dosis eines Wirkstoffes, bei der messbare extrapyramidalmotorische Nebenwirkungen auftreten. Als Messverfahren entwickelte er einen Test der feinmotorischen Fähigkeiten, der auf Beobachtung der Handschrift basiert und später als Haase-Schwellentest bekannt wurde. Die neuroleptische Schwellendosis war laut Haase zugleich die minimale antipsychotisch wirksame Dosis.[24][25]
Die neuroleptische Potenz definierte er als ein Maß für die Wirksamkeit einer Substanz. Je höher die neuroleptische Potenz eines Wirkstoffes, desto geringer ist die Dosis, die zum Erreichen der neuroleptischen Schwelle nötig ist.[24]
Haases Beobachtungen führten nach ihrer Veröffentlichung zu einer massiven Verringerung der in Europa und den USA verabreichten Neuroleptika-Dosierungen.[26][27]
Für die später eingeführten Neuroleptika der zweiten Generation, den sogenannten atypischen Neuroleptika, verloren die Konzepte von Haase ihre Gültigkeit, da bei ihnen kein direkter Zusammenhang mehr zwischen der antipsychotischen Wirkung und dem Auftreten von extrapyramidalmotorischen Nebenwirkungen besteht.[24][25]
Einführung der atypischen Neuroleptika
[Bearbeiten | Quelltext bearbeiten]Die Einführung der Neuroleptika stellte zwar einen Durchbruch dar, bei 30–40 % der Patienten waren sie jedoch unwirksam.[20] Mit dem Clozapin wurde im Jahre 1971 eine neue Generation von Neuroleptika eingeführt, die sogenannten atypischen Neuroleptika. Sie versprachen eine vergleichbare antipsychotische Wirkung bei geringen oder fehlenden extrapyramidalmotorischen Nebenwirkungen,[28][29] zudem wirkten sie auch auf die sogenannten Negativsymptome der Schizophrenie.[20][29] Sie lösten die älteren Medikamente als Mittel der ersten Wahl ab[30] und wirkten häufig auch bei Patienten, die auf die bisherigen Medikamente nicht ansprachen.[28][20][29] Zur Abgrenzung gegen die bisherigen Neuroleptika werden diese neuen Wirkstoffe als atypische Neuroleptika oder Neuroleptika der zweiten Generation (seit 1994) bezeichnet, die alten Wirkstoffe hingegen als typische, konventionelle oder klassische Neuroleptika.[25] Seitdem wurde eine Reihe weiterer atypischer Neuroleptika erforscht und auf den Markt gebracht.[28]
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]Wirkmechanismus
[Bearbeiten | Quelltext bearbeiten]
Der genaue Wirkmechanismus von Neuroleptika ist nicht vollständig geklärt und Gegenstand aktueller Forschung. Nach der gängigen Dopaminhypothese der Schizophrenie werden sogenannte Positivsymptome wie Halluzinationen und Wahngedanken durch eine erhöhte Konzentration des Neurotransmitters Dopamin im mesolimbischen Trakt des Gehirns verursacht.[31]
Neuroleptika hemmen die Signalübertragung von Dopamin im Gehirn durch ihre antagonistische Wirkung auf postsynaptische D2-Rezeptoren. Die daraus resultierende Hemmung der mesolimbischen Bahnen könnte demzufolge die antipsychotische Wirkung erklären.[32]
Die klassischen, auch als dopamin-antagonistisch bezeichneten Neuroleptika wirken in dieser Hinsicht jedoch wenig spezifisch, da sich ihre dopaminhemmende Wirkung nicht nur auf die mesolimbischen Bahnen, sondern auf das gesamte dopaminerge System erstreckt. Dadurch entstehen neben der erwünschten antipsychotischen Wirkung auch eine Reihe von Nebenwirkungen. Im nigrostriatalen System wirken Neuroleptika störend auf körperliche Bewegungsabläufe, bei denen Dopamin eine wichtige Rolle spielt. Auch wirken klassische Neuroleptika nicht auf die sogenannten Negativsymptome der Schizophrenie, sondern können sie sogar verschlimmern, da sie gemäß der Dopaminhypothese durch eine verminderte Dopaminkonzentration im mesokortikalen System des Gehirns verursacht werden.[32][31]
Die neueren atypischen Neuroleptika haben eine mit den klassischen Neuroleptika vergleichbare antipsychotische Wirkung, verursachen aber weniger extrapyramidalmotorische Nebenwirkungen und wirken zusätzlich auch auf die sogenannten Negativsymptome der Schizophrenie. Diese Eigenschaften werden auf Besonderheiten ihres Rezeptorbindungsprofils zurückgeführt, das sich je nach Wirkstoff signifikant unterscheiden kann. So wird etwa eine spezifischere Bindung an die mesolimbischen D2-Rezeptoren vermutet. Die Interaktion mit Rezeptoren weiterer Neurotransmitter wie Serotonin, Acetylcholin, Histamin und Noradrenalin könnte die zusätzliche Wirkung auf die Negativsymptome erklären.[32]
Neuroleptika wirken symptomatisch, können also psychische Krankheiten nicht im eigentlichen Sinne heilen. Symptome wie Halluzinationen, Wahn oder Erregungszustände können aber zumindest für die Dauer der medikamentösen Behandlung unterdrückt werden. Dies ermöglicht dem Patienten eine Distanzierung von der Erkrankung, sodass er seinen eigenen Zustand als krankhaft erkennen kann.
Unerwünschte Wirkungen
[Bearbeiten | Quelltext bearbeiten]Die möglichen unerwünschten Wirkungen hängen stark vom jeweiligen Wirkstoff und der Dosierung ab.
Bei den unerwünschten Wirkungen sind solche vegetativer Art (hormonelle und sexuelle Störungen, Muskel- und Bewegungsstörungen, Schwangerschaftsschäden, Körpertemperaturstörungen etc.) und solche psychischer Art (sedierende Wirkungen unter anderem mit erhöhter Sturzgefahr, Depressionen, Antriebslosigkeit, emotionale Verarmung, Verwirrtheit, Delir und andere Wirkungen auf das Zentralnervensystem mit erhöhter Sterblichkeit bei Demenzkranken[33]) zu unterscheiden.
Störung von Bewegungsabläufen
[Bearbeiten | Quelltext bearbeiten]
Eine Folge der hemmenden Wirkung auf den Überträgerstoff Dopamin ist die Störung von körperlichen Bewegungsabläufen, da Dopamin daran wesentlich beteiligt ist. Da diese Störungen das extrapyramidalmotorische System betreffen, werden sie auch als extrapyramidales Syndrom zusammengefasst.[34] Sie lassen sich weiter unterteilen in folgende Symptome:
- Akathisie: Bewegungsunruhe, die den Betroffenen dazu bringt, ständig umherzulaufen oder sinnlos erscheinende Bewegungen wie auf der Stelle treten oder Wippen mit dem Knie zu vollziehen.
- Frühdyskinesien: Unwillkürliche Bewegungen bis hin zu krampfartigen Anspannungen von Muskeln und Muskelgruppen. Möglich sind auch Zungen- und Schlundkrämpfe.
- Parkinsonoid: Bewegungsstörungen, die in ihrem Erscheinungsbild der Parkinson-Krankheit ähneln. Häufig ist dabei eine Muskelstarre (Rigor), die die Bewegungen des Betroffenen ungelenk und roboterartig erscheinen lässt. Auffällig ist oft ein kleinschrittiger, schlurfender Gang. Auch dystone Störungen wie zum Beispiel ein Schiefhals kommen vor. Zur Früherkennung solcher Störungen kann der sogenannte Haase-Schwellentest genutzt werden, der zur Prüfung der Feinmotorik die Handschrift heranzieht.
- Spätdyskinesien: Bei Langzeitbehandlungen treten in bis zu 20 % aller Fälle Spätdyskinesien, auch tardive Dyskinesien genannt, auf. Dabei handelt es sich um Bewegungsstörungen im Gesichtsbereich (Zuckungen, Schmatz- und Kaubewegungen) oder Hyperkinesen (unwillkürliche Bewegungsabläufe) der Extremitäten. Die Schwere dieser Störungen hängt von Dosierung und Dauer der neuroleptischen Behandlung ab. Spätdyskinesien bilden sich in einigen Fällen auch nach Absetzen des Neuroleptikums nicht zurück und bleiben ein Leben lang. Das Absetzen des Neuroleptikums kann die Beschwerden vorübergehend verstärken, verhindert aber langfristig das weitere Fortschreiten.
Ein Anticholinergikum wie Biperiden kann diesen Symptomen entgegenwirken und daher ergänzend verabreicht werden.[35] Spätdyskinesien sprechen darauf allerdings nicht an.
Mögliche Beeinträchtigung des Gehirns
[Bearbeiten | Quelltext bearbeiten]Die Behandlung mit hochpotenten Neuroleptika kann zu einem dosis- und zeitabhängigen Umbau der Struktur des Gehirns mit einer Verschiebung des Verhältnisses von grauer zu weißer Substanz und einer Verringerung des Volumens verschiedener seiner Strukturen (Neurodegeneration) führen.[36]
Zwar geht bereits eine Schizophrenie als solche mit einem geringeren Hirnvolumen gegenüber gesunden Vergleichspersonen einher, es gibt jedoch eindeutige Hinweise in zahlreichen Studien und Befunden, dass die Medikamente unabhängig davon eine weitere Reduktion des Hirnvolumens bewirken können. Es gibt Hinweise, dass die Volumenreduktion mit einer Verschlechterung kognitiver Fähigkeiten einhergeht, etwa einer schlechteren Orientierung, Defiziten bei verbalen Aufgaben, nachlassender Aufmerksamkeit und einem geringeren Abstraktionsvermögen. Diese Beeinträchtigungen stehen in direktem Zusammenhang mit der Höhe der verabreichten Dosis. Dabei sind besonders ältere Empfehlungen problematisch, die auf heute als unnötig hoch erachteten Dosierungen und zu langen Behandlungszeiträumen basieren. Geringere und zeitlich beschränkte Dosierungen können demnach die Schädigungen begrenzen.[37] Die wichtigste deutsche Fachvereinigung für Psychiater, die DGPPN, behandelte die Problematik, die in neuerer Zeit immer mehr Beachtung findet, im Rahmen ihres Jahreskongresses.[38]
Weitere unerwünschte Wirkungen
[Bearbeiten | Quelltext bearbeiten]Weitere mögliche unerwünschte Wirkungen sind Leber- oder Nierenfunktionsstörungen, Herzrhythmusstörungen (mit Veränderung der QT-Zeit), Funktionsstörung der Bauchspeicheldrüse, Einschränkungen von Sexualität und Libido, Gewichtszunahme,[39] Hormonstörungen (u. a. bei Frauen: Störungen der Regelblutung). Fallkontrollstudien zeigten auch ein um etwa ein Drittel erhöhtes Risiko für eine Thromboembolie.[40]
Eine Reihe von Neuroleptika zeigen anticholinerge Wirkungen (so Chlorpromazin, Thioridazin, Fluphenazin, Perazin, Melperon und Clozapin).[41]
Bei Vorliegen einer entsprechenden Disposition können Neuroleptika der Auslöser für sogenannte Gelegenheitsanfälle sein.
Seltene (bis zu 0,4 %), aber unter Umständen lebensgefährliche Nebenwirkungen sind das maligne neuroleptische Syndrom mit Fieber, Muskelsteifigkeit und Bewegungsstarre, Bewusstseinsstörungen, starkem Schwitzen und beschleunigter Atmung sowie Störungen der Bildung weißer Blutkörperchen (Agranulozytose).
Bestimmte Neuroleptika dürfen unter anderem nicht eingenommen werden bei einigen Blutbildveränderungen (z. B. Clozapin), Hirnerkrankungen, akuten Vergiftungen, bestimmten Herzerkrankungen sowie bei schweren Leber- und Nierenschäden. Die Einnahme von Neuroleptika zusammen mit Alkohol oder Beruhigungsmitteln kann zu einer gefährlichen Wirkungsverstärkung führen. Tee, Kaffee und andere koffeinhaltige Getränke können die Wirkung von Neuroleptika verringern. Durch Neuroleptika kann es zu einer Beeinträchtigung des Reaktionsvermögens kommen. Die Fahrtüchtigkeit kann eingeschränkt sein, und es kann zu einer Gefährdung am Arbeitsplatz (zum Beispiel beim Bedienen von Maschinen) kommen.
Antipsychotika schränken Problemlösen[42] und Lernen[43] ein. Sie werden mit der Entstehung von Hypophysentumoren in Verbindung gebracht[44] und können im Alter zu Stürzen führen. Nach Auswertungen mehrerer Studien (Metaanalysen)[45][46] führt die Verabreichung von Antipsychotika bei dementiellen Patienten zu einem erhöhten Mortalitätsrisiko im Vergleich zur Placeboverabreichung.
Psychische Nebenwirkungen: Bei 10 – 60 % der mit typischen Neuroleptika Behandelten kommt es zu pharmakogener Anhedonie[47] oder Dysphorie.[48][49][50] Auch bei Atypika treten diese Nebenwirkungen auf, allerdings weniger häufig.[51]
Lebenserwartung
[Bearbeiten | Quelltext bearbeiten]Der Einfluss von Antipsychotika auf die Lebenserwartung ist umstritten. So erklärte Friedrich Walburg, Vorsitzender der Deutschen Gesellschaft für Soziale Psychiatrie (DGSP), 2007:[52] „Anders als häufig angenommen, erhöhen Neuroleptika aber die Lebenserwartung der Patienten nicht. Vielmehr sinkt sie sogar.“
Eine finnische Studie von 2009, die 66881 Schizophreniepatienten in Finnland umfasste und über elf Jahre (1996–2006) lief, konnte jedoch zeigen, dass Patienten mit einer schizophrenen Erkrankung länger lebten, wenn sie antipsychotisch behandelt wurden.[53]
Neuroleptikadebatte
[Bearbeiten | Quelltext bearbeiten]Auch innerhalb der Psychiatrie gibt es eine andauernde Debatte über die Vor- und Nachteile der Neuroleptika, die als Neuroleptikadebatte in den Medien bekannt geworden ist. Die Deutsche Gesellschaft für Soziale Psychiatrie hat dazu eine eigene Informationsseite, die mit neuen Informationen aktualisiert wird.[54] Die Soteria Bewegung versucht mit wenig oder keinen Neuroleptika die Schizophrenie zu behandeln.
Chemie
[Bearbeiten | Quelltext bearbeiten]Trizyklische Neuroleptika (Phenothiazine und Thioxanthene)
[Bearbeiten | Quelltext bearbeiten]
Seit den 1950er-Jahren finden die trizyklischen Neuroleptika therapeutische Anwendung. Sie besitzen ein trizyklisches Phenothiazin- (Phenothiazine: zum Beispiel Chlorpromazin, Fluphenazin, Levomepromazin, Prothipendyl, Perazin, Promazin, Thioridazin und Triflupromazin) oder Thioxanthenringsystem (Thioxanthene: zum Beispiel Chlorprothixen und Flupentixol). Das trizyklische Promethazin war zudem das erste therapeutisch genutzte Antihistaminikum. Strukturell ähneln trizyklische Neuroleptika weitgehend den trizyklischen Antidepressiva. Unterschiede in der pharmakologischen Wirkung zwischen beiden Substanzklassen werden mit einer voneinander abweichenden dreidimensionalen Konformation des trizyklischen Ringsystems in Verbindung gebracht.
Dibenzepine
[Bearbeiten | Quelltext bearbeiten]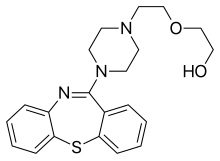
Von den älteren trizyklischen Neuroleptika sind die neueren trizyklischen Dibenzepine (zum Beispiel Clozapin, Olanzapin, Quetiapin und Zotepin) abzugrenzen. Sie verfügen über ein Dibenzothiepin- (Zotepin), Dibenzodiazepin- (Clozapin), Thienobenzodiazepin- (Olanzapin) oder ein Dibenzothiazepin-Ringsystem (Quetiapin), welche eine von den klassischen trizyklischen Neuroleptika abweichende dreidimensionale Anordnung besitzen und somit für deren abweichende (atypische) pharmakologische Wirkung verantwortlich sind.
Butyrophenone und Diphenylbutylpiperidine
[Bearbeiten | Quelltext bearbeiten]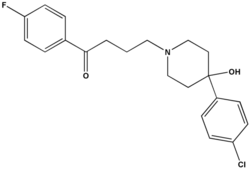
Die Butyrophenone (z. B. Haloperidol, Melperon, Bromperidol und Pipamperon) zeichnen sich chemisch durch einen 1-Phenyl-1-butanon-Baustein aus. Ausgehend vom Haloperidol wurden zahlreiche weitere Neuroleptika entwickelt, etwa das Spiperon mit klar erkennbarer Strukturverwandtschaft zu den Butyrophenonen. Therapeutische Anwendung finden auch die abgeleiteten Diphenylbutylpiperidine Fluspirilen und Pimozid.
Benzamide
[Bearbeiten | Quelltext bearbeiten]Eine Sonderstellung nehmen die Benzamide (Wirkstoffe Sulpirid und Amisulprid) ein, die außer einem neuroleptischen noch einen gewissen stimmungsaufhellenden, aktivierenden Effekt haben.
Benzisoxazol-Derivate, andere Stoffe
[Bearbeiten | Quelltext bearbeiten]Zwischen den Atypika Risperidon und Ziprasidon bestehen ebenfalls Strukturparallelen, sie können als entfernt mit Haloperidol verwandt betrachtet werden. Das neuere Aripiprazol weist einige Gemeinsamkeiten mit den älteren Substanzen auf. Während Risperidon besonders stark antipsychotisch wirkt, zeigt Ziprasidon noch einen Noradrenalin-spezifischen Effekt. Aripiprazol und Cariprazin sind Partialagonisten an Dopamin-Rezeptoren und unterscheiden sich dadurch von den meisten anderen Neuroleptika.
Alkaloide
[Bearbeiten | Quelltext bearbeiten]Das pentazyklische Rauvolfia-Alkaloid Reserpin hat in der Therapie der Schizophrenie nur noch historische Bedeutung.
Darreichungsformen
[Bearbeiten | Quelltext bearbeiten]
Neuroleptika werden in verschiedenen Darreichungsformen angeboten. Am häufigsten ist dabei die orale Einnahme in Tablettenform, seltener in flüssiger Form als Tropfen oder Saft. Flüssige Präparate sind zumeist teurer, haben aber den Vorteil einer besseren Resorption im Magen-Darm-Trakt, auch kann bei unkooperativen Patienten die Einnahme besser kontrolliert werden.[55] In psychiatrischen Kliniken und in der Notfallmedizin werden Neuroleptika auch intravenös verabreicht, um etwa in Krisensituationen einen schnelleren Wirkungseintritt herbeizuführen.
Für die Langzeittherapie existieren sogenannte Depotpräparate, die mit einer Spritze intramuskulär verabreicht werden. Die Bezeichnung „Depot“ kommt daher, dass der injizierte Wirkstoff im Muskelgewebe gespeichert bleibt und von dort langsam in den Blutkreislauf abgegeben wird. Eine Auffrischung der Dosis ist erst nach mehreren Wochen nötig, wenn das Depot erschöpft ist. Dadurch erhöht sich die tendenziell geringe Compliance von Neuroleptika-Patienten, da ein Vergessen oder eigenmächtiges Absetzen der Medikation für diesen Zeitraum ausgeschlossen wird. Depotpräparate besitzen im Vergleich zur oralen und intravenösen Verabreichung pharmakokinetische Vorteile wie eine bessere Verfügbarkeit und durch die langsame, kontinuierliche Freisetzung des Wirkstoffes im Blut einen stabileren Plasmaspiegel, wodurch Nebenwirkungen verringert werden können.[56]
Im Rahmen einer Zwangsbehandlung können Neuroleptika in psychiatrischen Kliniken unter bestimmten Voraussetzungen auch gegen den Willen des Patienten verabreicht werden. Hierbei kommen häufig injizierbare Präparate zum Einsatz, da zur oralen Einnahme bestimmte Präparate von unkooperativen Patienten ausgespuckt oder im Mund versteckt werden können.
Klassifizierung
[Bearbeiten | Quelltext bearbeiten]Hoch- und niederpotente Neuroleptika
[Bearbeiten | Quelltext bearbeiten]Klassische Neuroleptika wurden hinsichtlich ihres Wirkungsspektrums früher in sogenannte hoch- und niederpotente Wirkstoffe eingeteilt. Die Potenz ist ein Maß für die antipsychotische Wirksamkeit eines Wirkstoffs bezogen auf die Menge. Jeder Wirkstoff hat sowohl eine antipsychotische (den Realitätsverlust bekämpfende) als auch eine sedierende (beruhigende) Wirkkomponente, die jeweils unterschiedlich stark ausgeprägt ist. Ebenso unterscheiden sich die Abbruchraten einer medikamentösen Behandlung aufgrund der jeweiligen Nebenwirkungen. Antipsychotische Neuroleptika wirken hauptsächlich antipsychotisch und weniger sedierend. Sie eignen sich besonders zur Behandlung von sogenannten Positivsymptomen wie Wahn und Halluzinationen. Bei den sedierenden Stoffen ist es umgekehrt, sie wirken hauptsächlich sedierend und kaum antipsychotisch. Daher werden sie bei Symptomen wie Unruhe, Angst, Schlafstörungen und Erregungszuständen verabreicht.[4] Auch eine kombinierte Einnahme ist möglich. Häufig bei der Behandlung einer akuten Psychose ist beispielsweise die tägliche Gabe eines antipsychotisch wirksamen Stoffes, während ein sedierendes Präparat bei Bedarf zusätzlich eingenommen werden kann.[2] Eine Meta-Analyse aus dem Jahr 2013 über 15 Neuroleptika schlug eine feinere Einteilung nach der jeweiligen Indikation und Wirksamkeit vor.[57]
Zur Einteilung der Wirkstoffe in hoch- und niederpotent kann man ihre sogenannte Äquivalenzdosis heranziehen. Die Äquivalenzdosis ist ein Maß für die antipsychotische Wirksamkeit einer Substanz und wird mit der Einheit Chlorpromazin-Äquivalent (CPZ) angegeben. Als Referenzwert von 1 wurde Chlorpromazin festgelegt, der erste als Neuroleptikum verwendete Wirkstoff. Ein Wirkstoff mit einem CPZ von 2 ist doppelt so stark antipsychotisch wirksam wie Chlorpromazin.[25]
Das Konzept der Äquivalenzdosis ist vor allem im Zusammenhang mit den typischen Neuroleptika von Bedeutung, da sich diese in ihrer Wirkungsweise und den auftretenden Nebenwirkungen ähneln. Sie unterscheiden sich hauptsächlich in ihrem Verhältnis von sedierender zu antipsychotischer Wirkung. Die atypischen Neuroleptika unterscheiden sich wesentlich stärker hinsichtlich ihrer Wirkungsweise, Nebenwirkungen und Einsatzgebiete, wodurch ein direkter Vergleich mittels einer Äquivalenzdosis an Bedeutung verliert.[58]
Die Einteilung der Wirkstoffe (nach Möller, 2001) wird anhand ihrer Chlorpromazin-Äquivalenzdosis vorgenommen:
- niederpotente Neuroleptika (CPZi ≤ 1,0) Diese Substanzen haben keine „antipsychotischen“ Eigenschaften
- Beispiele: Promethazin, Levomepromazin, Thioridazin, Promazin
- mittelpotente Neuroleptika (CPZi = 1,0–10,0)
- Beispiele: Chlorpromazin, Perazin, Zuclopenthixol
- hochpotente Neuroleptika (CPZi > 10,0)
- Beispiele: Perphenazin, Fluphenazin, Haloperidol, Benperidol
| Neuroleptikum (Arzneistoff) |
Stoffklasse | CPZ- Äquivalent X |
mittlere (–max.) Dosis je Tag in mg |
Handelsname(n) |
|---|---|---|---|---|
| Hochpotente N.: | ||||
| Benperidol | Butyrophenon | 75 | 1,5–20 (–40) | Glianimon |
| Haloperidol | Butyrophenon | 50 | 1,5–20 (–100) | Haldol |
| Bromperidol | Butyrophenon | 50 | 5–20 (–50) | Impromen |
| Flupentixol | Thioxanthen | 50 | 3–20 (–60) | Fluanxol |
| Fluspirilen | DPBP | 50 | 1,5–10 mg/Wo. (max.) | Imap |
| Olanzapin | Thienobenzodiazepin | 50 | 5–30 (max.) | Zyprexa |
| Pimozid | DPBP | 50 | 1–4 (–16) | Orap |
| Risperidon | Benzisoxazolderivat | 50 | 2–8 (–16) | Risperdal |
| Fluphenazin | Phenothiazin | 40 | 2,5–20 (–40) | Lyogen |
| Trifluoperazin | Phenothiazin | 25 | 1–6 (–20) | |
| Perphenazin | Phenothiazin | 15 | 4–24 (–48) | Decentan |
| Mittelpotente N.: | ||||
| Zuclopenthixol | Thioxanthen | 5 | 20–40 (–80) | Clopixol |
| Clopenthixol | Thioxanthen | 2,5 | 25–150 (–300) | |
| Chlorpromazin | Phenothiazin | 1 | 25–400 (–800) | |
| Clozapin | Dibenzodiazepin | 1 | 12,5–450 (–900) | Leponex |
| Melperon | Butyrophenon | 1 | 25–300 (–600) | Eunerpan |
| Perazin | Phenothiazin | 1 | 75–600 (–800) | Taxilan |
| Quetiapin | Dibenzothiazepin | 1 | 150–750 (max.) | Seroquel |
| Thioridazin | Phenothiazin | 1 | 25–300 (–600) | |
| Niedrigpotente N.: | ||||
| Pipamperon | Butyrophenon | 0,8 | 40–360 (max.) | Dipiperon |
| Triflupromazin | Phenothiazin | 0,8 | 10–150 (–600) | Psyquil |
| Chlorprothixen | Thioxanthen | 0,8 | 100–420 (–800) | Truxal |
| Prothipendyl | Azaphenothiazin | 0,7 | 40–320 (max.) | Dominal |
| Levomepromazin | Phenothiazin | 0,5 | 25–300 (–600) | Neurocil |
| Promazin | Phenothiazin | 0,5 | 25–150 (–1.000) | Prazine |
| Promethazin | Phenothiazin | 0,5 | 50–300 (–1.200) | Atosil |
| Amisulprid | Benzamid | 0,2 | 50–1.200 (max.) | Solian |
| Sulpirid | Benzamid | 0,2 | 200–1.600 (–3.200) | Dogmatil |
(Modifiziert nach Möller 2001, S. 243)
Typische und atypische Neuroleptika
[Bearbeiten | Quelltext bearbeiten]
Die Neuroleptika der ersten Generation, auch als typische Neuroleptika bezeichnet, sind bei 30–40 % der Patienten unwirksam.[20] Außerdem verursachten sie neben der erwünschten antipsychotischen Wirkung eine Reihe von Nebenwirkungen, darunter das sogenannte extrapyramidale Syndrom. Dabei handelt es sich um Störungen der Bewegungsabläufe, die sich beispielsweise in Form einer Sitzunruhe oder einer Muskelstarrheit ähnlich wie bei Parkinson-Erkrankten äußern. Je stärker ein typisches Neuroleptikum antipsychotisch wirkt, desto stärker sind auch diese Nebenwirkungen. Zudem wirken die typischen Neuroleptika nicht gegen die sogenannten Negativsymptome der Schizophrenie und können diese sogar verschlimmern.
Die neueren, sogenannten atypischen Neuroleptika zeichnen sich dadurch aus, dass sie in wesentlich geringerem Maße extrapyramidalmotorische Nebenwirkungen verursachen.[28][29] Sie lösten die typischen Neuroleptika als Mittel der ersten Wahl ab[59] und wirken häufig auch bei Patienten, die auf die bisherigen Medikamente nicht ansprechen.[28][20][29] Zudem wirken sie auch auf die sogenannten Negativsymptome der Schizophrenie.[20][29] Den atypischen Neuroleptika wird ein insgesamt günstigeres Nebenwirkungsprofil zugeschrieben, was sich positiv auf die vergleichsweise geringe Compliance von Neuroleptika-Patienten auswirkt. Im Gegenzug können sie jedoch andere, neue Nebenwirkungen wie starke Gewichtszunahme aufweisen.[39]
Die Unterschiede zwischen typischen und atypischen Präparaten wurden durch eine Vielzahl an vergleichenden Studien untersucht.[60][61][62][63][64] Im Jahre 2009 wurde eine deutschlandweite, durch das Bundesministerium für Bildung und Forschung geförderte Studie ins Leben gerufen, die häufig verschriebene atypische Neuroleptika hinsichtlich Wirksamkeit und Nebenwirkungsprofil mit klassischen Neuroleptika vergleicht und bis heute andauert.[65]
Kritisiert wird das Kosten-Nutzen-Verhältnis moderner atypischer Neuroleptika.[66][29] Die neuesten Präparate sind deutlich teurer als diejenigen, die aufgrund des abgelaufenen Patentschutzes als Generika verfügbar sind. Atypische Neuroleptika machten 2011 in Deutschland etwa die Hälfte aller verschriebenen Neuroleptika aus, waren aber für 87 % der erzielten Umsätze verantwortlich.[67] Laut einem von der Barmer GEK veröffentlichten Arzneimittelreport waren im Jahr 2011 unter den 20 am meisten Kosten verursachenden Präparaten mit Seroquel und Zyprexa zwei atypische Neuroleptika vertreten.[68] Der Arzneiverordnungs-Report 2012 kritisiert die hohen Kosten einiger atypischen Präparate und ist der Ansicht, dass ältere, jedoch ähnlich gut wirksame Alternativen zur Verfügung stehen, deren Verwendung deutliche Einsparungen ermöglichen würden.[69]
Wirtschaftliche Bedeutung
[Bearbeiten | Quelltext bearbeiten]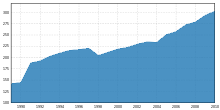
Neuroleptika sind heute nach den Antidepressiva die am häufigsten verordneten Psychopharmaka, bei den erzielten Umsätzen liegen sie sogar an erster Stelle.[70] Bei der Behandlung der Schizophrenie gelten sie heute als Mittel der Wahl.[23] Aber auch als Beruhigungsmittel sind sie verbreitet, etwa im Bereich der Altenpflege.[3] Etwa 30–40 % der Bewohner in Altenheimen erhalten Neuroleptika.[5][6]
Präventivbehandlung
[Bearbeiten | Quelltext bearbeiten]Bisherigen Studienergebnissen zufolge verringert eine präventive Langzeitbehandlung mit Neuroleptika bei Schizophreniekranken die Wahrscheinlichkeit, einen Rückfall zu erleiden.[71] Einer anderen Studie zufolge können jedoch Schizophreniekranke, die nicht mit Neuroleptika behandelt werden, unter Umständen weniger psychotische Rezidive erleiden als solche, die regelmäßig Neuroleptika einnehmen. Personeninterne Faktoren beeinflussen die Wahrscheinlichkeit, ein Rezidiv zu erleiden, möglicherweise stärker als die Verlässlichkeit der Medikamenteneinnahme.[72]
Literatur
[Bearbeiten | Quelltext bearbeiten]- Hans Bangen: Geschichte der medikamentösen Therapie der Schizophrenie. VWB, Verlag für Wissenschaft und Bildung, Berlin 1992, ISBN 3-927408-82-4.
- Hans-Jürgen Möller u. a.: Psychopharmakotherapie. 2. Auflage. Kohlhammer, Stuttgart 2000, ISBN 3-17-014297-6.
- Otto Benkert, Hanns Hippius: Psychiatrische Pharmakotherapie. Springer, Berlin u. a. 1996, ISBN 3-540-58149-9.
- Klaus Windgassen, Olaf Bick: Fortschritte in der neuroleptischen Schizophreniebehandlung: Neuroleptika der zweiten Generation.
- Barbara Dieckmann, Margret Osterfeld, Nils Greeve: Gewichtszunahme unter Neuroleptika. In: Psychosoziale Umschau. April 2004. Artikel über Gewichtszunahme durch Neuroleptika sowie deren Folgen und Risiken.
- R. B. Mailman, V. Murthy: Third generation antipsychotic drugs: partial agonism or receptor functional selectivity? In: Curr. Pharm. Des. Band 16, Nr. 5, 2010, S. 488–501, PMID 19909227, PMC 2958217 (freier Volltext) – (englisch).
- J. A. Allen, J. M. Yost, V. Setola u. a.: Discovery of β-arrestin-biased dopamine D2 ligands for probing signal transduction pathways essential for antipsychotic efficacy. In: Proc. Natl. Acad. Sci. U.S.A. Band 108, Nr. 45, 2011, S. 18488–18493, doi:10.1073/pnas.1104807108, PMID 22025698, PMC 3215024 (freier Volltext) – (englisch).
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Frank Meyer, Katrin Jahnsen, Gerd Glaeske: Arzneimittelreport 2005 über Neuroleptika. Artikel über Neuroleptika und Dyskinesien
- Laut Studien wirkt Omega 3 genauso gut gegen Psychosen wie Neuroleptika:
- Übersichtsartikel: Tran statt Wahn.
- Vollständige Studie auf Englisch: Long-Chain Omega-3 Fatty Acids for Indicated Prevention of Psychotic Disorders
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Roland Depner: Alles Nervensache? Wie unser Nervensystem funktioniert – oder auch nicht. Schattauer, Stuttgart 2012, ISBN 978-3-7945-2887-5, S. 106 (Volltext/Vorschau in der Google-Buchsuche).
- ↑ a b Gerd Laux, Otto Dietmaier: Psychopharmaka. Springer, Heidelberg 2009, ISBN 978-3-540-68288-2, S. 92.
- ↑ a b Ulrich Schwabe, Dieter Paffrath: Arzneiverordnungs-Report 2011. 2011, ISBN 978-3-642-21991-7, S. 833.
- ↑ a b Peter Riederer, Gerd Laux, Walter Pöldinger: Neuro-Psychopharmaka – Ein Therapie-Handbuch. 2. Auflage. Band 4: Neuroleptika. Springer, 1998, ISBN 3-211-82943-1, S. 28 (Volltext/Vorschau in der Google-Buchsuche).
- ↑ a b Stefan Georg Schröder: Psychopathologie der Demenz. Schattauer, Stuttgart 2006, ISBN 3-7945-2151-X, S. 118.
- ↑ a b Landespräventionsrat Nordrhein-Westfalen: Alter – ein Risiko? LIT Verlag, Münster 2005, ISBN 3-8258-8803-7, S. 91.
- ↑ T. Pringsheim, M. Pearce: Complications of antipsychotic therapy in children with tourette syndrome. PMID 20682197
- ↑ K. Komossa, A. M. Depping, M. Meyer, W. Kissling, S. Leucht: Second-generation antipsychotics for obsessive compulsive disorder. PMID 21154394
- ↑ J. Chen, K. Gao, D. E. Kemp: Second-generation antipsychotics in major depressive disorder: update and clinical perspective. PMID 21088586
- ↑ Klaus Schmeck, Susanne Schlüter-Müller: Persönlichkeitsstörungen im Jugendalter. Springer, 2008, ISBN 978-3-540-20933-1, S. 95.
- ↑ Nele Langosch: Schaden Psychopharmaka Kindern und Jugendlichen? Spektrum.de, 9. Oktober 2015, abgerufen am 16. Oktober 2015.
- ↑ David J. Posey, Kimberly A. Stigler, Craig A. Erickson, Christopher J. McDougle: Antipsychotics in the treatment of autism. PMC 2171144 (freier Volltext)
- ↑ Hans Bangen: Geschichte der medikamentösen Therapie der Schizophrenie. Berlin 1992, ISBN 3-927408-82-4, S. 134–136.
- ↑ Neurolepsie. In: Uwe Henrik Peters: Wörterbuch der Psychiatrie und medizinischen Psychologie. 3. Auflage. Urban & Schwarzenberg, München 1984, S. 370.
- ↑ Hans Bangen: Geschichte der medikamentösen Therapie der Schizophrenie. Berlin 1992, ISBN 3-927408-82-4, S. 92.
- ↑ Jack A. Gottschalk: Book Section: Essays and Review: Brain Disabling Treatments in Psychiatry, Second Edition. In: The Journal of Psychiatry & Law. Band 37, Nr. 4, Dezember 2009, S. 489–492, doi:10.1177/009318530903700417 (englisch).
- ↑ a b Sandra Caponi: On the so-called psychopharmacological revolution: the discovery of chlorpromazine and the management of madness. In: História, Ciências, Saúde-Manguinhos. Band 28, 3. September 2021, S. 661–683, doi:10.1590/S0104-59702021000300003 (englisch, scielo.br [abgerufen am 23. November 2021]).
- ↑ Vgl. auch www.spiegel.de.
- ↑ Bei Angst-Spannungs-Zuständen. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. XL.
- ↑ a b c d e f g Frank Theisen, Helmut Remschmidt: Schizophrenie – Manuale psychischer Störungen bei Kindern und Jugendlichen. 2011, ISBN 978-3-540-20946-1, S. 150.
- ↑ Christoph Lanzendorfer, Joachim Scholz: Psychopharmaka. Springer, Berlin/ Heidelberg 1995, ISBN 3-642-57779-2, S. 118.
- ↑ Elisabeth Höwler: Gerontopsychiatrische Pflege. Schlütersche, Hannover 2004, ISBN 3-89993-411-3, S. 15.
- ↑ a b Wolfgang Gaebel, Peter Falkai: Behandlungsleitlinie Schizophrenie. 2006, ISBN 3-7985-1493-3, S. 195.
- ↑ a b c d Ulrich Hegerl: Neurophysiologische Untersuchungen in der Psychiatrie. 1998, ISBN 3-211-83171-1, S. 183 (Volltext/Vorschau in der Google-Buchsuche).
- ↑ a b c d Wolfgang Gaebel, Peter Falkai: Behandlungsleitlinie Schizophrenie. 2006, ISBN 3-7985-1493-3, S. 46.
- ↑ Hans-Joachim Haase, Paul Adriaan Jan Janssen: The action of neuroleptic drugs: a psychiatric, neurologic and pharmacological investigation. North-Holland, Amsterdam 1965.
- ↑ Edward Shorter: A historical dictionary of psychiatry. Oxford University Press, New York 2005, ISBN 0-19-517668-5, S. 55.
- ↑ a b c d e Harald Schmidt, Claus-Jürgen Estler: Pharmakologie und Toxikologie. Schattauer, Stuttgart 2007, ISBN 978-3-7945-2295-8, S. 229.
- ↑ a b c d e f g Borwin Bandelow, Oliver Gruber, Peter Falkai: Kurzlehrbuch Psychiatrie. Steinkopff, [Berlin] 2008, ISBN 978-3-7985-1835-3, S. 236.
- ↑ Frank Theisen, Helmut Remschmidt: Schizophrenie – Manuale psychischer Störungen bei Kindern und Jugendlichen. 2011, ISBN 978-3-540-20946-1, S. 165.
- ↑ a b Neel L. Burton: Der Sinn des Wahnsinns – Psychische Störungen verstehen. Spektrum, Akademischer Verlag, Heidelberg 2011, ISBN 978-3-8274-2773-1, S. 63–65 (Volltext/Vorschau in der Google-Buchsuche).
- ↑ a b c Wielant Machleidt, Manfred Bauer, Friedhelm Lamprecht, Hans K. Rose, Christa Rohde-Dachser: Psychiatrie, Psychosomatik und Psychotherapie. Thieme, Stuttgart 2004, ISBN 3-13-495607-1, S. 333 (Volltext/Vorschau in der Google-Buchsuche).
- ↑ Torsten Kratz, Albert Diefenbacher: Psychopharmakotherapie im Alter. Vermeidung von Arzneimittelinteraktionen und Polypharmazie. In: Deutsches Ärzteblatt International. Band 116, Nr. 29, 22. Juli 2019, S. 508–517, S. 515, doi:10.3238/arztebl.2019.0508.
- ↑ Stefan Schwab (Hrsg.): NeuroIntensiv. Springer-Medizin-Verlag, Heidelberg 2012, ISBN 978-3-642-16910-6, S. 286.
- ↑ Hans-Jürgen Möller: Therapie psychischer Erkrankungen. 2006, ISBN 3-13-117663-6, S. 231.
- ↑ B. K. Puri: Brain tissue changes and antipsychotic medication. In: Expert Rev Neurother. Band 11, 2011, S. 943–946, PMID 21721911 (englisch).
- ↑ V. Aderhold, S. Weinmann, C. Hägele, A. Heinz: Frontale Hirnvolumenminderung durch Antipsychotika? In: Der Nervenarzt. Band 86, 2015, S. 302–323, doi:10.1007/s00115-014-4027-5.
- ↑ Martina Lenzen-Schulte: Neuroleptika: Wenn Psychopillen das Gehirn schrumpfen lassen. In: FAZ. 26. Januar 2015, abgerufen am 30. Januar 2015.
- ↑ a b Frank Theisen, Helmut Remschmidt: Schizophrenie – Manuale psychischer Störungen bei Kindern und Jugendlichen. 2011, ISBN 978-3-540-20946-1, S. 159.
- ↑ C. Parker, C. Coupland, J. Hippisley-Cox: Antipsychotic drugs and risk of venous thromboembolism: nested case-control study. In: BMJ (British Medical Journal). Band 341, 2010, S. c4245, PMID 20858909 (englisch).
- ↑ Torsten Kratz, Albert Diefenbacher: Psychopharmakotherapie im Alter. Vermeidung von Arzneimittelinteraktionen und Polypharmazie. In: Deutsches Ärzteblatt. Band 116, Heft 29 f. (22. Juli) 2019, S. 508–517, hier S. 511.
- ↑ J. I. Wasserman, R. J. Barry, L. Bradford, N. J. Delva, R. J. Beninger: Probabilistic classification and gambling in patients with schizophrenia receiving medication: comparison of risperidone, olanzapine, clozapine and typical antipsychotics. In: Psychopharmacology (Berl). 2012, PMID 22237855 (englisch).
- ↑ M. S. Harris, C. L. Wiseman, J. L. Reilly, M. S. Keshavan, J. A. Sweeney: Effects of risperidone on procedural learning in antipsychotic-naive first-episode schizophrenia. In: Neuropsychopharmacology. 2009, PMID 18536701 (englisch).
- ↑ J. I. Wasserman, R. J. Barry, L. Bradford, N. J. Delva, R. J. Beninger: Atypical antipsychotics and pituitary tumors: a pharmacovigilance study. In: Pharmacotherapy. 2006, PMID 16716128 (englisch).
- ↑ L. S. Schneider, K. S. Dagerman, P. Insel: Risk of death with atypical antipsychotic drug treatment for dementia: meta-analysis of randomized placebo-controlled trials. In: JAMA. Band 294, Nr. 15, 2005, S. 1934–1943, doi:10.1001/jama.294.15.1934, PMID 16234500 (englisch).
- ↑ C. Ballard, L. Waite: The effectiveness of atypical antipsychotics for the treatment of aggression and psychosis in Alzheimer's disease. In: Cochrane Database Syst Rev. Nr. 1, 2006, Artikel CD003476, doi:10.1002/14651858.CD003476.pub2, PMID 16437455 (englisch).
- ↑ L. Voruganti, A. G. Awad: Neuroleptic dysphoria: towards a new synthesis. In: Psychopharmacology. Band 171, 2004, S. 121–132.
- ↑ A. G. Awad, L. N. P. Voruganti: Neuroleptic dysphoria: revisiting the concept 50 years later. In: Acta Psychiatr. Scand. Band 111, Suppl. 427, 2005, S. 6–13.
- ↑ Martin Harrow, Cynthia A. Yonan, James R. Sands, Joanne Marengo: Depression in Schizophrenia: Are Neuroleptics, Akinesia or Anhedonia Involved? In: Schizophrenia Bulletin. Vol. 20, No. 2, 1994.
- ↑ Nev Jones: Antipsychotic Medications, Psychological Side Effects and Treatment Engagement. In: Issues in Mental Health Nursing. Band 33, 2012, S. 492–493.
- ↑ A. G. Awad, LNP Voruganti: Neuroleptic dysphoria: revisiting the concept 50 years later. In: Acta Psychiatr. Scand. Band 111, Suppl. 427, 2005, S. 6–13.
- ↑ Zu viele Psychopillen senken die Lebenserwartung. welt.de, 25. September 2009.
- ↑ J. Tiihonen, J. Lönnqvist, K. Wahlbeck, T. Klaukka, L. Niskanen, A. Tanskanen, J. Haukka: 11-year follow-up of mortality in patients with schizophrenia: a population-based cohort study (FIN11 study). In: Lancet. Band 374, Nr. 9690, Aug 2009, S. 620–627. PMID 19595447.
- ↑ Neuroleptikadebatte. Deutsche Gesellschaft für Soziale Psychiatrie, abgerufen am 19. Juli 2019.
- ↑ Peter Riederer, Gerd Laux, Walter Pöldinger: Neuro-Psychopharmaka: Ein Therapie-Handbuch. Band 4: Neuroleptika. 2. Auflage. Springer Vienna, Vienna 1998, ISBN 3-211-82943-1, S. 209.
- ↑ Peter Riederer, Gerd Laux, Walter Pöldinger: Neuro-Psychopharmaka: Ein Therapie-Handbuch. 2. Auflage. Band 4: Neuroleptika. Springer Vienna, Vienna 1998, ISBN 3-7091-6458-3, S. 233.
- ↑ S. Leucht, A. Cipriani, L. Spineli, D. Mavridis, D. Orey, F. Richter, M. Samara, C. Barbui, R. R. Engel, J. R. Geddes, W. Kissling, M. P. Stapf, B. Lässig, G. Salanti, J. M. Davis: Comparative efficacy and tolerability of 15 antipsychotic drugs in schizophrenia: a multiple-treatments meta-analysis. In: Lancet. Band 382, Nummer 9896, September 2013, S. 951–962, doi:10.1016/S0140-6736(13)60733-3. PMID 23810019.
- ↑ Wolfgang Gaebel, Peter Falkai: Behandlungsleitlinie Schizophrenie. 2006, ISBN 3-7985-1493-3, S. 48.
- ↑ Frank Theisen, Helmut Remschmidt: Schizophrenie – Manuale psychischer Störungen bei Kindern und Jugendlichen. 2011, ISBN 978-3-540-20946-1, S. 165.
- ↑ T. Stargardt, S. Weinbrenner, R. Busse, G. Juckel, C. A. Gericke: Effectiveness and cost of atypical versus typical antipsychotic treatment for schizophrenia in routine care. PMID 18509216
- ↑ John Geddes, Nick Freemantle, Paul Harrison, Paul Bebbington: Atypical antipsychotics in the treatment of schizophrenia: systematic overview and meta-regression analysis. PMC 27538 (freier Volltext)
- ↑ C. Stanniland, D. Taylor: Tolerability of atypical antipsychotics. In: Drug safety. Band 22, Nr. 3, März 2000, S. 195–214. PMID 10738844. (Review).
- ↑ B. Luft, D. Taylor: A review of atypical antipsychotic drugs versus conventional medication in schizophrenia. PMID 16925501
- ↑ S. Leucht, G. Pitschel-Walz, D. Abraham, W. Kissling: Efficacy and extrapyramidal side-effects of the new antipsychotics olanzapine, quetiapine, risperidone, and sertindole compared to conventional antipsychotics and placebo. A meta-analysis of randomized controlled trials. PMID 9988841
- ↑ The Neuroleptic Strategy Study – NeSSy. Kompetenzzentrum für klinische Studien Bremen.
- ↑ Frank Theisen, Helmut Remschmidt: Schizophrenie – Manuale psychischer Störungen bei Kindern und Jugendlichen. 2011, ISBN 978-3-540-20946-1, S. 162.
- ↑ Jürgen Fritze: Psychopharmaka-Verordnungen: Ergebnisse und Kommentare zum Arzneiverordnungsreport 2011. In: Wissenschaftliche Verlagsgesellschaft Stuttgart (Hrsg.): Psychopharmakotherapie. Band 18, Nr. 6, 2011, S. 249, doi:10.1055/s-0032-1313192. PDF ( vom 16. Dezember 2014 im Internet Archive)
- ↑ BARMER GEK Arzneimittelreport 2012. (PDF; 377 kB). Barmer GEK, abgerufen am 25. Januar 2013.
- ↑ Markus Grill: Arzneiverordnungsreport 2012: Ein Drittel aller neuen Pillen ist überflüssig. In: Spiegel Online. abgerufen am 25. Januar 2013.
- ↑ Jürgen Fritze: Psychopharmaka-Verordnungen: Ergebnisse und Kommentare zum Arzneiverordnungsreport 2011. In: Wissenschaftliche Verlagsgesellschaft Stuttgart (Hrsg.): Psychopharmakotherapie. Band 18, Nr. 6, 2011, S. 246, doi:10.1055/s-0032-1313192. PDF ( vom 16. Dezember 2014 im Internet Archive)
- ↑ Peter Riederer, Gerd Laux, Walter Pöldinger: Neuro-Psychopharmaka – Ein Therapie-Handbuch. 2. Auflage. Band 4: Neuroleptika, 1998, ISBN 3-211-82943-1, S. 211.
- ↑ Martin Harrow, Thomas H. Jobe: Factors involved in outcome and recovery in schizophrenia patients not on antipsychotic medications: a 15-year multifollow-up study. 2007. PMID 17502806.