Zinkdithionit
Zur Navigation springen
Zur Suche springen
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
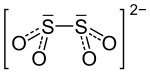
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Zinkdithionit | |||||||||||||||
| Andere Namen |
Zinkhydrosulfit | |||||||||||||||
| Summenformel | ZnS2O4 | |||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 193,45 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Löslichkeit |
löslich in Wasser[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Zinkdithionit (chem. Formel ZnS2O4) entsteht aus Schwefeldioxid oder Hydrogensulfiten durch Reduktion mit Zink.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Hergestellt wird es durch Einleiten von Schwefeldioxid in eine Wasser-Zinkstaub-Mischung.
oder
Verwendung
[Bearbeiten | Quelltext bearbeiten]Zinkdithionit wird als Bleichmittel in der Textil- und Papierindustrie eingesetzt. Dabei muss ein Kontakt mit Sauerstoff vermieden werden, da es von Sauerstoff oxidiert und unwirksam wird.[4]
Aus ökologischen Gründen (keine Belastung des Abwassers mit Zinksalzen) wird es vermehrt u. a. durch Natriumdithionit ersetzt.[5][6]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Datenblatt.
- ↑ Datenblatt bei NOAA (englisch).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Martin B. B. Hocking: Handbook of Chemical Technology and Pollution Control, 3rd Edition. Academic Press, 2006, ISBN 978-0-080-47827-2, S. 485 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry. 2nd ed., vol. 1, Academic Press 1963, S. 394–395.
- ↑ Bleiche (peroxygen-chemicals).
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Patent US3197289A: Modification of zinc hydrosulfite crystals by use of high molecular weight colloidal materials. Angemeldet am 11. Dezember 1961, veröffentlicht am 27. Juli 1965, Anmelder: Nopco Chem Co, Erfinder: Thomas E. Rogers.
- Kinetics of Zinc Hydrosulfite Slurry Reaction (PDF; 363 kB)


