1-Methoxy-1-buten-3-in
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1-Methoxy-1-buten-3-in | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C5H6O | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 82,10 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
0,906 g·cm−3[1] | ||||||||||||||||||
| Siedepunkt |
122–125 °C[1] | ||||||||||||||||||
| Brechungsindex |
1,4818 (bei 20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
1-Methoxy-1-buten-3-in ist eine chemische Verbindung aus der Stoffgruppe der Enolether und der Alkine. Sie wird aufgrund ihrer vielfältigen Reaktionsmöglichkeiten in der chemischen Technik zur Synthese verschiedener organischer Verbindungen verwendet.[3]
Herstellung
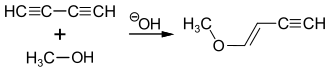
[Bearbeiten | Quelltext bearbeiten]Die Synthese von 1-Methoxy-1-buten-3-in erfolgt durch die exotherme Reaktion von Diacetylen mit Methanol.[3]
Die Reaktionsführung ist aufgrund der Instabilität von Diacetylen nicht einfach. Ein großtechnische Anlage mit einer Monatskapazität von 60 t zur Herstellung von 1-Methoxy-1-buten-3-in-Lösung in einem vollkontinuierliches Verfahren wurde 1964 von den Chemischen Werken Hüls errichtet. Dabei wird eine methanolische Diacetylenlösung mit einer 15- bis 20%igen Kaliumhydroxid-Lösung bei 100 °C und erhöhtem Druck in zwei hintereinandergeschalteten Röhrenreaktoren zu 1-Methoxy-1-buten-3-in umgesetzt.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Mit Schwefelsäure wird die Enolether-Gruppe von 1-Methoxy-1-buten-3-in gespalten und es bildet sich 3-Butinal.[4]
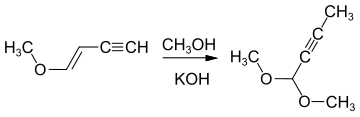
Durch die Umsetzung mit Methanol und Kaliumhydroxid ist das ungesättigte Acetal 1,1-Dimethoxy-2-butin[5] zugänglich.[6]
Die Addition von Wasser an 1,1-Dimethoxy-2-butin ergibt 4,4-Dimethoxy-2-butanon[7], ein Zwischenprodukt zur Herstellung von Pyrimidinen, Oxazolen und Pyrazolen.[8]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. 58. Auflage. CRC Press, West Palm Beach 1977, ISBN 0-8493-0458-X, S. C-232.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c G. Scharein: Verfahren zur Herstellung von 1-Methoxybuten-(1)-in-(3). In: Chemie Ingenieur Technik. Band 38, Nr. 10, 1966, S. 1021–1025, doi:10.1002/cite.330381002.
- ↑ Theo Herbertz: Studien zur Chemie der Acetylene, I. Mitteil.: Vom Diacetylen ausgehende Synthesen. In: Chemische Berichte. Band 85, Nr. 5, 1952, S. 475–482, doi:10.1002/cber.19520850526.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 1,1-Dimethoxy-2-butin: CAS-Nr.: 22022-34-0, PubChem: 557729, ChemSpider: 484841, Wikidata: Q82108868.
- ↑ Patent DE871006: Verfahren zur Herstellung von ungesättigten Acetalen. Angemeldet am 5. August 1942, veröffentlicht am 19. März 1953, Anmelder: Chemische Werke Hüls GmbH, Erfinder: Walter Franke, Karl Heinz Seemann.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 4,4-Dimethoxy-2-butanon: CAS-Nr.: 5436-21-5, EG-Nr.: 226-605-1, ECHA-InfoCard: 100.024.186, GESTIS: 494651, PubChem: 228548, ChemSpider: 198921, Wikidata: Q27236836.
- ↑ Walter Franke, Richard Kraft: Neuere Methoden der präparativen organischen Chemie II. Über Synthesen mit Acetessigaldehyd. In: Angewandte Chemie. Band 67, Nr. 14-15, 1955, S. 395–399, doi:10.1002/ange.19550671406.