2,2,4,4-Tetramethyl-1,3-cyclobutandiol
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
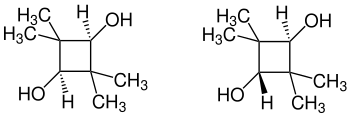
| ||||||||||||||||
| cis-Form (links), trans-Form | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 2,2,4,4-Tetramethyl-1,3-cyclobutandiol | |||||||||||||||
| Andere Namen |
CBDO | |||||||||||||||
| Summenformel | C8H16O2 | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 144,21 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
210–215 °C[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
2,2,4,4-Tetramethylcyclobutan-1,3-diol ist eine chemische Verbindung aus der Gruppe der Diole. Sie kommt in zwei isomeren Formen vor, der cis-Form und der trans-Form.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]2,2,4,4-Tetramethylcyclobutan-1,3-diol kann durch Umsetzung von Isobuttersäurechlorid mit Triethylamin gefolgt von der Hydrierung des erhaltenen 2,2,4,4-Tetramethylcyclobutan-1,3-dions gewonnen werden.[3][4]

Eigenschaften
[Bearbeiten | Quelltext bearbeiten]2,2,4,4-Tetramethylcyclobutan-1,3-diol ist ein weißer Feststoff.[1] Der C4-Ring des cis-Isomers der Verbindung ist nicht planar. Für einfache nicht-planare Cyclobutane liegen die Öffnungswinkel zwischen 19 und 31°. Das cis-Isomer von 2,2,4,4-Tetramethylcyclobutan-1,3-diol kristallisiert als zwei Konformere mit einem durchschnittlichen Öffnungswinkel von 17,5° aus.[5] Das trans-Isomer hat jedoch einen Öffnungswinkel von 0°.[6]
Verwendung
[Bearbeiten | Quelltext bearbeiten]2,2,4,4-Tetramethylcyclobutan-1,3-diol wird als Zwischenprodukt zur Herstellung von Polymeren verwendet, z. B. von Tritan.[7][8] Dabei kann es Bisphenol A ersetzen.[9]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Eintrag zu 2,2,4,4-Tetramethylcyclobutan-1,3-diol, Isomerengemisch in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Datenblatt 2,2,4,4-Tetramethyl-1,3-cyclobutanediol, mixture of isomers, 99% bei Sigma-Aldrich, abgerufen am 17. Oktober 2018 (PDF).
- ↑ E. Wedeking, W. Weisswange: Ueber die Synthese eines Diketons der Cyclobutanreihe. In: Berichte der deutschen chemischen Gesellschaft. 39, 1906, S. 1631, doi:10.1002/cber.19060390287.
- ↑ Houben-Weyl Methods of Organic Chemistry Vol. VI/1b, 4th Edition Alcohols III. Georg Thieme Verlag, 2014, ISBN 3-13-180044-5, S. 40 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ C. D. Shirrell, D. E. Williams: The crystal and molecular structure of cis-2,2,4,4-tetramethyl-1,3-cyclobutanediol. In: Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 32, 1976, S. 1867, doi:10.1107/S0567740876006559.
- ↑ T. N. Margulis: Planar cyclobutanes: structure of 2,2,4,4-tetramethyl-cyclobutane-trans-1,3-diol. In: Journal of the Chemical Society D: Chemical Communications. 1969, S. 215, doi:10.1039/C29690000215.
- ↑ Donald R. Kelsey, Betty M. Scardino, Janusz S. Grebowicz, Hoe H. Chuah: High Impact, Amorphous Terephthalate Copolyesters of Rigid 2,2,4,4-Tetramethyl-1,3-cyclobutanediol with Flexible Diols, Macromolecules, 2000, 33 (16), S. 5810–5818, doi:10.1021/ma000223+.
- ↑ Patent US5955565A: Polyesters from terephthalic acid, 2,2,4,4-tetramethyl-1,3-cyclobutanediol and ethylene glycol. Angemeldet am 23. Dezember 1997, veröffentlicht am 21. September 1999, Anmelder: Eastman Chemical Company, Erfinder: John C. Morris, James R. Bradley.
- ↑ Wolfgang Kaiser: Kunststoffchemie für Ingenieure Von der Synthese bis zur Anwendung. Carl Hanser Verlag GmbH Co KG, 2015, ISBN 978-3-446-44774-5, S. 345 (eingeschränkte Vorschau in der Google-Buchsuche).
