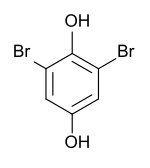
2,6-Dibromhydrochinon
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,6-Dibromhydrochinon | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H4Br2O2 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 267,90 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
löslich in Ethanol und Diethylether, schwer löslich in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
2,6-Dibromhydrochinon ist eine chemische Verbindung, die sowohl zu den Polyphenolen als auch zu den Halogenaromaten gehört. Sie ist zusammen mit 2,3-Dibromhydrochinon und 2,5-Dibromhydrochinon eines der drei stellungsisomeren Dibromhydrochinone.
Darstellung
[Bearbeiten | Quelltext bearbeiten]2,6-Dibromhydrochinon kann in einer mehrstufigen Reaktion aus Phenol hergestellt werden. Zunächst wird Phenol mit einem Überschuss von Brom behandelt, dabei bildet sich über 2,4,6-Tribromphenol als Zwischenstufe 2,4,4,6-Tetrabrom-2,5-cyclohexadienon (Trivialname: Tribromphenolbrom). Dieses wird mit rauchender Salpetersäure oxidiert, dabei bildet sich 2,6-Dibromchinon, das mit Schwefliger Säure zum 2,6-Dibromhydrochinon reduziert werden kann.[4]

Derivate
[Bearbeiten | Quelltext bearbeiten]Die Nitrierung von 2,6-Dibromhydrochinon mit Salpetersäure verläuft im Gegensatz zum 2,5-Dibromhydrochinon glatt, es bildet sich 2,6-Dibrom-3,5-dinitrohydrochinon.[4]

Durch Reaktion mit Dimethylsulfat entsteht der Dimethylether, der einen Schmelzpunkt von 56 °C hat und unter der CAS-Nummer 74076-59-8 registriert ist.[1]

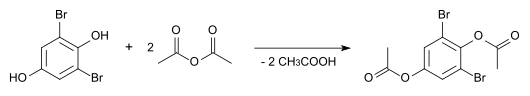
Das Diacetat, das durch Esterbildung mit Essigsäureanhydrid dargestellt werden kann, hat einen Schmelzpunkt von 116,5 °C.[1]
Durch Reaktion mit Chloracetonitril entsteht das 2,6-Dibrom-4-hydroxyphenoxyacetonitril mit einem Schmelzpunkt von 166–167 °C.[5]
Vorkommen in der Natur
[Bearbeiten | Quelltext bearbeiten]2,6-Dibromhydrochinon ist ein Zwischenprodukt im biologischen Abbau des Herbizids Bromoxynil.[6]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c J. Buckingham: Dictionary of Organic Compounds. CRC Press, ISBN 978-0-412-54090-5, S. 1914 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ D. A. Hystazarin: "Dictionary of organic compounds", Volume 2. Oxford University Press 1953. Volltext
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b M. Kohn, L. W. Guttmann: "Zur Kenntnis der Bromsubstitutionsprodukte des Hydrochinons. VII. Mitteilung über Bromphenole" in Monatshefte für Chemie 1924, 45(10), S. 573–588. doi:10.1007/BF01524599.
- ↑ Patent US3860633A: 3,5-Dihalo-4-carobxyalkoxy phenols and esters thereof. Angemeldet am 24. Oktober 1972, veröffentlicht am 14. Januar 1975, Anmelder: Dow Chemical Co, Erfinder: Linneaus C. Dorman.
- ↑ E. Topp, L. Y. Xun, C. S. Orser: Biodegradation of the herbicide bromoxynil (3,5-dibromo-4-hydroxybenzonitrile) by purified pentachlorophenol hydroxylase and whole cells of Flavobacterium sp. strain ATCC 39723 is accompanied by cyanogenesis. In: Appl Environ Microbiol. 1992, 58(2), S. 502–506. PMC 195275 (freier Volltext)