Arachidonsäure
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
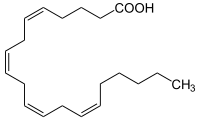
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Arachidonsäure | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C20H32O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose, klare Flüssigkeit[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 304,46 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||||||||
| Dichte |
0,922 g·cm−3[3] | |||||||||||||||||||||
| Schmelzpunkt |
−49,5 °C[2] | |||||||||||||||||||||
| Siedepunkt | ||||||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser,[3] gut löslich in unpolaren Lösungsmitteln (Benzol) | |||||||||||||||||||||
| Brechungsindex |
1,4824 (20 °C)[4] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Arachidonsäure ist eine vierfach ungesättigte Fettsäure in der Gruppe der Omega-6-Fettsäuren. Die Polyensäure zählt zu den Isolensäuren, da die vier cis-Doppelbindungen durch eine Methylengruppe (CH2) getrennt sind. Ihr Trivialname leitet sich von der vollständig gesättigten Arachinsäure ab, welche durch Hydrierung der Arachidonsäure entsteht.
Vorkommen und biologische Bedeutung
[Bearbeiten | Quelltext bearbeiten]Die Arachidonsäure kommt in Pflanzen nur in geringen Mengen vor. In Speiseölen kommt sie nicht oder nur in Spuren vor.[5]
Arachidonsäure wird in den meisten tierischen Organismen – Ausnahme sind z. B. Hauskatzen[6] – aus der essentiellen Omega-6-Fettsäure Linolsäure über die Zwischenstufen γ-Linolensäure (GLA) und Dihomo-γ-linolensäure (DGLA) synthetisiert oder über die Nahrung aufgenommen. Sie ist als Bestandteil von Lipiden wie etwa Phospholipiden in veresterter (physiologisch inaktiver) Form vor allem in den Zellmembranen lokalisiert. Sie kann durch das Enzym Phospholipase A2 (häufig aus 1,2-Diacylglycerinen, DAG) freigesetzt und dadurch biologisch aktiviert werden.
Cytosolische Arachidonsäure wird von Enzymen unterschiedlicher Gruppen metabolisiert, wobei Derivate entstehen, die als Signalmoleküle wirken. Obwohl deren Wirkung nicht einheitlich ist, gilt Arachidonsäure selbst als eher entzündungsfördernd. So inhibieren Cortisol und Vitamin E die Phospholipase und können so Entzündungsprozesse z. B. bei Gelenkerkrankungen wie der aktivierten Arthrose und weiterer Arthritis-Formen positiv beeinflussen. Eine möglichst geringe Aufnahme oder Synthese von Arachidonsäure scheint in den meisten Fällen gesundheitlich sehr wünschenswert zu sein. Bei entzündlichen Autoimmunerkrankungen (vor allem bei Multipler Sklerose (MS), aber auch bei Autoimmunthyreopathien und Rheuma) wird ebenfalls oft eine Diät empfohlen, die arm an Arachidonsäure ist. Gesicherte Nachweise für den Nutzen spezieller Diäten fehlen bislang.[7] Dieser Zusammenhang mag sich künftig auch in Bezug auf Colitis ulcerosa bestätigen. Einer Auswertung im Rahmen der EPIC-Studie nach trat Colitis ulcerosa gehäuft bei Personen auf, die eine höhere Einnahme von Linolsäure hatten, auch wenn aus den Studienergebnissen noch keine direkte Diätempfehlung folgt.
Die biologische Wirkung der Arachidonsäure-Derivate ist nicht auf Entzündungen beschränkt. Sie ist sehr umfangreich, teilweise auch gegensätzlich und wird daher bei den einzelnen Metaboliten abgehandelt.
So ist die Arachidonsäure für Säuglinge unabdingbar. Studien stützen keine Säuglingsnahrung ohne Arachidonsäure. Muttermilch enthält als beste Säuglingsnahrung weltweit mehr Arachidonsäure als beispielsweise die Omega-3 Fettsäure Docosahexaensäure (DHA). Ein hoher DHA-Anteil bei niedrigem Arachidon-Säuregehalt schadete Kindern langfristig bis zu 9 Jahren. Für nicht oder nicht vollgestillte Säuglinge gilt Nahrung nur als tauglich, die neben DHA mindestens ebenso viel Arachidonsäure enthält.[8]
Metabolisierung
[Bearbeiten | Quelltext bearbeiten]Arachidonsäure hat (vereinfacht) drei Wege weiterer Metabolisierung:
- Über die Cyclooxygenasen entstehen Prostaglandine,
- über die Lipoxygenasen entstehen Leukotriene und
- Cytochrom-P450 (CYPs) bewirken eine Epoxidation oder Hydroxylierung, wobei EETs bzw. Hydroxyeicosatetraensäuren (HETEs, bspw. 20-HETE) gebildet werden.
Über die Wege des Arachidonsäure-Metabolismus entstehen Metaboliten mit zum Teil gegensätzlichen Eigenschaften. So wirkt eine Verstärkung der Cyclooxygenase-2 fieberauslösend, eine Verstärkung epoxidierender CYPs jedoch auf verschiedenen Wegen direkt und indirekt fieberunterdrückend bzw. begrenzend. Acetylsalicylsäure und Ibuprofen hemmen nicht nur den Cyclooxygenaseweg, sondern induzieren auch den Epoxygenaseweg, dessen Stoffwechselprodukte wiederum die Cyclooxygenasen stärker hemmen als diese Medikamente.[9] Eine Metabolisierung durch CYPs bewirkt nicht immer eine Entzündungshemmung: Das von hydroxylierenden CYPs gebildete 20-HETE wirkt proinflammatorisch.[10]
Arachidonsäure in Lebensmitteln
[Bearbeiten | Quelltext bearbeiten]Arachidonsäurehaltige Glyceride finden sich in zahlreichen Lebensmitteln. Besonders hoch ist ihr Anteil in Schweineschmalz (1700 mg pro 100 g), Schweineleber (870 mg pro 100 g), Eigelb (297 mg pro 100 g), Thunfisch (280 mg pro 100 g) und Leberwurst (230 mg pro 100 g). Darüber hinaus kann es bei zuckerreicher Ernährung zu einer verstärkten hormonell gesteuerten Einschleusung in die Zellen kommen. Stark linolsäurehaltige Pflanzenöle und davon abgeleitete Produkte enthalten selbst kaum Arachidonsäure, tragen jedoch durch ihre Inhaltsstoffe zu deren Bildung bei. Da Omega-3- und Omega-6-Fettsäuren um die gleichen Enzyme konkurrieren, wird überdies die Biosynthese entzündungshemmender Stoffe aus Omega-3-Fettsäuren reduziert.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Arachidonsäure auf KEGG
- Tabelle mit dem Arachidonsäuregehalt(AA) verschiedener Lebensmittel
- Arachidonsäure
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu ARACHIDONIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 19. Januar 2022.
- ↑ a b c Eintrag zu Arachidonsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 20. Juni 2014.
- ↑ a b c Datenblatt Arachidonic acid bei Sigma-Aldrich, abgerufen am 14. Oktober 2023 (PDF).
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-228.
- ↑ 5,8,11,14-Eicosatetraenoic acid bei PlantFA Database, abgerufen am 27. Oktober 2017.
- ↑ Michael S. Hand (Hrsg.), Hans Joachim Oslage (Red.): Klinische Diätetik für Kleintiere. 4. Auflage, Band 1, Schlütersche 2004, ISBN 978-3-87706-893-9, S. 376.
- ↑ Stefan Schwarz u. a.: Unkonventionelle Therapien der multiplen Sklerose: Nutzen unklar. In: Deutsches Ärzteblatt Köln. 102.30, 2005, S. 1678 f.
- ↑ Should formula for infants provide arachidonic acid along with docosahexaenoic acid? A position paper of the European Academy of Pediatrics and the Child Health Foundation. American Journal of Clinical Nutrition; 26. Oktober 2019. doi:10.1093/ajcn/nqz252.
- ↑ W. Kozak et al.: Molecular mechanisms of fever and endogenous antipyresis. In: Ann. N Y Acad. Sci.917: 2000, S. 121–134, PMID 11268336.
- ↑ M. Laniado-Schwartzman et al.: 20-Hydroxyeicosatetraenoic acid stimulates nuclear factor-kappaB activation and the production of inflammatory cytokines in human endothelial cells. In: J. Pharmacol. Exp. Ther. 324(1): 2008, S. 103–110, PMID 17947496.