Allylgruppe

Allyl-Kation (Mitte) und Allyl-Radikal (unten). Der Allyl-Rest ist blau markiert.

Als Allylgruppe wird in der organischen Chemie ein ungesättigter Kohlenwasserstoffrest bezeichnet, der die Formel H2C=CH–CH2– hat, also eine 2-Propenyl-Gruppe darstellt. Es handelt sich dabei formal um eine Vinylgruppe H2C=CH–, an die eine Methylengruppe –CH2– angehängt ist. Allyl-Kationen und -Radikale sind mesomeriestabilisiert und deshalb deutlich stabiler als das entsprechende tert-Butyl-Kation bzw. -Radikal. Zum Beispiel hat Allylalkohol die Formel H2C=CH–CH2–OH.
Die Bezeichnung Allyl wurde 1844 von Theodor Wertheim geprägt und leitet sich ab von Allium, lateinisch für Knoblauch, in dem sich eine Reihe von Allylverbindungen wie z. B. Allicin finden.[1]
Eigenschaften und Verwendung
[Bearbeiten | Quelltext bearbeiten]Die Allylgruppe ist durch die leichte Abstrahierbarkeit eines der allylständigen, d. h. am sp3-hybridisierten, der Doppelbindung benachbarten Kohlenstoffatom gebundenen, Wasserstoffatome oder Protonen eine reaktionsfreudige funktionelle Gruppe in organischen Molekülen. Sind dort außerdem zwei unterschiedliche weitere Substituenten gebunden, so kann die aufgrund der 1,3-Allylspannung auftretende eindeutige Orientierung der Gruppen zueinander in der stereoselektiven Synthese ausgenutzt werden.
Allylverbindungen
[Bearbeiten | Quelltext bearbeiten]Es existieren zahlreiche natürliche und synthetische organische Verbindungen, die eine oder mehrere Allylgruppen enthalten. Technisch wichtige Allylverbindungen sind der Allylalkohol, das Allylchlorid sowie das Allylamin (mit Diallyl- und Triallylamin). Daneben existieren Allylverbindungen, die meist intermediär bei chemischen Reaktionen auftreten. Dazu zählen Allylkationen, -anionen sowie -radikale. Diese sind aufgrund der auftretenden Mesomerie sehr gut stabilisiert.
Allyl-Kation
[Bearbeiten | Quelltext bearbeiten]Das Allyl-Kation stellt eine positiv geladene Allylgruppe dar. Es lassen sich folgende zwei gleichwertige mesomere Grenzstrukturen (Resonanzformeln) formulieren:
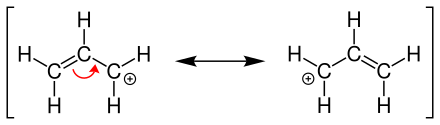
Die positive Ladung ist dabei über das gesamte Molekül verteilt, also delokalisiert.
Allyl-Anion
[Bearbeiten | Quelltext bearbeiten]Im Gegensatz zum Allylkation, stellt das Allyl-Anion eine negativ geladene Allylgruppe dar. Wiederum lassen sich hierbei zwei mesomere Grenzstrukturen zeichnen:

Das freie Elektronenpaar ist dabei nicht an den endständigen Kohlenstoffatomen lokalisiert, sondern mesomer über das gesamte Molekül delokalisiert.
Literatur
[Bearbeiten | Quelltext bearbeiten]- K. Peter C. Vollhardt, Neil E. Schore, Katrin-M. Roy: Organische Chemie. Hrsg.: Holger Butenschön. 5. Auflage. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2011, ISBN 978-3-527-32754-6.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu Allyl.... In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. April 2020.