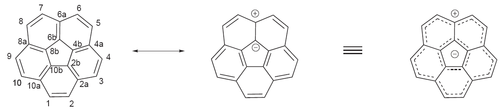
Corannulen
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Corannulen | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C20H10 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 250,30 g·mol−1 | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Corannulen, auch [5]-Circulen und Dibenzo[ghi,mno]fluoranthen genannt, ist der kleinste bekannte und erfolgreich synthetisierte Vertreter der [n]-Circulene. Es wurde erstmals 1966 von Barth und Lawton in einer bemerkenswerten, 16-stufigen Synthese mit klassischen Methoden hergestellt.[2]
Struktur
[Bearbeiten | Quelltext bearbeiten]Corannulen besteht aus fünf anellierten Benzolringen, die ein zentrales Fünfeck bilden, und kann somit als kleinstes Fragment von Fulleren (C60) betrachtet werden, welches noch dessen charakteristische Wölbung aufweist. Diese strukturelle Eigenschaft „zwingt“ das Molekül, einen bestmöglichen Kompromiss zwischen Delokalisation und Spannung einzugehen. Bevor die Struktur eindeutig durch Röntgenstrukturanalyse bestätigt wurde, war die Voraussage, ob es eine planare oder gewölbte Struktur aufweist, schwierig. Hanson und Nordmann zeigten, dass Corannulen eine gewölbte, schalenartige Struktur mit C5v-Symmetrie (siehe Punktgruppen) aufweist.[3]

Das Molekül zeigt eine schnelle Schaleninversion, dessen Energiebarriere an Corannulenderivaten mittels NMR-Experimenten (bei −64 °C) zu 42,7 kJ/mol (10,2 kcal/mol) gemessen wurde (ca. 200.000 Inversionen pro Sekunde). Die Standardbildungsenthalpie ΔHf0 beträgt 463,7 kJ/mol und wurde mittels Bombenkalorimetrie bestimmt.
Die Schalentiefe, die durch die Distanz zwischen den zwei Ebenen (die vom zentralen Fünfring und von den zehn Kohlenstoffatomen des Randes aufgespannt werden) definiert ist, beträgt 87 pm.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Eintrag zu Corannulene bei TCI Europe, abgerufen am 18. November 2024.
- ↑ W. E. Barth, R. G. Lawton: Dibenzo[ghi,mno]fluoranthene, in J. Am. Chem. Soc. 88. 1966, S. 380–381; doi:10.1021/ja00954a049.
- ↑ W. E. Barth, R. G. Lawton: The Synthesis of Corannulene, in: J. Am. Chem. Soc. 93. 1971, S. 1730–1745; doi:10.1021/ja00736a028.