Dinitrofluoranthene
Dinitrofluoranthene sind chemische Verbindungen aus der Gruppe der Fluoranthenderivate, die aus Fluoranthen und zwei Nitrogruppen bestehen. Durch die unterschiedliche Anordnung der Nitrogruppen sind theoretisch 25 verschiedene Isomere möglich.[1]
Vorkommen
[Bearbeiten | Quelltext bearbeiten]3,7- und 3,9-Dinitrofluoranthen wurden in geringen Mengen in Emissionen von Dieselmotoren, Kerosinheizungen und anderen Verbrennungsquellen nachgewiesen.[2]
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]3,7- und 3,9-Dinitrofluoranthen werden für Laborzwecke durch Nitrierung von Fluoranthen hergestellt.[2] Bei Renitrierung von 3-Nitrofluoranthen[S 1] in Gegenwart von rauchender Salpetersäure entsteht neben 3,7- und 3,9-Dinitrofluoranthen auch 3,4-Dinitrofluoranthen und 3,4,7-[S 2], 3,4,8-[S 3] oder 3,4,9-Trinitrofluoranthen.[3] Die Nitrierung von Fluoranthen mit NO2/N2O4 ergibt neben verschiedenen Mononitrofluoranthenen auch 1,2- und 1,3-Dinitrofluoranthen.[4][5] 1,2- und 2,3-DNF wiederum können durch Nitrierung von Fluoranthen mit N2O5 in CCl4 synthetisiert werden. 1,4-, 1,7-, 1,8-, 1,9-, 3,4-, 3,7-, 3,8-, 3,9- und 3,10-DNF können durch Nitrierung von 1-, 3-, 7- und 8-Nitrofluoranthen mit Salpetersäure synthetisiert, während die 1,5-, 2,4-, 2,5-, 2,7-, 2,8-, 2,9- und 2,10-DNF entweder durch Nitrierung von 1-[S 4], 2-[S 5], 3-, 7-[S 6] und 8-Nitrofluoranthen[S 7] mit N2O5 in CCl4 oder durch Nitrierung von 2-Nitrofluoranthen mit Salpetersäure erhalten werden können.[1]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]| wichtige Dinitrofluoranthene[6] | weitere Dinitrofluoranthene | ||||
| Name | 3,4-Dinitrofluoranthen | 3,7-Dinitrofluoranthen | 3,8-Dinitrofluoranthen | 3,9-Dinitrofluoranthen | 3,10-Dinitrofluoranthen |
| Strukturformel | 
|

|

|

|

|
| CAS-Nummer | 55691-69-5 | 105735-71-5 | 105735-74-8 | 22506-53-2 | 105735-69-1 |
| PubChem | 41534 | 60018 | 184574 | 31186 | 184570 |
| Wikidata | Q83077674 | Q27155875 | Q82879365 | Q27155876 | Q82879361 |
| Summenformel | C16H8N2O4 | ||||
| Molare Masse | 292,25 g·mol−1 | ||||
| Aggregatzustand | fest | ||||
| Kurzbeschreibung | gelbe Nadeln | gelb-orange Kristalle | |||
| Schmelzpunkt | 203–204 °C | 275–276 °C | |||
| Dichte | ? | ||||
| Löslichkeit | ? | ||||
| GHS- Kennzeichnung |
| ||||
| H- und P-Sätze | siehe oben | ||||
| siehe oben | |||||
| weitere Dinitrofluoranthene | |||||||
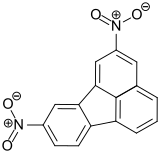
| Name | 2,3-Dinitrofluoranthen | 2,4-Dinitrofluoranthen | 2,5-Dinitrofluoranthen | 2,7-Dinitrofluoranthen | 2,8-Dinitrofluoranthen | 2,9-Dinitrofluoranthen | 2,10-Dinitrofluoranthen |
| Strukturformel | 
|

|

|

|

|
|

|
| CAS-Nummer | 105735-66-8 | 102493-19-6 | 102493-21-0 | 105735-70-4 | 105735-75-9 | 105735-77-1 | 105735-73-7 |
| PubChem | 149706 | 149088 | 149119 | 184571 | 184575 | 184577 | 184573 |
| Wikidata | Q83012572 | Q83009606 | Q83009609 | Q82879362 | Q82879367 | Q82879368 | Q83012574 |
| Summenformel | C16H8N2O4 | ||||||
| Molare Masse | 292,25 g·mol−1 | ||||||
| weitere Dinitrofluoranthene | |||||||
| Name | 1,2-Dinitrofluoranthen | 1,3-Dinitrofluoranthen | 1,4-Dinitrofluoranthen | 1,5-Dinitrofluoranthen | 1,7-Dinitrofluoranthen | 1,8-Dinitrofluoranthen | 1,9-Dinitrofluoranthen |
| Strukturformel | 
|

|

|

|

|

|

|
| CAS-Nummer | 25896-23-5 | 110419-21-1 | 105735-67-9 | 105735-68-0 | 105735-65-7 | 105735-72-6 | 105735-76-0 |
| PubChem | 119264 | 135718 | 184568 | 184569 | 184567 | 184572 | 184576 |
| Wikidata | Q82926630 | Q27288374 | Q83012573 | Q82879360 | Q83012571 | Q82879363 | Q83012575 |
| Summenformel | C16H8N2O4 | ||||||
| Molare Masse | 292,25 g·mol−1 | ||||||
| Dinitrofluoranthene ohne weitere Informationen | |||||||
| Name | 1,6-Dinitrofluoranthen | 1,10-Dinitrofluoranthen | 7,8-Dinitrofluoranthen | 7,9-Dinitrofluoranthen | 7,10-Dinitrofluoranthen | 8,9-Dinitrofluoranthen | |
| Strukturformel | 
|

|

|

|

|

| |
| Summenformel | C16H8N2O4 | ||||||
| Molare Masse | 292,25 g·mol−1 | ||||||
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Die subkutane Injektion von 3,7- und 3,9-Dinitrofluoranthenen bei Ratten führte zu einer hohen Inzidenz von subkutanen Tumoren an der Injektionsstelle, bei denen es sich zumeist um bösartige fibröse Histiozytome handelte. Das Einatmen von 3,7- und 3,9-Dinitrofluoranthenen führte zu einer hohen Inzidenz von Lungentumoren, bei denen es sich zumeist um Plattenepithelkarzinome handelte. Die Verbindungen sind für Bakterien hochgradig mutagen, insbesondere wenn kein exogenes Stoffwechselsystem vorhanden ist. In Säugetierzellen induzierten diese Verbindungen in vitro Chromosomenaberrationen, aber keine Genmutationen.[2][7] Auch von anderen Dinitrofluoranthenen sind ähnliche Wirkungen bekannt.[7]
Anmerkungen
[Bearbeiten | Quelltext bearbeiten]- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 3-Nitrofluoranthen: CAS-Nr.: 892-21-7, EG-Nr.: 681-940-4, ECHA-InfoCard: 100.207.060, PubChem: 13462, ChemSpider: 12885, Wikidata: Q27116002.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 3,4,7-Trinitrofluoranthen: CAS-Nr.: 109791-11-9, Wikidata: Q124209746.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 3,4,8-Trinitrofluoranthen: CAS-Nr.: 55691-68-4, PubChem: 180525, Wikidata: Q83077673.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 1-Nitrofluoranthen: CAS-Nr.: 13177-28-1, PubChem: 25759, Wikidata: Q83025356.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 2-Nitrofluoranthen: CAS-Nr.: 13177-29-2, PubChem: 25760, ChemSpider: 24000, Wikidata: Q27893894.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 8-Nitrofluoranthen: CAS-Nr.: 13177-32-7, PubChem: 25762, Wikidata: Q83025358.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 7-Nitrofluoranthen: CAS-Nr.: 13177-31-6, PubChem: 25761, Wikidata: Q83025357.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Th. Ramdahl, J. Arey, B. Zielinska, R. Atkinson, A. M. Winer: Analysis of dinitrofluoranthenes by high resolution capillary gas chromatography/mass spectrometry. In: Journal of High Resolution Chromatography. Band 9, Nr. 9, 1986, S. 515–517, doi:10.1002/jhrc.1240090905.
- ↑ a b c IARC: 3,7-Dinitrofluoranthene and 3,9-Dinitrofluoranthene (IARC Summary & Evaluation, Volume 65, 1996), abgerufen am 6. Januar 2024.
- ↑ Reiko Nakagawa, Kazumi Horikawa, Nobuyuki Sera, Yasushi Kodera, Hiroshi Tokiwa: Dinitrofluoranthene: induction, identification and gene mutation. In: Mutation Research Letters. Band 191, Nr. 2, 1987, S. 85–91, doi:10.1016/0165-7992(87)90134-5.
- ↑ Giuseppe L. Squadrito, Frank R. Fronczek, Daniel F. Church, William A. Pryor: A dichotomy in the nitration of fluoranthene with nitrogen dioxide/dinitrogen tetroxide: mechanistic and toxicological implications. In: The Journal of Organic Chemistry. Band 55, Nr. 9, 1990, S. 2616–2621, doi:10.1021/jo00296a015.
- ↑ Giuseppe L. Squadrito, Daniel F. Church, William A. Pryor: Anomalous nitration of fluoranthene with nitrogen dioxide in carbon tetrachloride. In: Journal of the American Chemical Society. Band 109, Nr. 21, 1987, S. 6535–6537, doi:10.1021/ja00255a062.
- ↑ Patty's Toxicology, 6 Volume Set. Wiley, ISBN 0-470-41081-7, S. 763 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Hiroshi Tokiwa, Kazumi Horikawa, Yoshinari Ohnishi: Genetic toxicology and carcinogenicity of mono- and dinitrofluoranthenes. In: Mutation Research/Reviews in Genetic Toxicology. Band 297, Nr. 2, 1993, S. 181–195, doi:10.1016/0165-1110(93)90002-5.