Diskussion:Glycerin
Physikalische Eigenschaften
[Quelltext bearbeiten]Ist ja schön, die Formel für die Viskosität zu sehen! Aber leider sagt mir das gar nix! Ist Glycerin so dickflüssig wie Ketchup (der gr. Name "süßes Wachs" ließe das Vermuten) oder eher wie Tomatensaft? Wer weiß es? Könnte man ja ergänzen! (nicht signierter Beitrag von Schlaukeks (Diskussion | Beiträge) )
- Nun, im Artikel steht Glycerin hat eine Viskosität von 1760 mPa·s. Unter typische Vergleichswerte kannst Du im Artikel Viskosität nachlesen wie sich das vergleicht: Olivenöl hat z.B. 100, Honig 10.000. In der englischen Wikipedia kann man nachlesen, dass die Viskosität mit der von Rhizinusöl vergleichbar ist. -- Ukko 22:05, 4. Jun. 2008 (CEST)
Der hier angegebene Wert für die Viskosität stimmt nicht mit dem Wert aus der Tabelle im Artikel Viskosität üerein. Welcher Wert ist richtig? -- 93.129.177.56 09:42, 11. Mär. 2010 (CET)
Bezeichnung
[Quelltext bearbeiten]Hier steht, dass Glycerin auch als Propan-1,2,3-triol bezeichnet wird. Beim Propylenglykol wird dagegen die Bezeichnung 1,2-Propandiol verwendet. Frage:
Wäre hier also auch 1,2,3-Propantriol richtig?
- beides ist AFAIK nach der iupac-nomenklatur richtig..es gibt auch noch Propantriol-(1,2,3) (oder so ähnlich) --217.95.247.70 21:24, 23. Apr. 2007 (CEST)
Der Name leitet sich von griech. '"glykeros" ab (heißt ebenfalls "süß"; siehe z. B. http://www.brockhaus.de/wissen/glycerin. --FK1954 08:56, 6. Jan. 2009 (CET)
Kann man auch Tri-Hydroxy-Propan sagen? --Lehnni 11:29, 19. Jun. 2009 (CEST)
- Kann man... Nochmal zu glykys/glykeros: beides heißt "süß", aber die bessere Übereinstimmung zwischen "glykeros" und "Glycerin" ist doch wohl erkennbar... Hiernach http://www.wissen.de/wde/deutsches_woerterbuch/Glycerin ist "glykeros" die poetische Form von "glykys". Gruß, --FK1954 09:25, 27. Jul. 2009 (CEST)
Besser wäre dann 1,2,3-Trihydroxypropan.--78.54.123.78 23:45, 16. Feb. 2010 (CET)
"Glycerin wird in Shisha-Tabak verwendet, um ihn feucht zu halten. Dies ist als sehr kritisch zu betrachten, da beim Verbrennen von Glycerin Acrolein und Acrylamid entstehen."
Der Shishatabak wird nicht verbrannt sondern durch die warme Kohle "gedünstet" --Inferno 15:06, 18. Okt. 2006 (CEST)
- Ach, und deshalb entsteht kein Acrolein, oder wie soll ich das jetzt verstehen? ;-) Anmerkung: Acrolein entsteht schon bei um die 200 °C, und die Temperatur wird locker erreicht. Also hier nicht versuchen, alles zu verharmlosen... 80.136.244.73 01:01, 6. Mär. 2007 (CET)
Im Tabakkopf selbst wird aber nur eine Temperatur von ~80 Grad erreicht! Dass die Kohle über 200 °C hat ist keine Frage, aber im Kopf selbst wird diese Temperatur nicht überall, bzw nur selten erreicht... Dass das ganze nicht verharmlost werden sollte ist klar, aber abheben sollte man auch nicht...Boaschti 22:07, 27. Mär. 2008 (CET)
Um Glycerin (oder Tabak) in Rauch zu verwandeln, reichen 80 °C bei Weitem nicht aus... --FK1954 08:56, 6. Jan. 2009 (CET)
- Im Text steht, dass zumindestenss Acrolein nur bei Sauerstoffmangel entsteht. Das ist bei der Wasserpfeife aber eher nicht zu erwarten. da ja stehts Luft am Tabak vorbeigezogen werden muss. (nicht signierter Beitrag von 88.77.241.173 (Diskussion | Beiträge) 00:10, 21. Dez. 2009 (CET))
In der Einleitung ist von dem Isomer Propan-1,1,2-triol die Rede. Das ist aber nach der Erlenmeyer-Regel verboten und somit garnicht existent, oder etwa nicht?(Der vorstehende, nicht signierte Beitrag stammt von DerHannes1983 (Diskussion • Beiträge) 12:03, 8. Dez 2007) --NEUROtiker 12:13, 8. Dez. 2007 (CET)
- Ist es, ich habe die Einleitung entsprechend umformuliert. Gruß, --NEUROtiker 12:13, 8. Dez. 2007 (CET) P.S.: Bitte signieren
Ist der Schmelzpunkt nicht -18°C ?
Der Vollständigkeitshalber könnte man noch erwähnen, dass es auch als "Kunstträne" verwendet wird, d.h. in manchen Filmen(vieleicht ja auch vielen Filmen kA) wird es für "Heulszenen" verwendet.
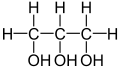
Die Strukturformel ist falsch. Es fehlen die C-Atome.
Wäre es nicht sinnvoller es unter dem UPAC Namen einzuordnen und vom Trivialnamen Glycerin aus den Verweis anzulegen?? Lars73 15:34, 5. Apr 2005 (CEST)
- Bei organischen Verbindungen die ganzen Cs (und einzelnen Hs) wegzulassen, ist eine standardisierte vereinfachte Darstellung. Es ist ja ohne weiteres aus der Strukturformel zu erkennen, wo sie sitzen.
immer an den ecken der Verbindungen der anderen Atome
Steht in jedem Chemiebuch
Achtung Widerspruch
[Quelltext bearbeiten]In bezug auf die Löslichkeit von Acrylaldehyd besteht ein Widerspruch!
Acrolein (Beachte "Weitere Eigenschaften")
Glycerin (Beachte "In Wasserpfeifentabak wird..." >> letzter Absatz)
Einmal wird ausgesagt es wäre schwer löslich (Stichwort:Glycerin) das andere mal leicht löslich (Stichwort:Acrylaldehyd). Was stimmt nun?
BloodReaver 13:01, 14. Apr 2005 (CEST)
Glycerin als solches ist schwer löslich aber die abfallproduckte der Reaktion beim Verbrennen sind dagegen leicht löslich!
Kannst auch bei Holz sehen ! versuch mal holz in wasser zulösen und dannach sein abfallproduckt nach der verbrennung! asche !!!!
VORSICHT! Asche ist kein Holz, sondern Mineralien welche im ursprünglichen Holz eingeschlossen waren. Die chemische Zusammensetzung ist komplett unterschiedlich! Das Selbe gilt in gewisser Weise für Glycerin. (nicht signierter Beitrag von 79.254.85.155 (Diskussion) 15:38, 10. Jan. 2014 (CET))
Strukturformel
[Quelltext bearbeiten]Zur Strukturformel: die mittlere OH-Gruppe sollte in die andere Richtung zeigen. Etwa so:
HO H OH | | | H-C-C-C-H | | | H OHH
(natürlich mit Abstand zwischen dem unteren OH und H)
Gruß, Chris, 16.04.2005
Da keine Doppelbindung besteht ist das Molekül frei drehbar und die Stellung der OH-Gruppe ist somit egal --Kaiser Bob 14:55, 16. Mai 2005 (CEST)
Ganz so einfach ist es nicht, bei Sacchariden sind auch keine Doppelbindungen zwischen den Kohlenstoffen, trotzem besitzen sie ein chirales Zentrum aufgrund ihrer Konfiguration und damit optische Aktivität... Chemisch korrekt in Fischer-Projektion würde das Glycerin so aussehen:
|
-C-OH
|
OH-C-
|
-C-OH
|
Wobei die Fischer-Projektion nur ein Modell darstellt, welches die R- und S-Stellungen der OH-Gruppen aufzeigt.
P.S.: Ich finde dass der Anhang mit der Diskussion der Entstehung von Acrolein beim Shisha-Rauchen nicht unbedingt in den Artikel gehört, da meiner Meinung nach zu Subjektiv ist. Beim Rauchen entsteht definitiv Acrolein, da ein Sauerstoffmangel herrschen muss, ansonsten würde es nicht Rauchen sondern lediglich H2O und CO2 entstehen. Zweitens ist die Temperatur der Kohle ausreichend, um aus Glycerin Acrolein zu Bilden (sofern es gute Kohlen sind) und drittens ist nicht geklärt, wieviel Acrolein durch das Wasser in der Shisha absorbiert wird und somit beim Raucher ankommt. Ich schätze dass der hauptsächliche Anteil des Acroleins durch den Nebenstromrauch beim Raucher ankommt, also das, was nicht durch den Schlauch gelangt, sondern einfach oben abraucht.
Gruß, Flo(rian) 20:06, 29. November 2005 (CEST)
Da am C2 zwei gleiche Substituenten (Hydroxymethylgruppen, selber achiral) sitzen, liegt kein Chiralitätszentrum vor, und damit ist die Stellung der mittleren OH-Gruppe egal. Was die Wasserlöslichkeit von Acrolein angeht, so ist sie deutlich geringer als die von Glycerol, und damit dürfte ein nicht unbeträchtlicher Teil in den Hauptstromrauch geraten, wenngleich auch weniger als bei ungefiltertem Rauch. 131.220.136.195 13:53, 6. Mär. 2007 (CET)
- Nachtrag: Propylenglykol hingegen wäre chiral. 131.220.136.195 12:20, 8. Mär. 2007 (CET)
was passiert wenn ich frostschutzmittel mit konz. Schwefelsaüre+konz Salpetersäure! Sylvester
- Dein Satz kein Verb. --193.100.62.29 10:23, 4. Jan. 2011 (CET)
Frage an die Fachleute
[Quelltext bearbeiten]Wäre es nicht sinnvoll einen Hinweis auf die (industrielle) Gewinnung von Glycerin einzufügen? Wer kann das machen? --vocat 20:11, 31. Jan 2006 (CET)
Unter http://www.innovations-report.de/html/berichte/verfahrenstechnologie/bericht-60490.html finden sich Hinweise auf die Gewinnung von Glycerin als Abfallprodukt der Biodieselherstellung, dies ist aber mit Sicherheit nicht die Einzige "Glycerinquelle". Unter http://www.chemistryworld.de/cheminfo/glycerol.html wird die Gewinnung aus Propylengas beschrieben.
Glycerin als Rauschmittel?
[Quelltext bearbeiten]Da Glycerin ein Alkohol ist, also ein dreiwertiges Alkohol, kann man daraus den Entschluss ziehen dass es einem wie bei einem Alkoholgenuß z.B. Bier, die Sinne raubt? (Vorstehender nicht signierter Beitrag stammt von 88.65.217.81 (Diskussion • Beiträge) 17:41, 6. Dez 2006 (CEST))
- Nein. Für die berauschende Wirkung beim Ethanol ist nicht direkt die Hydroxylgruppe verantwortlich, sondern, soweit ich weiß der Dipolcharakter, der ihn auch die guten Eigenschaften als Lösungsmittel ausmacht. Viele der zahlreichen Alkohole wirken nicht berauschend, beispielsweise die Zuckeralkohole, die sechs OH-Gruppen und mehr tragen und beispielsweise als Süßungsmittel eingesetzt werden. --NEUROtiker 18:41, 6. Dez. 2006 (CET)
- Eigentlich ist es das enzymatische Abbauprodukt des Ethanols, das uns "besoffen" werden lässt. Das meine ich zumindest irgendwann einmal gehört zu haben. Glycerin selber ist verdammt süss. Kannst es ja mal als süsser in den Kaffee tun. Schmeckt in dann etwa so wie Sorbit oder andere künstliche "Süssstoffe". (Vorstehender nicht signierter Beitrag stammt von 193.103.148.68 (Diskussion • Beiträge) 8:06, 7. Dez 2006 (CEST))
- Für den Rausch ist schon der Alkohol selbst verantwortlich. Das Abbauzwischenprodukt Acetaldehyd ist verantwortlich für den Kater. Glycerin kann, wie Sorbit auch, als Zuckeralkohol – in diesem Fall der Triosen – aufgefasst werden.--NEUROtiker 11:32, 7. Dez. 2006 (CET
Danke für diese Erkenntnis, da ich islamischen Glaubens bin und bemerkt habe, dass in sehr vielen Produkten Glycerin enthalten ist und ich deshalb diese Befürchtung (Glycerin=Rauschmittel) gehabt habe. Vielen Dank.! By Serkan aus Coburg.
Herstellung von Datteln?
[Quelltext bearbeiten]Im Text wird die Herstelung von Datteln erwähnt. Datteln wachsen auf Palmen. Was ist damit gemeint? Trocknen? Haltbarmachen? --Poc 23:00, 26. Dez. 2006 (CET)
Shishatabak---
Hab Mit Interesse die Berichte über Shisha-Tabak u. Glycerin gelesen. Was kann man davon halten, wenn der Tabak selber hergestellt wird. Z.B. Zitronen mit Glycerin gemischt werden. Vielleicht hat jemand eine Antwort für mich.
- Das Glycerin muss in die Blattzellen, sonst verdampft es einfach nur. Draufgießen ist sinnlos. Ausführlicher Artikel dazu hier.
Schmelzpunkt?
[Quelltext bearbeiten]Es ist von einem Schmelzpunkt bei 18,2 °C die Rede. Doch in meinem Versuch geht Glycerin nichteinmal bei - 10 °C in den festen Aggregatzustand über. Entweder es geschieht bei - 18 °C oder es Glycerin ändert seinen Aggregatzustand nicht. Mein Glycerin stammt aus der Apotheke. Fachliteratur gibt den Schmelzpunkt auch mit 18 °C an. Warum wird meins nicht fest?- Metoc ☺ 22:36, 27. Feb. 2007 (CET)
- Schon mal was von Schmelzpunkterniedrigung gehört? Handelsübliches Glycerol hat einen Gehalt von 85 % und einen entsprechend niedrigeren Schmelzpunkt. Kannst ja mal ausrechnen. 80.136.244.73 01:08, 6. Mär. 2007 (CET)
- Glycerin aus der Apotheke wird im Tiefkühlfach Gummi, das Zeug ist einfach zu hydrophil. -- Lumi 23:18, 23. Apr. 2007 (CEST)
- Aus aktuellem Anlass, habe neulich Praktikumsversuch mit Glycerin/Glycerol gemacht: Das Zeug hat keinen festen Schmelzpunkt/Gefrierpunkt. Es findet auch bei langsamem Abkühlen ein Glasübergang statt. Also kein schlagartiges Erstarren, sondern Viskositätserhöhung über viele Größenordnungen. In so einem Fall gibt man stattdessen die Glastemperatur an, die (willkürlich) als die Temperatur definiert ist, bei der ein Stoff die Viskosität 10^12 Pas erreicht. Im Fall von Glycerin ist das 185K (laut P. Lunkenheimer et al., Physikalische Blätter 6/2000, S. 37). (Offtopic: Wollte das auf die Hauptseite von Glycerin reinschreiben, war unfähig dazu? Der Edit hat jedenfalls nicht geklappt...) -- by pixelbrei, noch nicht registriert, edit-neuling sozusagen
- Der Schmelzpunkt liegt tatsächlich bei ca. +18 °C. Allerdings gehört Glycerin zu den Stoffen, die nur ungern kristallisieren, zumal in Gegenwart von ein wenig Wasser. --FK1954 17:29, 30. Jan. 2009 (CET)
- Habe jetzt mal Informationen zum Glasübergang von Glycerin ergänzt (bei "Physikalische Eigenschaften"), mitsamt dem von pixelbrei vorgeschlagenen Zitat. In der Physik ist es wohl das meistuntersuchte glasbildende System, da es praktisch nie kristallisiert. --Doctorludens (Diskussion) 18:29, 22. Jan. 2023 (CET)
Name
[Quelltext bearbeiten]- Glycerol ist, im Gegensatz zu Benzol oder Toluol, die einzig richtige Bezeichnung, weil die alkoholische Hydroxylfunktion die höchste Priorität besitzt. Glycerin ist sogar falsch, weil hier kein Alkaloid vorliegt, das die Endung -in rechtfertigen würde. Also: Nach Glycerol verschieben! Und wo man gerade dabei ist, dasselbe bei Cholesterol aus denselben Gründen auch gleich. Danke! 80.136.244.73 01:01, 6. Mär. 2007 (CET)
Ist Glycerin nicht auch ein wesentlicher Bestandteil der meisten wasserlöslichen Produkte? --Nemissimo 酒?!? 12:37, 11. Apr. 2007 (CEST)
Tabak
[Quelltext bearbeiten]Stimmt es, das es seit ca. 3 Jahren verboten ist, losen Tabak mit mehr als 5 % Glycerinanteil aus nicht-europäischen Ländern, nach Deutschland zu importieren, bzw. ihn zu verkaufen? --Nemissimo 酒?!? 12:43, 11. Apr. 2007 (CEST)
- Es ist seit fast 30 Jahren verboten, nur hat es keiner bemerkt. Mit dem Import von Shisha-Tabak mit mehr als 30% Glycerinanteil hat sich das Anfang 2004 geändert, inzwischen gibt es regelrechte Razzias vor allem in Shishaläden und -lokalen. Quelle: Tabakverordnung ("Verordnung über Tabakerzeugnisse") vom 20.12.1977, Anlage 1 "Zugelassene Stoffe", Punkt 2 "Feuchthaltemittel", a): "für Rauchtabak, Zigarren, Zigaretten, Tabakfolie und Kunstumblatt Glycerin (E 422) ... bis zu einer Höchstmenge von insgesamt 5 vom Hundert der Trockenmasse des Erzeugnisses". Summiert allerdings mit Propylenglykol und anderen üblichen Zusatzstoffen zur Feuchthaltung von Tabakprodukten, die Liste umfasst 2 Seiten. Die Tabaktrockenmasse macht bei Shishatabak allerdings wegen des hohen Melasseanteils nur etwa ein Drittel des Gesamtgewichts aus, so dass in diesem Fall de facto ein Drittel von 5% am Gesamtgewicht zulässig sind. -- Lumi 22:26, 23. Apr. 2007 (CEST)
In diesem Zusammenhang wäre es interessant ob es Studien gibt wie sich der Glycerol-Zusatz im Shisha-Tabak auswirkt. Wie im Artikel beschrieben kann sich aus Glycerol in der Hitze das toxische Propenal (Acrolein) bilden.141.52.232.84 13:27, 12. Dez. 2007 (CET)
Eine aktuelle Untersuchung des Bundesinstitut für Risikobewertung (BfR) deutet in eine andere Richtung: Im Rauch von feuchtem Wasserpfeifentabak wurden erhebliche Mengen der Feuchthaltemittel Glycerin und Propylenglykol nachgeweisen, die Konzentrationen lagen so hoch, dass Gesundheitsgefahren drohen, siehe BfR-Pressemitteilung vom 03. August 2011. (nicht signierter Beitrag von Shisha-Tom (Diskussion | Beiträge) 20:53, 14. Nov. 2011 (CET))
Verwendung als Panschmittel
[Quelltext bearbeiten]Ich habe den tippfehlerbehafteten Satz "2005 erregte ein Fall Aufmerksamkeit, in dem Glycerin dem Wein der Supermarktkette Penny zugestzt wurde" unter dem Punkt "Verwendung" rausgenommen: Das halte ich so formuliert sachlich für nicht richtig, weil es den Glycerinzusatz durch Mitarbeiter der Rewe suggeriert, wovon die Staatsanwaltschaft damals (2005) nicht ausgegangen ist. Das Thema passt besser zu Panschen und sollte dann auch weiter ausgeführt werden, Beispiele gibt es genug. -- Lumi 18:41, 6. Mai 2007 (CEST)
Toxizität / Sicherheitshinweise?
[Quelltext bearbeiten]Lt. MSDS gibt es folgende Angaben zur Toxizität von Glycerol:
- IPR-RAT LD50 8700 mg kg-1
- ORL-RAT LD50 12600 mg kg-1
- SCU-RAT LD50 100 mg kg-1
- ORL-MUS LD50 8700 mg kg-1
Glycerol ist auch auf www.gifte.de verzeichnet. Im Wikipedia-Artikel sind jedoch bisher keinerlei Sicherheitshinweise vermerkt. Eventuell könnte jemand die Angaben überarbeiten. 217.94.203.244 00:45, 14. Aug. 2007 (CEST)
- Ich hab die ORL-RAT mal hochgerechnet: für den Durchschnittsmenschen mit 75 kg wären das fast ein Kilo! Da kann man sich den Hinweis auf die Giftigkeit schenken, da sollte man eher darauf achten, dass man nicht in einer Glycerinpfütze ausrutscht, nachdem man das zeug getrunken hat! --128.246.48.130 13:28, 11. Jun. 2008 (CEST)
Ich weiß - die Dosis macht das Gift. Aber irgendwie dünkt es mich komisch, wenn Glycerol als Futtermittel für Kühe und Schweine genannt wird und gleichzeitig eine LD50 von ca. 4g /kg Körpergewicht für Mäuse angegeben wird. So ein 250 kg Schwein würde dann im statistischen Mittel - so der Maus vergleichbar - nach 1 kg Glycerol tot umkippen. D.h. ein Teil der Population (des Stalles) würde schon nach viel weniger und ganz ohne Metzger in die ewigen Jagdgründe übertreten. Um Kalorienrelevanz zu bekommen, müßten die verzehrten Mengen doch sicher im Bereich einiger hundert Gramm liegen? Auch nach obiger ORL-RAT Rechnung müßte man unter Beachtung der Statistik davon ausgehen, daß beim Menschen bereits nach Mengen im Bereich von unter 100g einzelne Todesfälle zu beklagen wären - also weniger als ein 0,2 l Glas. Siehe http://de.wikipedia.org/wiki/Letale_Dosis: "Ein tödlicher Effekt kann also auch erst bei wesentlich höheren oder schon bei niedrigeren Dosen/Konzentrationen auftreten, zum Beispiel bei einer Schwächung durch Krankheit.". Also was jetzt? Nahrungsmittel oder doch Gift?
Es KANN bei geringerer Dosierung schon zu Todesfällen kommen, MUSS aber nicht, da macht der LD50 keine Aussage. Außerdem kann man LD-Ratte nicht ohne Weiteres auf Schweine oder Menschen übertragen. Jedes Fett wird im Körper zu Fettsäuren und Glycerin zerlegt. Auch Wasser oder Kochsalz zeigen in sehr hohen Dosen toxische Effekte, aber das ist bei weitem kein Grund, auf ihre Giftigkeit hinzuweisen. Glycerin ist definitiv kein Gift. Naclador 14:21, 23. Mär. 2011 (CET)
Kosmetik
[Quelltext bearbeiten]Habe vor Jahren gehört, dass Glycerin in Feuchtigkeitscremes tatsächlich das Gegenteil bewirke: Es entzieht der Haut Feuchtigkeit, macht sie damit kurzzeitig geschmeidiger und führt damit zu einer Art Abhängigkeit bei längerem Gebrauch? Kann das jemand bestätigen oder ist das in den Bereich Verschwörungstheorie einzuordnen? Wie wirkt Glycerin als Feuchtigkeitsspender in der Kosmetik? Wird (ausschließlich) der Umgebungsluft Wasser entzogen und der Haut zugefügt oder auch etwa tieferen Hautschichten? --Wurfholz 22:52, 11. Nov. 2007 (CET)
Glycerin Bestandteil von allen Fetten?
[Quelltext bearbeiten]Ist Glycerin wirklich Betstandteil von allen Fetten? Ich dachte nur von den Triglyceriden, aber das sind doch nicht alle Fette, oder? 87.160.120.37 22:19, 29. Mai 2008 (CEST)Racer1
- Speisefette sind immer Triglyceride. --128.246.48.130 13:30, 11. Jun. 2008 (CEST)
Fette sind chemisch so definiert, dass es Triglyceride sind. Es gibt natürlich noch andere fettähnliche Stoffe, die dann eher Wachse etc oder anderes sind. Cholo Aleman 22:13, 2. Okt. 2008 (CEST)
"Energieerzeugung"
[Quelltext bearbeiten]Wer von "Energieerzeugung" spricht, tut damit kund, dass er von der Sache entweder nichts versteht oder sich an Ahnungslose wenden will. Weil in dem Beitrag die Rede von "Energieerzeugung" ist, habe ich den Begriff durch "Stromerzeugung" ausgetauscht. Wir kleine Menschlein sind nur in der Lage, Energie umzuwandeln. Um Energie zu produzieren, müssten wir allmächtige Götter sein. (nicht signierter Beitrag von Christoph Müller (Diskussion | Beiträge) 13:28, 13. Jun. 2009 (CEST))
Falsche Strukturformel
[Quelltext bearbeiten]Die derzeit gezeigte Strukturformel ist offenkundig falsch. Als Nicht-Chemiker kann ich's nicht selbst ändern. Wer übernimmt es? -- w-alter ∇ 18:15, 12. Jan. 2011 (CET) (CET)
- Nein, die Strukturformel ist richtig. Kohlenstoff- und direkt daran hängende Wasserstoffatome werden üblicherweise nicht explizit gezeichnet. Viele Grüße --Orci Disk 18:16, 12. Jan. 2011 (CET)
Molmasse
[Quelltext bearbeiten]Mit den Atommassen aus der deutschen Wikipedia (Kohlenstoff, Sauerstoff, Wasserstoff) bekomme ich eine Molmasse von 92.094 g/mol heraus, was zu 92.09 g/mol abgerundet und nicht auf 92.10 g/mol aufgerundet werden müsste. Naclador 14:53, 23. Mär. 2011 (CET)
- 92,094 g/mol ist korrekt, hast Du ja schon geändert. Gruß --Cvf-psDisk+/− 19:21, 10. Okt. 2012 (CEST)
Brille / optik
[Quelltext bearbeiten]Macht Glycerin beim Putzen die Brillengläser kaputt (matter -> Durchsichtprobleme), wenn es im Spülmittel drin ist? In meinem Spülmittel ist laut dem was drauf steht drin: anionische Tenside, nicht anionische Tenside, amphotene Tenside, Lactia Acid, Zitronenöl. Ist dann da Glycerin drin? Gehört das da irgendwo dazu? Und wenn ja, schadet das den Brillengläsern tatsächlich? Danke für Antworten! (nicht signierter Beitrag von 46.5.101.177 (Diskussion) 00:24, 12. Nov. 2011 (CET))
- andererseits , wie ist die verträglichkeit mit mikroskopobjektiven (immersionsflüssigkeit), bzw der fassung der linsen , die ja von alkohol angegriffen werden können . außerdem gibt es keinen hinweis zum säure-base-verhalten (pks-wert) und chemisches verhalten . glycerin hat den brechungsindex nahe dem von glas , jedoch kunstoffgläser haben einen weit höheren . mit glycerin könnte man vielleicht kratzer optisch ausgleichen , ähnlich dem kanada-balsam , aber es ist wohl nicht sehr haltbar, vielleicht ist das der klarspül-hochglanz-effekt ? . bei glas im geschirrspüler gibt es ja das herauslösen von mineralien aus dem glas , was zur blindung führt . kein bleikristall in die spülmaschine . und dann gibt es noch die antireflexbeschichtung die chemisch nicht die härteste ist . aber ich glaube spüli ist nicht schlimm . --Konfressor (Diskussion) 08:17, 11. Dez. 2015 (CET)
Doping
[Quelltext bearbeiten]Auf der Internetwebseite der Zeitung "Fit for Fun" wird Glycerin als Dopingmittel empfohlen. Findet es als solches tatsächlich Anwendung? Und bringt das der Gesundheit nicht mehr Schaden als Nutzen? Sonst würde es doch wahrscheinlich schon Kindern im Schulsport verabreicht?--**** (nicht signierter Beitrag von 87.155.41.138 (Diskussion) 12:00, 25. Aug. 2014 (CEST))
Wo ist der Kohlenstoff in der Strukturformel?
[Quelltext bearbeiten]Die Summenformel lautet C3H8O3, das Zeugs muss also 3 Kohlenstoffatome haben. Die sind in der Grafik zur Strukturformel aber gar nicht zu sehen, warum? Vielleicht ist das ne doofe Frage, allerdings bin ich kein Chemiker und bisher immer davon ausgegangen, dass die Anzahl an Elementen in der Summenformel als auch grafischen Sturkturformel immer gleich sein muss. Wenn dem nicht so ist, dann bitte ich um Erläuterung. --77.0.49.24 13:45, 11. Nov. 2015 (CET)
- Hi,
- das ist eine Frage der Darstellung. Hier gewählt wurde die so genannte Skelettformel, bei der die C-Atome das Grüst darstellen und nciht explizit benannt werden. Sie sind also an den Stellen, an denen "Knicke" oder Verzweigungen auftauchen. In der Valenzstrichformel werden dagegen alle Atome gezeigt, es gibt aber auch Mischformen:
-
Fischerprojektion mit Skelettanteil
- Alle Formen sind korrekt und sinnvoll - man muss sie nur verstehen. Neben den gezeigten gibt es zahlreiche weitere Möglichkeiten, die Moleküle darzustellen. Gruß -- Achim Raschka (Diskussion) 14:10, 11. Nov. 2015 (CET)
- Vielen Dank für deine Antwort. Das mit den Knicken wusste ich nicht. --77.0.49.24 16:53, 11. Nov. 2015 (CET)
kein zuckeralkohol
[Quelltext bearbeiten]sondern ein kohlenhydrat ist glycerin (nicht signierter Beitrag von Dnvuma (Diskussion | Beiträge) 14:00, 14. Sep. 2020 (CEST))
Geschichte
[Quelltext bearbeiten]Irgendwie verstehe ich nicht, warum Glyzerin erst 1779 "entdeckt" wurde . . . . also die "Verseifung" als chemische Reaktion ist mindestens 2000 Jahre alt. Und bei der Verseifung entsteht IMMER - unter anderem - ein Gemisch von Glyzerin und Wasser. Es mag jetzt sein, dass bis Scheele niemand das Gemisch trennen konnte oder wollte . . . oder niemand eine Anwendung für Glyzerin hatte. Aber der Stoff (als Gemsich mit Wasser) an sich war sicherlich schon lange bekannt. Tö Pentaclebreaker (Diskussion) 09:01, 20. Sep. 2024 (CEST)