Koronare Herzkrankheit
| Klassifikation nach ICD-10 | |
|---|---|
| I20 – I25 | Ischämische Herzkrankheiten |
| ICD-10 online (WHO-Version 2019) | |

– Herzkammern und -vorhöfe (weiß): rechter Ventrikel (RV), rechter Vorhof (RA) und linker Ventrikel (LV).
Der linke Vorhof (LA) wird durch den linken Ventrikel verdeckt.
– Arterien (rot) und Venen (blau) des großen und kleinen Kreislaufs: Aortenbogen der Aorta (A), Truncus pulmonalis (TP) mit linker und rechter Pulmonalarterie (RPA und LPA) sowie Vena cava superior und inferior (VCS und VCI) sowie die linken Pulmonalvenen (PV).
Die rechten Pulmonalvenen sind durch den rechten Ventrikel verdeckt.
– Koronararterien (orange): Hauptstamm der linken Koronararterie (LCA) mit den Hauptästen Ramus circumflexus (RCX) und Ramus interventricularis anterior (RIVA) sowie der Hauptstamm der rechten Koronararterie (RCA) mit den Hauptästen Ramus interventricularis posterior (RIP) und Ramus posterolateralis (RPL).
Der Ursprung der Coronararterien ist in dieser Zeichnung fälschlicherweise an der Wurzel der Pulmonalarterien und nicht im Bereich der Aortenwurzel eingezeichnet!
– Die Koronarvenen sind nicht dargestellt.
Eine koronare Herzkrankheit (von altgriechisch κορώνα korona: „Krone“, „Kranz“; kurz KHK, auch (chronische) ischämische Herzkrankheit, IHK) ist eine Erkrankung der Herzkranzgefäße (Koronararterien).
Sie wird in den meisten Fällen durch Arteriosklerose (umgangssprachlich „Arterienverkalkung“) verursacht. Hierbei bedingen Ablagerungen in und nicht etwa an den Gefäßwänden eine Versteifung dieser sowie eine zunehmende Verminderung des Gefäßquerschnitts (obstruktive KHK) bis zur vollständigen Verstopfung. Die Folge einer Koronarsklerose ist eine Beeinträchtigung der Durchblutung und damit eine verminderte Sauerstoffversorgung der Herzmuskulatur. Es entsteht ein Missverhältnis zwischen Sauerstoffbedarf und Sauerstoffangebot, welches als Myokard-Ischämie (beschreibt die Auswirkung auf die Muskulatur) oder als Koronarinsuffizienz (beschreibt die Ursache an den Herzkranzgefäßen) bezeichnet wird.
Das Leitsymptom der KHK und Hauptmerkmal der Koronarinsuffizienz ist die Angina pectoris (Brustenge). Mit zunehmendem Fortschreiten der Erkrankung erhöht sich die Wahrscheinlichkeit für das Auftreten von Begleiterscheinungen wie Herzrhythmusstörungen und Herzinsuffizienz sowie akuten lebensbedrohlichen Komplikationen wie Herzinfarkt und plötzlicher Herztod.
Die KHK ist eine chronische Erkrankung, die im Verlauf von Jahren bis Jahrzehnten fortschreitet. Eine Heilung, d. h. die Beseitigung der Ursache im Sinne einer Entfernung der Ablagerungen in den betroffenen Gefäßwänden, ist zurzeit nicht möglich, jedoch kann die zunehmende Verschlechterung verzögert oder angehalten werden. Hierzu gibt es eine ganze Reihe von Möglichkeiten, die von einer Ernährungsumstellung bis zur Umstellung der Lebensgewohnheiten reichen. Des Weiteren kann die koronare Herzkrankheit medikamentös, durch therapeutische Eingriffe mittels Herzkatheter und operativ behandelt werden.
Die KHK ist mit ihren akuten Manifestationen die häufigste Todesursache in den Industrienationen.[1][2][3]
Definition
[Bearbeiten | Quelltext bearbeiten]Der Begriff der koronaren Herzkrankheit wird in der Literatur nicht von allen Autoren einheitlich definiert. Die koronare Herzkrankheit wird in vielen Lehrbüchern und in der nationalen Versorgungsleitlinie der Bundesärztekammer als die Manifestation der Arteriosklerose an den Herzkranzarterien definiert.[4][5] Darüber hinaus gibt es auch eine etwas weiter gefasste Definition. Hiernach entsteht die koronare Herzkrankheit durch eine Koronarinsuffizienz, bei der neben der Arteriosklerose noch zahlreiche andere Ursachen zugrunde liegen können.[2][6]
Epidemiologie
[Bearbeiten | Quelltext bearbeiten]Herz-Kreislauf-Erkrankungen, zu denen unter anderem die KHK gehört, sind mit Abstand die häufigste Todesursache in den Industrienationen.[7][8] Dabei führen die KHK und ihre Manifestationen die Todesstatistik an. In Deutschland wurden im Jahr 2005 insgesamt mehr als 17 Prozent aller registrierten Todesfälle durch chronische KHK und Herzinfarkt verursacht.[9] Die Inzidenz der KHK beträgt etwa 0,6 % pro Jahr über alle Altersklassen hinweg mit Zunahme in den höheren Altersklassen. Inzidenz bedeutet in diesem Zusammenhang, dass die Erkrankung sich klinisch manifestiert. In etwa 50 % der Fälle ist das Erstereignis ein Herzinfarkt, bei 10 % ein plötzlicher Herztod und beim Rest der Fälle definitionsgemäß eine instabile Angina pectoris. Etwa 2 % der Bevölkerung leiden unter einer asymptomatischen KHK, das heißt, einer Durchblutungsstörung des Herzens ohne Krankheitserscheinungen wie Angina pectoris.
Ursachen und Krankheitsentstehung
[Bearbeiten | Quelltext bearbeiten]Unabhängig davon, welche Definition zugrunde gelegt wird, ist die Arteriosklerose die Hauptursache der koronaren Herzkrankheit. Andere Ursachen treten sehr häufig in Kombination mit der Arteriosklerose auf. Für die Arteriosklerose gibt es zahlreiche Risikofaktoren, deren Vermeidung für die Vorbeugung (Prävention) dieser Erkrankung eine wichtige Rolle spielt.
Ursachen und Entstehung der Arteriosklerose
[Bearbeiten | Quelltext bearbeiten]
Die Arteriosklerose (im Volksmund auch als Arterienverkalkung bezeichnet) oder Atherosklerose ist die häufigste Systemerkrankung von Arterien. Nach der Definition der Weltgesundheitsorganisation (WHO) ist die Arteriosklerose eine variable Kombination von Veränderungen der Gefäßinnenwand (Intima) der Arterien, bestehend aus herdförmiger Ansammlung von Fettsubstanzen, komplexen Kohlenhydraten, Blut und Blutbestandteilen, Bindegewebe und Kalziumablagerungen, verbunden mit Veränderungen der Gefäßmuskelschicht (Media).[10]
Diese Veränderungen führen zu Verhärtung der Gefäßwände, was mit einem Elastizitätsverlust einhergeht, sowie zu einer Verengung der Gefäßlichtung durch Wandverdickungen (arteriosklerotische Plaques) und sekundäre Thrombosen. Dadurch wird die Durchblutung des Herzmuskels eingeschränkt. In Abhängigkeit vom Ausmaß der Arteriosklerose kann der Herzmuskel bei körperlicher Belastung und psychischer Erregung oder bereits in Ruhe nicht mehr ausreichend durchblutet werden (Koronarinsuffizienz). Die Entstehung der Arteriosklerose ist ein in Stadien ablaufender, schleichender und fortschreitender Prozess, der über viele Jahre bis Jahrzehnte andauert. Zahlreiche Risikofaktoren begünstigen die Entstehung der Arteriosklerose.
Risikofaktoren der Arteriosklerose
[Bearbeiten | Quelltext bearbeiten]Die Risikofaktoren für die Entstehung einer koronaren Arteriosklerose bei KHK und der entsprechenden Gefäßveränderungen bei anderen Erkrankungen, beispielsweise der peripheren arteriellen Verschlusskrankheit, unterscheiden sich nur unwesentlich. Allerdings gibt es einen spezifischen Bezug der Risikofaktoren zur KHK, der insbesondere hinsichtlich epidemiologischer Daten von Bedeutung ist.
Zu den Risikofaktoren gehören nicht beeinflussbare oder konstitutionelle Risiken, wie eine genetische Prädisposition, das Alter und das Geschlecht des Patienten. Zu den beeinflussbaren Risikofaktoren gehören Fettstoffwechselstörungen im Allgemeinen und ein erhöhter Cholesterinspiegel (Hypercholesterinämie) im Speziellen, Übergewicht, Tabakrauchen, arterielle Hypertonie (arterieller Bluthochdruck), Diabetes mellitus, Bewegungsmangel und psychosoziale Faktoren. Die einzelnen Risikofaktoren wirken nicht nur additiv, sondern erhöhen zusammen das kardiovaskuläre Risiko überproportional (synergistisch).[2]
Die Hypercholesterinämie gehört, zusammen mit Tabakrauchen, arteriellem Hypertonus und dem Diabetes mellitus, in Bezug auf Morbidität und Mortalität, zu den wichtigsten beeinflussbaren Risikofaktoren der KHK. In mehreren großen Studien konnte gezeigt werden, dass das kardiovaskuläre Risiko mit einer Erhöhung des Gesamtcholesterins und LDL-Cholesterins[11][12] sowie der Phospholipase A₂[13][14] steigt. Das HDL-Cholesterin wirkt dagegen kardioprotektiv. Raucher haben in Abhängigkeit von der Anzahl täglich gerauchter Zigaretten und der Anzahl der Jahre, in denen geraucht wurde (Zigarettenpackungsjahre, pack-years) ein 2–5-fach erhöhtes Risiko, einen Herzinfarkt zu erleiden. Zwischen Blutdruck und dem Risiko, an einer KHK zu erkranken, besteht ab systolischen Werten über 125 mmHg und diastolischen Werten über 85 mmHg eine lineare Beziehung, das heißt, dass über den genannten Blutdruckwerten das Risiko proportional mit der Erhöhung des Blutdrucks steigt.[2] Diese Faktoren werden zur Systematic Coronary Risk Evaluation verwendet. Mehr als die Hälfte der an Diabetes mellitus erkrankten Patienten versterben an einer KHK. Diabetiker haben im Vergleich zu Nichtdiabetikern ein 2–3fach erhöhtes Risiko, an einer KHK zu erkranken.[15]
Des Weiteren stellt auch eine Strahlentherapie im Rahmen einer Krebstherapie, z. B. bei Brustkrebs, ein Risiko für eine koronare Herzerkrankung dar. Das Risiko steigt abhängig von der Organdosis des Herzens um etwa 7,4 % pro Gray, mit einem Anstieg des Risikos nach fünf Jahren bis über zwanzig Jahre, ohne dass ein Schwellenwert besteht und unabhängig von weiteren kardiologischen Risikofaktoren.[16]
Ursachen der Koronarinsuffizienz
[Bearbeiten | Quelltext bearbeiten]Alle im Folgenden genannten Ursachen steigern für sich allein und vor allem in Kombination mit einer Arteriosklerose die Wahrscheinlichkeit, eine koronare Herzkrankheit zu entwickeln. In Bezug auf die Pathophysiologie kann zwischen einer Verminderung des Sauerstoffangebots und einer Erhöhung des Sauerstoffbedarfs unterschieden werden.
Zu einer Verminderung des Sauerstoffangebots kann es unter anderem durch eine Verengung des Gefäßlumens kommen. Als Ursache spielen neben der Arteriosklerose vor allem Thrombosen und Embolien, infektiöse oder autoimmune Entzündungen der Gefäße (Vaskulitiden) und Koronarspasmen eine Rolle. Letztere können auch durch verschiedene Medikamente und durch Drogenmissbrauch (z. B. bei Kokain-Missbrauch) verursacht werden. Eine Kompression der Koronararterien von außen, beispielsweise bei Herzhypertrophie oder verschiedenen Tumoren, führt ebenfalls zu einer Verminderung des Sauerstoffangebots. Darüber hinaus ist die Hypoxämie (zum Beispiel bei Anämie, Ateminsuffizienz und Kohlenmonoxidvergiftung), bei welcher der Sauerstoffgehalt im Blut vermindert ist, eine mögliche Ursache der Koronarinsuffizienz. Auch eine Zunahme der Blutviskosität, wie sie bei Leukämien vorkommt, ist eine weitere seltene Ursache.
Eine Erhöhung des Sauerstoffbedarfs tritt unter anderem bei Herzmuskelhypertrophie, bestimmten Formen der Kardiomyopathie, Herzklappenerkrankungen, Hyperthyreose, Bluthochdruck, Infektionskrankheiten und Fieber auf. Auch körperliche Belastung und emotionaler Stress erhöhen den Sauerstoffbedarf. Diese Belastungen lösen aber nur eine Koronarinsuffizienz aus, wenn entsprechende Erkrankungen vorliegen.[2]
Klinische Erscheinungen
[Bearbeiten | Quelltext bearbeiten]Das Leitsymptom der KHK ist die Angina pectoris. Synonyme sind die Kurzform AP-Symptomatik sowie pektanginöse Beschwerden. Für die chronische KHK sind weitere Symptome relativ unspezifisch. Neben der AP-Symptomatik treten häufig Atemnot (Dyspnoe), Blutdruckabfall (Hypotonie), eine Erhöhung der Herzfrequenz (Tachykardie), vermehrte Schweißproduktion, Gesichtsblässe und Todesangst auf. Eine KHK verläuft nicht selten asymptomatisch. Das bedeutet, dass bei diesen Patienten keine AP-Symptomatik oder andere Symptome auftreten. Diese Form der KHK wird als latente KHK oder stumme Myokardischämie bezeichnet, die häufig bei älteren Patienten und bei Diabetikern auftritt. Bei Letzteren spielt die diabetische Polyneuropathie, die durch den gestörten Zuckerstoffwechsel verursacht wird, eine entscheidende Rolle. Die Diagnose einer asymptomatischen KHK ist schwierig. Dadurch, dass die Patienten keine Schmerzen bei Myokardischämien verspüren, werden Herzinfarkte und andere Manifestationen der KHK häufig gar nicht oder zu spät bemerkt.
Angina pectoris als Leitsymptom
[Bearbeiten | Quelltext bearbeiten]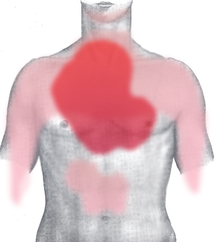
rot: häufig und stark
rosa: selten oder ausstrahlend

Bei der Angina pectoris handelt es sich typischerweise um dumpfe, drückende, einschnürende und häufig brennende Schmerzen, die hinter dem Brustbein (retrosternal) lokalisiert sind. Von den Betroffenen wird der Schmerz häufig als „Engegefühl in der Brust“ beschrieben. Typisch ist außerdem eine Ausstrahlung des Schmerzes in den linken oder seltener in beide Arme. Darüber hinaus können pektanginöse Beschwerden ein atypisches Bild zeigen (atypische Angina pectoris), das heißt, sie können einen anderen Schmerzcharakter sowie eine andere Schmerzlokalisation haben, und sie können in andere Körperregionen (Hals, Unterkiefer, Oberbauch, Rücken) oder überhaupt nicht ausstrahlen. Der Mechanismus, wie es zu einer Schmerzwahrnehmung (Nozizeption) bei Ischämie kommt, ist bisher noch nicht sicher geklärt.
Eine Reihe anderer Erkrankungen können sich ebenfalls durch Brustschmerz äußern.
Stabile Angina pectoris
[Bearbeiten | Quelltext bearbeiten]Es gibt verschiedene Formen der Angina pectoris. Die stabile Angina pectoris ist das führende Symptom der chronischen KHK. (Das chronische Koronarsyndrom wurde früher stabile KHK genannt[17]). Dabei handelt es sich um sich wiederholende, kurzzeitige Schmerzanfälle mit der oben beschriebenen Symptomatik, die bei körperlicher Belastung auftreten. Dabei verbraucht der Herzmuskel mehr Sauerstoff. Die sklerotischen Koronararterien können jedoch der Herzmuskulatur nicht genügend Sauerstoff zuführen. Die stabile Angina pectoris tritt im Anfangsstadium vor allem bei Belastung auf und wird daher als „Belastungsangina“ bezeichnet. Nach Beendigung der Belastung sind die Patienten in der Regel nach wenigen Minuten wieder beschwerdefrei. Eine Ausnahme bildet eine Sonderform der stabilen Angina pectoris, die sogenannte „Walk-through-Angina“. Wenn die körperliche Belastung über längere Zeit beibehalten wird, bessern sich die Beschwerden bei dieser Form wieder. Neben der körperlichen Belastung gibt es noch andere Ursachen, die eine stabile Angina pectoris auslösen können. Dazu gehören psychische Erregung, Kälte und ausgiebige Mahlzeiten. Charakteristisch für die stabile Angina pectoris ist darüber hinaus, dass die Gabe von Nitraten („Nitropräparate“) im Anfall zu einer raschen Besserung der Schmerzen führt. Nitropräparate führen zu einer Erweiterung der Blutgefäße. Im Herzmuskel (und anderen Organen) wird dadurch die Durchblutung gesteigert und das Sauerstoffdefizit, das die AP-Symptomatik ausgelöst hat, beseitigt. Die stabile Angina pectoris kann nach der CCS-Klassifikation (Klassifikation der Canadian Cardiovascular Society) in verschiedene Schweregrade eingeteilt werden. Dies spielt vor allem für die Therapie der chronischen KHK eine Rolle.
Instabile Angina pectoris
[Bearbeiten | Quelltext bearbeiten]Von der stabilen Angina pectoris müssen andere Formen abgegrenzt werden, insbesondere die instabile Angina pectoris, die im Rahmen eines akuten Koronarsyndroms auftreten kann. Jede erstmals aufgetretene Angina pectoris bei zuvor asymptomatischen Patienten wird als instabile Angina pectoris gewertet. Als instabile Angina pectoris wird außerdem eine AP-Symptomatik bezeichnet, die in Ruhe auftritt („Ruheangina“), sowie eine AP-Symptomatik, die in Stärke, Dauer und/oder Frequenz zunimmt („Crescendo-Angina“). Die Unterscheidung zwischen stabiler und instabiler Angina pectoris hat eine große differentialdiagnostische Bedeutung.
Buddenbrook-Syndrom
[Bearbeiten | Quelltext bearbeiten]Das Buddenbrook-Syndrom ist eine sehr seltene, aber umso mehr gefürchtete Fehldiagnose in der Zahnheilkunde. Zahnschmerzenähnliche Beschwerden im Unterkiefer, bevorzugt der linken Seite, führen zum Aufsuchen eines Zahnarztes. Sollte sich tatsächlich ein medizinisches Korrelat finden lassen, beispielsweise ein pulpitischer oder devitaler, eitriger Zahn, bleibt die Primärursache unentdeckt, nämlich eine koronare Herzerkrankung, was lebensbedrohlich sein kann.
Untersuchungsmethoden
[Bearbeiten | Quelltext bearbeiten]
An erster Stelle steht die Basisdiagnostik. Die Diagnosemaßnahmen, die ein Arzt einleitet, um eine chronische KHK zu diagnostizieren, hängen ab von der Manifestation der KHK und dem Schweregrad. Der typische an chronischer KHK erkrankte Patient leidet meist unter einer stabilen Angina pectoris. Bei diesen kann mit Hilfe einer ausführlichen Anamnese mit Risikostratifizierung, einer körperlichen Untersuchung, der Auswertung verschiedener Laborparameter sowie der Interpretation eines Ruhe- und Belastungs-Elektrokardiogramms eine relativ sichere Verdachtsdiagnose erhoben werden. Eine erweiterte Diagnoseprozedur ist meist nicht erforderlich.
Dagegen ist die Diagnose einer asymptomatischen KHK schwierig. Die Erstmanifestation der KHK ist in diesen Fällen sehr häufig das akute Koronarsyndrom. Allerdings können regelmäßige Hausarztbesuche mit auf den Patienten zugeschnittenen Untersuchungen dazu beitragen, dass diese Form rechtzeitig erkannt wird, bevor es zu einer lebensbedrohlichen Komplikation kommt. Bei Patienten mit Verdacht auf ein akutes Koronarsyndrom unterscheidet sich die Diagnoseprozedur maßgeblich zur chronischen KHK.
Bei Verdacht auf eine obstruktive KHK empfiehlt die europäische Leitlinie (Stand 2019) eine CT-Angiografie oder einen nichtinvasiven Ischämie-Test, gegebenenfalls gefolgt von einer invasiven Koronarangiografie.[18]
Basisdiagnostik
[Bearbeiten | Quelltext bearbeiten]Anamnese
[Bearbeiten | Quelltext bearbeiten]Die Verdachtsdiagnose der KHK kann häufig schon durch eine ausführliche Anamnese gestellt werden. Wenn ein Patient unter den typischen pektanginösen Beschwerden leidet, ist dies hochverdächtig für das Vorliegen einer KHK. Um den Verdacht zu erhärten, sollte der Patient möglichst genau zum Schmerzcharakter, zu bestehenden Risikofaktoren sowie zu Begleitsymptomen und anderen bekannten Erkrankungen wie der peripheren arteriellen Verschlusskrankheit (PAVK) und zurückliegenden Schlaganfällen befragt werden, deren Hauptursache ebenfalls die Arteriosklerose ist. Patienten mit einer PAVK oder zurückliegenden Schlaganfällen haben ebenfalls ein erhöhtes Risiko, an einer KHK zu erkranken. Zusätzlich sollte eine ausführliche Familienanamnese erhoben werden, um zu klären, ob Herzkreislauferkrankungen naher Verwandter bekannt sind, da eine genetische Prädisposition vorliegen könnte, die das Risiko für eine chronische KHK erhöhen würde.[2] Durch eine genaue Anamnese können die meisten Differentialdiagnosen mit hoher Wahrscheinlichkeit ausgeschlossen werden.
Körperliche Untersuchung
[Bearbeiten | Quelltext bearbeiten]Für die KHK charakteristische Untersuchungsbefunde lassen sich sehr selten erheben.[2] Die körperliche Untersuchung dient vor allem einer Erhärtung der Verdachtsdiagnose sowie dem Aufdecken eventuell vorhandener Begleiterkrankungen und Risikofaktoren. Die im Folgenden genannten Beispiele stellen nur eine kleine Auswahl von möglichen Untersuchungsbefunden dar. So können eventuell Zeichen einer Hypercholesterinämie wie Xanthelasmen und Xanthome als Risikofaktoren aufgedeckt werden. Kalte Beine und fehlende periphere Pulse können auf eine periphere arterielle Verschlusskrankheit (PAVK) hinweisen. Gefäßgeräusche, beispielsweise bei Auskultation der Arteria carotis externa, sind ebenfalls häufig bei Arteriosklerose zu finden. Durch Auskultation des Herzens können andere Herzerkrankungen, wie beispielsweise eine Aortenklappenstenose, als Ursache für die Brustschmerzen aufgedeckt werden. Rasselgeräusche bei Auskultation der Lunge, eine sichtbare Stauung der Halsvenen, Unterschenkelödeme sowie eine tastbare Leber können auf eine manifeste Herzinsuffizienz hinweisen. Die Palpation der Leber und bestimmte Veränderungen des Auges und Geschwüre der Unterschenkel (Ulcera crurum) sind häufig Zeichen einer manifesten Zuckerkrankheit (Diabetes mellitus). Mit einer Augenhintergrundspiegelung kann ein über längere Zeit bestehender Bluthochdruck aufgedeckt werden.[6] Zur körperlichen Untersuchung gehört im weitesten Sinne auch die routinemäßige Blutdruckmessung, mit der ein eventuell vorhandener Bluthochdruck, ein wichtiger Risikofaktor der KHK, diagnostiziert werden kann.
Labor
[Bearbeiten | Quelltext bearbeiten]Zum Nachweis von Risikofaktoren (Diabetes mellitus und Fettstoffwechselstörungen) werden Blutzucker, HbA1c, LDL-, HDL-, Gesamtcholesterin und Triglyceride bestimmt. Als Weiteres üblicherweise zusätzlich das kleine Blutbild, Entzündungsparameter und TSH. Außerhalb der klinischen Praxis kann eine Protein-Muster-Diagnostik zur Bestimmung des Artherioskleroserisikos durchgeführt werden.
Bei instabiler Angina pectoris und Verdacht auf Herzinfarkt ist die Bestimmung von herzspezifischen Nekrosemarkern notwendig. Das herzspezifische Protein Troponin[19] ist hier der erste Marker für eine akute Ischämie. Im weiteren Verlauf steigen die Creatinkinase (CK) und dessen herzspezifischer Anteil (CK-MB) an sowie Glutamat-Oxalacetat-Transaminase (GOT) und Lactatdehydrogenase (LDH).
Elektrokardiogramm
[Bearbeiten | Quelltext bearbeiten]
Das EKG ist eine nicht-invasive Untersuchungsmethode, bei der die elektrische Aktivität der Herzmuskulatur mit Elektroden abgeleitet wird. Es gibt im Wesentlichen drei verschiedene Formen, die bei der Diagnose einer chronischen KHK von Bedeutung sind. Das Ruhe-EKG ist Bestandteil der Basisdiagnostik. Belastungs-EKG und Langzeit-EKG werden in Abhängigkeit vom Risikoprofil des Patienten und der Vortestwahrscheinlichkeit durchgeführt.
Ruhe-EKG
[Bearbeiten | Quelltext bearbeiten]Das Ruhe-EKG gehört zur grundlegenden internistischen Diagnostik, nicht nur bei Verdacht auf eine koronare Herzkrankheit. Für einen sicheren Nachweis einer chronischen KHK ohne bisher abgelaufenen Herzinfarkt ist das Ruhe-EKG allerdings eher ungeeignet. Es kommen Zeichen zur Darstellung, die für einen abgelaufenen Infarkt oder auch eine Verdickung des Herzmuskels im Rahmen einer Bluthochdruckerkrankung sprechen. Im Weiteren können Herzrhythmusstörungen wie Vorhofflimmern oder häufige Extraschläge (ventrikuläre Extrasystolie) gesehen werden, die ebenfalls ein indirektes Zeichen für das Vorliegen einer KHK sein können.[4]
Belastungs-EKG
[Bearbeiten | Quelltext bearbeiten]
A in Ruhe
B bei 75 Watt
C bei 100 Watt
D bei 125 Watt
Das Belastungs-EKG wird meist mit einem Fahrradergometer aufgezeichnet, abhängig vom Zustand des Patienten entweder im Liegen oder Sitzen. Es stellt den nächsten Schritt in der Diagnostik bei Verdacht auf eine koronare Herzerkrankung dar. Die Sensitivität (50–70 %) und Spezifität (60–90 %) sind bedeutend höher als beim Ruhe-EKG. Wie hoch, ist u. a. abhängig vom Schweregrad der Erkrankung, vom Geschlecht und vom Ausmaß der Belastung (Erreichen der Ausbelastungs-Herzfrequenz). Der Verdacht auf eine bestehende chronische KHK wird durch Erregungsrückbildungsstörungen unter Belastung, das vermehrte Auftreten von Extraschlägen oder plötzlichen Blutdruckabfall unter Belastung erhärtet.
Manche Herzmedikamente (Digitalisglykoside) erschweren die Beurteilbarkeit von Erregungsrückbildungsstörungen, auch kann die Einnahmen von herzfrequenzsenkenden Medikamenten die Beurteilbarkeit einschränken, da die Zielfrequenz nicht erreicht wird und der Patient so nicht voll ausgelastet ist. Der Verdacht auf einen akuten Herzinfarkt ist eine absolute Kontraindikation, und auch bei schon vor der Untersuchung deutlich überhöhtem Blutdruck oder Herzfrequenz sollte sie nicht durchgeführt werden.
Langzeit-EKG
[Bearbeiten | Quelltext bearbeiten]Ist der Befund des Belastungs-EKGs negativ, es besteht jedoch weiterhin die Verdachtsdiagnose chronische KHK, kann ein Langzeit-EKG sinnvoll sein. Insbesondere für das Aufdecken stummer Ischämien kann es hilfreich sein. Ein positives Testergebnis liegt mit hoher Wahrscheinlichkeit vor, wenn wiederholt ST-Streckensenkungen auftreten, die länger als 1 Minute andauern.[1] In der Praxis wird das Langzeit-EKG für diese Indikation eher selten verwandt.
Echokardiographie
[Bearbeiten | Quelltext bearbeiten]Im Rahmen der Ultraschall-Untersuchung des Herzens können Wandbewegungsstörungen gesehen werden, die nach abgelaufenem Herzinfarkt im Sinne einer Narbe bestehen bleiben. Aber auch diverse andere Erkrankungen des Herzens (Klappen, Herzmuskel) können erkannt werden.
Dopplersonographie der Gefäße
[Bearbeiten | Quelltext bearbeiten]Unter dem Gesichtspunkt, dass alle Gefäße im Körper etwa gleich stark von Atherosklerose betroffen sind, kann eine Dopplersonographie der Gefäße, meist der Halsschlagadern durchgeführt werden. Sind hier Veränderungen zu sehen, ist die Wahrscheinlichkeit hoch, dass an anderen Stellen, wie z. B. den Herzkranzgefäßen, ebenfalls Veränderungen vorliegen.
Risikostratifizierung
[Bearbeiten | Quelltext bearbeiten]In der Zusammenschau der erhobenen Befunde wird im Rahmen einer Risikostratifizierung das weitere diagnostische Vorgehen geplant. Es muss die Entscheidung gefällt werden, ob die Beschwerden
- mit höchster Wahrscheinlichkeit nicht vom Herzen kommen, dann muss nach anderen Ursachen geforscht werden,
- sie eher nicht vom Herzen kommen und man weitere nicht-invasive Diagnostik macht, oder
- die Wahrscheinlichkeit für das Vorliegen einer relevanten KHK als eher hoch bis sicher eingeschätzt wird.
Eine wertvolle Hilfe stellt das Punktesystem des Euro Heart Survey dar, bei dem Punkte für Risikofaktoren, Schweregrad der stabilen Angina pectoris und Komorbiditäten vergeben werden.[20]
| Risikofaktor | Punkte |
|---|---|
| Eine oder mehrere Komorbiditäten | 86 |
| Diabetes mellitus | 57 |
| Schweregrad der Angina pectoris | |
|
0 |
|
54 |
|
91 |
| Symptome > 6 Monate CCS III | 80 |
| Beeinträchtigte linksventrikuläre Funktion | 114 |
| ST-Streckensenkung oder T-Negativierung im EKG | 34 |
Erweiterte Diagnostik
[Bearbeiten | Quelltext bearbeiten]Die weiterführende Diagnostik bei bestehendem Verdacht auf eine koronare Herzkrankheit verfolgt zwei Ziele: zum einen den Nachweis von belastungsabhängigen Wandbewegungsstörungen der Herzkammern. Liegen diese vor, besteht die hohe Wahrscheinlichkeit, dass das den Wandabschnitt mit Blut versorgende Gefäß verengt und der Blutfluss unter der Belastung nicht ausreichend ist. Hierfür werden die Stress-Echokardiographie, die Myokardszintigraphie und seit kurzem auch die Magnetresonanztomographie des Herzens (Cardio-MR) verwendet. Das zweite Ziel ist die Darstellung der Herzkranzgefäße als Nachweis der vermuteten Gefäßenge, klassisch mit Hilfe der Koronarangiographie und seit neuerem auch nicht-invasiv mit einer Computertomographie des Herzens.
Stressechokardiographie
[Bearbeiten | Quelltext bearbeiten]Bei der Stressechokardiographie wird der Herzmuskel unter Belastung mittels Ultraschallbildgebung dargestellt. Die Belastung wird hierbei, ähnlich dem Belastungs-EKG, durch Fahrradfahren im Liegen erzeugt oder auch mittels Medikamenten. Durch die Belastung soll bei klinisch relevanter Stenose eine Wandbewegungsstörung ausgelöst werden.[21]
Myokardszintigraphie
[Bearbeiten | Quelltext bearbeiten]Bei der Myokardszintigraphie handelt es sich um eine nuklearmedizinische Untersuchungsmethode, deren Hauptindikation die Erfassung einer KHK bei mittlerer Wahrscheinlichkeit ist. Als Radionuklid wird 201Thallium oder 99mTechnetium verwendet, die jeweils intravenös injiziert werden. Mit der Myokardszintigraphie lassen sich Ausmaß, Schweregrad und Lokalisation der Ischämie feststellen sowie Aussagen über die Prognose des Patienten treffen. Die Myokardszintigraphie ist bezüglich Sensitivität und Spezifität dem Belastungs-EKG überlegen, insbesondere bei Vorliegen einer 1-Gefäßerkrankung.[1]
Zur Diagnose der KHK wird die Myokardszintigraphie zunächst, wenn keine Kontraindikationen bestehen, bei Belastung auf einem Fahrradergometer durchgeführt. Alternativ, wenn eine körperliche Belastung nicht möglich ist, kann diese pharmakologisch induziert werden, beispielsweise mit den Vasodilatatoren Adenosin und Dipyridamol oder dem Katecholaminanalogon Dobutamin.[4][22] Beim Gesunden kann die Durchblutung bei Belastung erheblich gesteigert werden, beim KHK-Patienten gibt es in Abhängigkeit von den betroffenen Koronararterien in bestimmten Arealen Durchblutungsdefizite. Nach mehrstündiger Pause wird erneut ein Szintigramm angefertigt, allerdings ohne Belastung des Patienten. In dieser Zeit hat sich die Durchblutung normalisiert, so dass sich der Tracer gleichmäßig im Herzmuskel verteilt. Finden sich dieselben Areale mit verminderter Anreicherung, handelt es sich mit hoher Wahrscheinlichkeit um eine irreversible Myokardischämie, das heißt, um eine Infarktnarbe, die durch einen zurückliegenden Herzinfarkt verursacht wurde.
Die Untersuchung mit 201Thallium kann neben Aussagen zur Durchblutung zusätzlich Informationen zur Vitalität des Herzmuskels geben.
Die Myokardszintigraphie mit 99mTechnetium kann wegen der besseren Ausbeute als Herzphasen-getriggerte Aufnahme durchgeführt werden, soweit keine ausgeprägten Herzrhythmusstörungen vorliegen. Dadurch lassen sich die Funktion der linken Herzkammer unter Belastung und in Ruhe beurteilen und indirekt endsystolisches und enddiastolisches Volumen sowie die Auswurffraktion bestimmen. Während der Belastung treten bei KHK-Patienten Wandbewegungsstörungen des Herzens auf, und die Auswurffraktion verringert sich.[1]
Magnetresonanztomographie des Herzens
[Bearbeiten | Quelltext bearbeiten]Das Cardio-MR ist eine noch relativ neue, zeitaufwendige, wenig verbreitete Untersuchungsmethode, die in absehbarer Zeit möglicherweise die Myokardszintigraphie verdrängen wird. Hierbei wird unter medikamentöser Belastung ebenfalls nach Wandbewegungsstörungen gesucht, zusätzlich können Aussagen über die Pumpleistung und abgelaufene Entzündungen des Herzmuskels gemacht werden. Wird keine Wandbewegungsstörung gesehen, ist eine koronare Herzerkrankung mit annähernd 100%iger Sicherheit ausgeschlossen.
Koronarangiographie und Ventrikulographie
[Bearbeiten | Quelltext bearbeiten]

Mit Hilfe der diagnostischen Koronarangiographie können Koronararterien dargestellt und deren Anatomie sowie das Ausmaß und die Lokalisation eventueller Stenosen beurteilt werden. Sie ist die Untersuchung mit der besten Aussagekraft. Bei dieser Untersuchung wird ein Herzkatheter über die Arteria femoralis (Oberschenkelarterie) oder seltener über die Arteria brachialis (Oberarmarterie) bis zu den Abgängen der Koronararterien aus der Aorta vorgeschoben und Kontrastmittel in die Abgänge injiziert. Mit Hilfe von Röntgenstrahlung können die Koronararterien sichtbar gemacht und beurteilt werden.[24] Der Katheter kann, unter Überbrückung der Aortenklappe, weiter in die linke Herzkammer vorgeschoben werden. Diese Untersuchung wird als Ventrikulografie bezeichnet. Sie ermöglicht zusätzlich regionale Kontraktionsstörungen sichtbar zu machen, die zum Beispiel Hinweise auf zurückliegende Herzinfarkte bieten können, sowie eine Beurteilung der linksventrikulären Pumpfunktion über Berechnung der Auswurffraktion und die Bestimmung der Dehnbarkeit der Herzmuskulatur (Compliance) durch Bestimmung des enddiastolischen Volumens.[1]
Da es sich bei der Koronarangiographie und der Ventrikuloangiografie um invasive Untersuchungsmethoden handelt, kann es neben relativ ungefährlichen Komplikationen (beispielsweise Hämatome an der Einstichstelle) in sehr seltenen Fällen zu schwerwiegenden lebensbedrohlichen Komplikationen kommen. Dazu gehören vor allem Herzinfarkte, Schlaganfall, Spaltungen (Dissektionen) der Gefäßwände, Herzrupturen, Luftembolien und Arrhythmien.[4] Die Letalität der Untersuchung liegt unter 1:100.[1]
Aufgrund der nicht völlig ausschließbaren Risiken für das Auftreten von Komplikationen, der Strahlenbelastung sowie der Belastung der Nieren durch das Röntgenkontrastmittel, sollte die Indikation der Koronarangiographie zur Diagnose einer chronischen KHK relativ streng gestellt und im Sinne einer Nutzen-Risikoanalyse abgewogen werden. Nach den Empfehlungen der nationalen Versorgungsleitlinie (NVL) sollte diese Untersuchung nur dann erfolgen, wenn entweder alle nicht-invasiven Untersuchungsmethoden ohne Ergebnis ausgeschöpft wurden und trotzdem die Verdachtsdiagnose chronische KHK wahrscheinlich ist, oder wenn der Patient von Revaskularisationsmaßnahmen profitieren könnte.[4] Bei der Abwägung spielen des Weiteren bestehende kardiovaskuläre Risikofaktoren, zurückliegende Herzinfarkte und andere bestehende Herz-Kreislauf-Erkrankungen, die Einschätzung der Lebensqualität durch den Patienten sowie der Schweregrad der stabilen Angina pectoris nach CCS-Klassifikation eine wichtige Rolle. Für Letztere gilt, dass bei einem CCS-Stadium < III sowie bei erfolgreicher konservativer Pharmakotherapie, normalerweise keine Indikation für eine erneute Koronarangiografie besteht.[4]
Computertomographie des Herzens
[Bearbeiten | Quelltext bearbeiten]Das Cardio-CT ist, wie auch das Cardio-MRT, ein neues, noch nicht etabliertes Untersuchungsverfahren. Hierbei wird eine Röntgenschichtaufnahme des Herzens gemacht, bei der zunächst der Kalk-Score bestimmt wird, d. h. die Menge an Kalk im erfassten Bereich. Überschreitet dieser einen bestimmten Grenzwert, wird die Untersuchung abgebrochen, da die Aussagekraft bzgl. Engstellen in den Herzkranzgefäßen zu gering ist. Kann die Untersuchung fortgeführt werden, ist die Aussagekraft über das Ausmaß einer KHK recht gut. Da bei Diagnose einer KHK im Cardio-CT eine Herzkatheteruntersuchung meist angeschlossen werden muss, sollte die Indikation, allein aus Gründen der Strahlenhygiene, eng gestellt werden. In Frage kommen hier Patienten, bei denen nur wenig für das Vorliegen einer KHK spricht, man diese aber mit nicht-invasiven Methoden doch nicht mit letzter Sicherheit ausschließen kann. Die Quantifizierung der koronaren Verkalkungen im CT erfolgt mit dem CACS (Coronary Artery Calcium Scoring), welcher 1990 von Agatston und Mitarbeitern beschrieben wurde[25].
Vorbeugung
[Bearbeiten | Quelltext bearbeiten]Unter Prävention oder Prophylaxe versteht man in der Medizin Maßnahmen, die eine Schädigung eines gesunden Organismus verhindern können (Primärprävention), die symptomlose Krankheitsfrühstadien aufdecken, so dass diese frühzeitig behandelt werden können (Sekundärprävention) sowie Maßnahmen, die Rückfälle der Erkrankung verhindern oder eine Progredienz der Erkrankung verlangsamen können (Tertiärprävention). Im Falle KHK sind die Übergänge zwischen den verschiedenen Präventionsformen fließend, so dass auf eine strenge Unterscheidung in diesem Artikel verzichtet wird.
Bei der Prävention der KHK spielt vor allem das Risikofaktoren-Management eine Rolle. Darunter versteht man Maßnahmen, die Risikofaktoren reduzieren oder besser vermeiden können. Zur Reduktion von Risikofaktoren sind insbesondere Lebensstilveränderungen des Patienten sowie eventuell eine Prävention mit Arzneimitteln notwendig. Zur Prävention gehört damit indirekt die medikamentöse Therapie von Begleiterkrankungen wie Bluthochdruck, Diabetes mellitus und Fettstoffwechselstörungen, da es sich hier ebenfalls um Risikofaktoren handelt.
Änderung des Lebensstils
[Bearbeiten | Quelltext bearbeiten]KHK-Patienten können durch Änderungen ihres Lebensstils einen wichtigen Beitrag dazu leisten, den Verlauf ihrer Erkrankung positiv zu beeinflussen. Zu den erfolgversprechenden Lebensstiländerungen gehören die Beendigung des Rauchens, eine zielgerichtete Ernährungsumstellung und eine Gewichtsreduktion bei bestehendem Übergewicht.
Das Rauchen ist einer der wichtigsten kardiovaskulären Risikofaktoren. Durch Rauchentwöhnung kann das Risiko von kardiovaskulären Ereignissen um bis zu 50 % verringert werden.[26]
Die Wirkung einer zielgerichteten Ernährungsumstellung geht über die reine Senkung des Cholesterinspiegels hinaus. Maßstab sollte die sogenannte mediterrane Kost sein, die sich durch kaloriengerechte, ballaststoffreiche und fettarme Nahrung auszeichnet und außerdem reich an ungesättigten und Omega-3-Fettsäuren ist. Neben Ernährung wirkt sich auch regelmäßige körperliche Bewegung positiv aus.[27]
Durch Berechnung des Body-Mass-Index (BMI) sowie des Bauchumfangs kann der Schweregrad des Übergewichts dokumentiert werden. Der Schweregrad korreliert mit der Häufigkeit und der Prognose der koronaren Herzkrankheit und anderen Erkrankungen, vor allem Diabetes mellitus Typ 2, arterieller Hypertonie, Herzinsuffizienz, Fettstoffwechselstörungen und Störungen der Blutgerinnung.[19]
Das Deutsche Ärzteblatt zieht in einem Übersichtsartikel zur Sekundärprävention bei KHK folgendes Fazit: „Die Wirksamkeit der angeführten Lebensstilveränderungen in der Summe dürfte die Effektivität einer kombinierten medikamentösen Therapie um das Mehrfache überschreiten.“[28] Zur dauerhaften Lebensstilveränderung kann der Besuch einer Herzschule sinnvoll sein.
| Lebensstilveränderung | Ref. | ARR % | Studiendauer (Jahre) | Anzahl Studienteilnehmer | NNT/1 Jahr |
|---|---|---|---|---|---|
| Rauchen aufgeben | [29] | 7,7 | 4,8 | 5878 | 62 |
| fettarme Kost | [30] | 16 | 3 | 100 | 19 |
| fettarme Kost | [30] | 38 | 12 | 100 | 32 |
| „mediterrane“ Kost | [31] | 12 | 4 | 605 | 33 |
| Ausgleichssport | [32] | 2,2 | 3 | 4554 | 136 |
| Stressmanagement | [33] | 20,9 | 5 | 107 | 24 |
Fettreduzierte Kost: < 20 % Fettanteil. Studien mit < 30 % erbrachten keinen Nutzen.
„Mediterrane“ Kost: Brot, Gemüse, Obst, Fisch, ungesättigte Fettsäuren, Olivenöl; wenig Fleisch.
Ausgleichssport: mindestens 3x/Woche, 30 min.
ARR = absolute Risikoreduktion für Tod sowie nichttödlichen Herzinfarkt; NNT = number needed to treat.
Walter C. Willett stellt fest, dass die Studien zu Low-Fat-Ernährung keinen signifikanten Einfluss auf das Risiko für koronare Herzkrankheit zeigen, wenn die Ernährung bei unverändertem Fettsäuresprektrum lediglich auf weniger von allem Fett abzielt. Die Studien zu Ernährungsformen, bei denen die Zufuhr von gesättigten Fettsäuren in dem Maße gesenkt werden wie die Zufuhr von ungesättigten Fettsäuren steigt, zeigten einen großen Einfluss auf das Risiko für koronare Herzkrankheit. Als Wirkungsmechanismus wird die Verringerung des Serum-Cholesterinspiegels durch weniger gesättigte Fettsäuren und mehr ungesättigte Fettsäuren in der Ernährung angesehen. Bei Risikopatienten zeige sich hierbei eine Risikoreduktion um 9 % je 10 % geringerem Serum-Cholesterinspiegel in den ersten 2 Jahren, eine Risikoreduktion um 14 % in den folgenden 3 Jahren und um 37 % nach mehr als fünf Jahren. Weitere Faktoren könnten der typischerweise hohe Gehalt von Antioxidantien in Pflanzenfetten sein, sowie der Gehalt von Omega-3-Fettsäuren z. B. in Rapsöl, die einen mäßigenden Effekt auf Herzrhythmusstörungen haben können. Besonders deutlich zeigte sich dies in der Lyon Heart Study, in der eine Variation der mediterranen Diät bei Herzpatienten zu einer Verringerung des Widerauftretens von kardiovaskulären Ereignissen um 70 % führte.[34]
Medikamentöse Prävention
[Bearbeiten | Quelltext bearbeiten]Thrombozytenaggregationshemmer
[Bearbeiten | Quelltext bearbeiten]Thrombozyten (Blutplättchen) sind kernlose Zellen, die eine wichtige Rolle bei der Blutgerinnung (Hämostase) spielen. Durch Hemmung der Thrombozytenaggregation wird die Wahrscheinlichkeit einer Thrombosebildung in den Koronararterien verringert. Die Gefahr, an einem akuten Koronarsyndrom zu erkranken oder an einem Herzinfarkt zu versterben, wird gesenkt.
Zu den gängigsten Thrombozytenaggregationshemmern gehören Acetylsalicylsäure (ASS) und Clopidogrel. Mittel der Wahl ist ASS, da der Nutzen für den Patienten, sowohl ohne als auch mit zurückliegendem Herzinfarkt, bezüglich Mortalität und Morbidität, verglichen mit anderen Thrombozytenaggregationshemmern mindestens gleichwertig ist. Die Dosierung ist abhängig vom kardiovaskulären Risikoprofil des Patienten.[4] Bei Patienten mit hohem kardiovaskulären Risiko oder mit stabiler Angina pectoris sinkt unter ASS-Medikation die Letalität. Eine Indikation für Clopidogrel besteht bei Kontraindikationen oder ASS-Unverträglichkeit.[19]
Cholesterinsenkende Arzneimittel
[Bearbeiten | Quelltext bearbeiten]Medikamente aus der Gruppe der Statine hemmen die HMG-CoA-Reduktase, ein Enzym im Cholesterinstoffwechsel, und damit die körpereigene Cholesterinproduktion. Man unterstellt ihnen auch eine gewisse Stabilisierung von atheromatösen Plaques.
Vitamin D
[Bearbeiten | Quelltext bearbeiten]In der Health Professionals Follow-up Study war das Risiko für einen Myokardinfarkt bei Männern mit Vitamin-D-Mangel (Plasma-25-OH-Vitamin D von höchstens 15 ng / mL) um den Faktor 2,4 höher als bei Gleichaltrigen mit ausreichender Vitamin-D-Versorgung (Plasma-25(OH) D von mindestens 30 ng / mL). Selbst unter Berücksichtigung von KHK-Risikofaktoren wie positive Familienanamnese, Hypertonie, ungünstiges Lipidprofil und Übergewicht war das Myokardinfarkt-Risiko bei niedrigen Vitamin-D-Werten immer noch verdoppelt.[35] Erhoben wurden diese Studiendaten bei 18.225 Männern im Alter zwischen 40 und 75 Jahren, deren Blut untersucht worden war. Zu Studienbeginn hatte noch keiner der Männer eine KHK. Innerhalb der nächsten zehn Jahre hatten 454 Studienteilnehmer einen nichttödlichen Herzinfarkt oder ein tödliches KHK-Ereignis erlitten. In einer anderen Studie mit mehr als 3000 Männern und Frauen waren bei denen mit niedrigen Vitamin-D-Werten (median 7,7 und 13,3 ng/ml) innerhalb von 7,7 Jahren die kardiovaskuläre sowie auch die Gesamtsterberate verdoppelt.[36] Als Vergleich dienten Teilnehmer mit guter Vitamin-D-Versorgung (median 28,4 ng/ml).[37]
Life’s Simple 7
[Bearbeiten | Quelltext bearbeiten]Die American Heart Association hat 7 Grundregeln erstellt, die nicht nur Herz-Kreislauf-Erkrankungen, sondern auch Krebs vorbeugen sollten.[38]
- Körperlich aktiv sein
- ein gesundes Gewicht halten
- gesund essen
- einen gesunden Cholesterinspiegel halten
- Blutdruck niedrig halten
- normalen Blutzucker halten
- nicht rauchen
Behandlung
[Bearbeiten | Quelltext bearbeiten]Bei einer Erkrankung der kleinen Gefäße ist bisher außer der medikamentösen Therapie keine invasive Behandlungsmethode erfolgversprechend. Bei Erkrankung der großen Gefäße besteht die Möglichkeit der Aufdehnung mittels eines Ballonkatheters oder die Durchführung einer Bypassoperation. Für eine einheitliche Qualität bei der Therapie bieten die gesetzlichen Krankenkassen seit Mitte 2004 Disease-Management-Programme (DMP) an.
Medikamentöse Therapie
[Bearbeiten | Quelltext bearbeiten]Nitrate
[Bearbeiten | Quelltext bearbeiten]Nitrate führen durch Verminderung des Gefäßwiderstands zu einer Senkung der Vorlast und der Nachlast des Herzens. Dadurch sinkt der Sauerstoffverbrauch des Herzmuskels. Es gibt sowohl kurzwirksame als auch langwirksame Nitratpräparate. Kurzwirksame Nitrate werden zur symptomatischen Behandlung einer akuten Angina pectoris eingesetzt. Die Wirkung tritt bei sublingualer oder kutaner Applikation innerhalb weniger Minuten ein, so dass sie sich zur Behandlung insbesondere im akuten AP-Anfall eignen. Kurz- und langwirksame Nitrate haben keinen Einfluss auf die Prognose der chronischen KHK.[4] Für eine Dauertherapie werden langwirksame Präparate eingesetzt, die allerdings aufgrund einer schnellen Toleranzentwicklung nur eingeschränkt geeignet sind. Durch spezifische Therapieschemata und mehrstündige Therapiepausen ist bei guter Compliance des Patienten eine Dauertherapie mit Nitraten möglich.[39]
Betablocker
[Bearbeiten | Quelltext bearbeiten]Betablocker senken die Herzfrequenz sowohl in Ruhe als auch bei körperlicher Belastung (negative Chronotropie). Darüber hinaus wirken sie negativ inotrop durch Senkung der Kontraktilität (Kontraktionskraft) des Herzens. Beide Mechanismen führen dazu, dass der Sauerstoffbedarf der Herzmuskulatur und der arterielle Blutdruck sinken. Betablocker können damit, wie Nitrate und Calciumkanalblocker, gegen pektanginöse Beschwerden eingesetzt werden. Im Gegensatz zu den beiden anderen Medikamenten senken sie zusätzlich das Risiko für das Auftreten kardiovaskulärer Ereignisse. Betablocker sind das Arzneimittel der ersten Wahl bei stabiler Angina pectoris. Wie bei allen Medikamenten müssen die Kontraindikationen beachtet werden. Hier sind dies insbesondere Asthma bronchiale sowie verschiedene Herzrhythmusstörungen, wie beispielsweise AV-Blockierungen.[19]
Calciumkanalblocker
[Bearbeiten | Quelltext bearbeiten]Die Calciumantagonisten (eigentlich Calciumkanalmodulatoren) vermindern den Calcium-Einstrom in die Muskelzelle und hemmen die elektromechanische Kopplung. Dies führt zur Abnahme der Kontraktilität und des Sauerstoffverbrauchs des Herzens.
Trapidil
[Bearbeiten | Quelltext bearbeiten]Das seit 1992 in Deutschland zugelassene Mittel Trapidil ist zur Behandlung der KHK insbesondere bei Patienten mit einer Unverträglichkeit gegenüber den standardmäßig eingesetzten Nitraten geeignet.
Revaskularisationstherapie
[Bearbeiten | Quelltext bearbeiten]Perkutane transluminale Koronarangioplastie und Stentimplantation
[Bearbeiten | Quelltext bearbeiten]Als diagnostische und therapeutische Maßnahme gilt die Darstellung der Herzkranzgefäße mittels Koronarangiographie als Goldstandard in der Diagnostik. In derselben Sitzung ist es möglich, signifikante Engstellen durch eine Ballondilatation (Perkutane transluminale coronare Angioplastie, PTCA), ggf. kombiniert mit der Implantation eines Stents aufzudehnen.
Bypassoperation
[Bearbeiten | Quelltext bearbeiten]Bei einer Bypassoperation werden mittels Gefäßtransplantation von vorher an den Extremitäten entnommenen Venen oder Arterien die Engstellen überbrückt, zusätzlich wird häufig eine innerhalb des Brustkorbs verlaufende Arterie, die linke A. thoracica interna (LIMA) (selten auch die rechte) mit einem Ast der Koronararterien jenseits der Engstelle verbunden. Im Regelfall wird die Operation im Herzstillstand mit Herz-Lungen-Maschine durchgeführt; unter bestimmten Voraussetzungen sind aber eine Operation am schlagenden Herzen (sog. off pump bypass) oder minimal-invasive Techniken möglich.
Indikationen
[Bearbeiten | Quelltext bearbeiten]Nach den Empfehlungen der nationalen Versorgungsleitlinie besteht in folgenden Fällen die Indikation zur Durchführung einer Revaskularisationstherapie:[4]
- Bei einer KHK, deren Symptome mit alleiniger medikamentöser Therapie nicht in den Griff zu bekommen sind, kann die Revaskularisationstherapie eine deutliche Linderung der AP-Symptomatik herbeiführen. Aufgrund der geringeren Invasivität ist die perkutane transluminale Koronarangioplastie die Therapie der ersten Wahl.
- Bei mittelgradigen Stenosen (> 50 Prozent) des Hauptstamms der linken Koronararterie ist die Bypassoperation die Therapie der ersten Wahl, da sie hinsichtlich Verbesserung der Lebensqualität und der Prognose sowie des Eintretens akuter KHK-Manifestationen der perkutanen transluminalen Koronarangioplastie überlegen ist. Bei Inoperabilität oder bei Ablehnung des Patienten wird dagegen die Durchführung einer perkutanen transluminalen Koronarangioplastie empfohlen. Inoperabilität kann aufgrund schwerer Begleiterkrankungen oder einer diffusen Arteriosklerose bestehen.
- Hochgradige proximale Stenosen (> 70 Prozent) des Ramus interventricularis anterior (RIVA-Stenose) sollten unabhängig von der Symptomatik einer Revaskularisationstherapie zugeführt werden, wobei die perkutane transluminale Koronarangioplastie und die Bypassoperation hinsichtlich Verbesserung der Prognose als gleichwertig angesehen werden. Besteht darüber hinaus eine deutliche Reduzierung der Auswurfleistung des linken Herzens, entstehen nach gegenwärtiger Studienlage Vorteile für die Bypasschirurgie.
- Bei einer Mehrgefäßerkrankung kann die AP-Symptomatik durch Revaskularisationstherapie unabhängig von der Methode deutlich reduziert werden. Eine Prognoseverbesserung im Vergleich zur alleinigen medikamentösen Therapie ist nicht belegt.
- Bei Dreigefäßerkrankung mit hochgradigen proximalen Stenosen wird die Bypasschirurgie als Therapie der ersten Wahl empfohlen. Beide Revaskularisationsmethoden verbessern die Lebensqualität (Reduktion der Symptome) und führen wahrscheinlich auch zu einer Verbesserung der Prognose.
Geschichte
[Bearbeiten | Quelltext bearbeiten]An Arteriosklerose beziehungsweise der koronaren Herzkrankheit litten bereits die Menschen im antiken Ägypten, wie man durch Untersuchungen an Mumien im 20. und 21. Jahrhundert feststellen konnte.
Unter anderem Caspar Bauhin (1592) sowie, wie Théophile Bonet 1679 bestätigte, William Harvey (1618) und Charles Drelincourt fanden steinartige Strukturen bzw. (wie Lorenzo Bellini, Adam Christian Thebesius und Johann Friedrich Crell) „Verknöcherungen“ in den Herzkrankgefäßen.[40] 1749 wurde die bei der Autopsie eines herzkranken Franziskaners gefundene Arterienverkalkung in Form von Ästchen, vergleichbar denen einen Korallenstock bildenden, verknöcherten Kranzarterien von Jean-Baptiste Sénac beschrieben.[41] Giovanni Battista Morgagni publizierte als exakte und anschauliche Beschreibung 1761 in De sedibus et causis morborum seine 1743 bei einer Sektion vorgefundene und Studenten demonstrierte, die Blutstrombahn einer linken Koronararterie einengende Verknöcherung am Herzen. Die Ursachen und die Bedeutung dieser als Bildung von „Knochen“, „Knorpel“, Klümpchen, steinartige Substanz, „Stein“ usw., auch (bei Johann Nikolaus Pechlin) als tuffsteinartige (den Tophi bei Gicht ähnelnde) Substanz, bezeichneten Gefäßveränderungen am Herzen, etwa einen Zusammenhang mit der Angina pectoris, wurde jedoch auch von Morgagni noch nicht erkannt, doch wie Albrecht von Haller widersprach er der von Meckel dem Jüngeren oder Boerhaave vertretenen Ansicht, dass es sich bei der im Gefäßsystem alter Menschen vorkommenden kalkigen Materie, die zu Verengerung von Gefäßen führt, um echten Knochen handle.[42]
Die erste und sehr genaue Beschreibung der AP-Symptomatik geht auf den englischen Mediziner William Heberden im Jahre 1768 zurück.[43] Dass ein Zusammenhang zwischen der Angina pectoris und der Arteriosklerose von Koronararterien besteht, erkannte Heberden nicht. Zu den ersten Medizinern, die einen Zusammenhang zwischen der Verhärtung der Herzkranzgefäße und der Angina pectoris sahen gehören die englischen Mediziner John Wall (1708–1776), der, nachdem er auf eine Veröffentlichung Heberdens gestoßen war, in einem Brief vom 17. November 1772 diesen formulierte, und John Fothergill. Dieser Zusammenhang wurde von Edward Jenner vermutet und 1799 von Caleb Hillier Parry, dem Jenner seine Ansicht und Beobachtungen mitgeteilt hat, beschrieben, wobei Parry die Unterversorgung des so erkrankten Herzens bzw. Herzmuskels mit Blut wie später etwa auch der Chirurg und Anatom Allan Burns in Observations on some of the most frequent and important diseases of the heart auch im Sinne einer Ischämie verstand. Zu den heutigen Kenntnissen makroskopischer und mikroskopischer Gefäßveränderungen durch Arteriosklerose haben Antonio Scarpa (1804) und Jean-Frédéric Lobstein (1833) mit ihren Arbeiten einen großen Beitrag geleistet. In seiner Abhandlung Von der Verengung und Schliessung der Pulsadern in Krankheiten publizierte Friedrich Tiedemann 1843 zahlreiche Beobachtungen zur Verengung der Koronarien und daraus resultierenden Veränderungen am Herzmuskel. Tierexperimentell zeigte der königliche Leibarzt und Chirurg John Erichsen 1842 an künstlich beatmeten Hunden und Kaninchen, bei denen er die „Kranz-Pulsadern“ abband, dass die Koronararterien zur Funktion des Herzens unentbehrlich sind.[44] Welche EKG-Veränderungen im Rahmen einer chronischen KHK entstehen können, wurde 1923 von Wean sowie 1957 von Himbert und Jean Lenègre erkannt.[45]
Koronarinsuffizienz, die sich durch Angina pectoris äußert, kann durch Revaskularisation des Herzmuskels behandelt werden. Chirurgische Maßnahmen zur Revaskularisation wurden erstmals in der ersten Hälfte des 20. Jahrhunderts durchgeführt. Zuvor standen lediglich symptomatische Therapien zur Verfügung. Methoden der Myokardrevaskularisation waren unter anderem das Aufnähen von körpereigenen Geweben wie Fettgewebe, Muskelgewebe, Netz (Omentum majus bei der Kardioomentopexie wie sie 1936 L. O’Shaughnessy beschrieben hat), Gewebe von Lunge und Darm. Eine entscheidende Bedeutung für die Revaskularisationschirurgie bzw. Koronararterienchirurgie[46] erlangte die Einführung der Herz-Lungen-Maschine in der zweiten Hälfte des 20. Jahrhunderts.[47]
KHK bei Tieren
[Bearbeiten | Quelltext bearbeiten]Bei Tieren haben arteriosklerotische Veränderungen der Koronargefäße beziehungsweise eine chronische KHK nur eine sehr geringe klinische Bedeutung; insbesondere für Großtiere fehlen außerdem entsprechende Dokumentationen. Bei Kleintieren gibt es einige Studien zur Arteriosklerose und deren Manifestation Myokardinfarkt. Im Zeitraum von 1970 bis 1983 wurde bei 21 Hunden im Rahmen einer Autopsie eine systemische Arteriosklerose diagnostiziert. Darüber hinaus konnten bei histologischen Untersuchungen Infarktareale in der Herzmuskulatur festgestellt werden.[48] Bei anderen Studien mit Hunden konnten ähnliche Veränderungen festgestellt werden, die unter anderem auch an den Koronararterien zu finden waren.[49][50] Darüber hinaus kommen systemische Veränderungen der Gefäße bei Katzen vor, deren Bedeutung für die Koronargefäße derzeit aber noch unklar ist.[51]
Das Herz des Hausschweins ähnelt in seinem anatomischen Aufbau und seiner Physiologie dem des Menschen. Komplexe Krankheitsbilder einer Arteriosklerose treten hier schon im Alter von etwa vier bis acht Jahren auf, was infolge der Haltung als Nutztier allerdings meist weit über der normalen Lebensspanne der Tiere liegt. Im Erkrankungsfall kommt es zu mit dem Menschen vergleichbaren ischämischen Veränderungen und Schäden bereits in relativ kurzen Zeiträumen. Die Herzkranzgefäße neigen außerdem in noch geringerem Umfang als die des Menschen zur Ausbildung von Kollateralgefäßen, was eine klinische Lokalisation von Infarktgebieten erleichtert. Durch diese Eigenschaften werden Schweineherzen als Modelle zur Untersuchung der menschlichen chronischen myokardialen Ischämie verwendet. Ferner kommen hierfür Ratten-, Kaninchen-, Hunde- und Primatenherzen zum Einsatz.[52]
Literatur
[Bearbeiten | Quelltext bearbeiten]- Chronische KHK. – Nationale Versorgungsleitlinie der Bundesärztekammer (BÄK), der Kassenärztlichen Bundesvereinigung (KBV) und der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) (Stand April 2019)
- Hans H. Lauer: Geschichtliches zur Koronarsklerose. BYK Gulden, Konstanz 1971 (Aus dem Institut für Geschichte der Medizin der Universität Heidelberg).
- J. O. Leibowitz: The history of coronary heart disease. Wellcome Institut of the History of Medicine, London 1970.
- Martin Ruß, Jochen Cremer u. a.: Differenzialtherapie der chronischen koronaren Herzkrankheit: Wann medikamentöse Therapie, wann perkutane Koronarintervention, wann aortokoronare Bypassoperation? In: Dtsch Arztebl Int. Band 106, Nummer 15, 2009, S. 253–261. doi:10.3238/arztebl.2009.0253
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Herz in Gefahr? – Ursachen, Prävention, Therapie – Ergebnisse der Herzkreislaufforschung. (PDF; 3,8 MB) Bundesministeriums für Bildung und Forschung, 2006; Broschüre
- Rechner für Herzinfarktrisiko der Deutschen Herzstiftung
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f M. Classen, V. Diehl, K. Kochsiek: Innere Medizin. 5. Auflage. Urban & Fischer-Verlag, München 2006, ISBN 3-437-44405-0.
- ↑ a b c d e f g H. Renz-Polster u. a.: Basislehrbuch Innere Medizin. 3. Auflage. Urban & Fischer-Verlag, München 2004, ISBN 3-437-41052-0.
- ↑ Todesursachenstatistik: Gesundheitsberichterstattung des Bundes
- ↑ a b c d e f g h i Chronische KHK, Version 1.8, April 2008. (PDF) Nationale Versorgungsleitlinie der Bundesärztekammer
- ↑ Nationale VersorgungsLeitlinie (NVL) Chronische KHK, Version 6, 2022. Hrsg.: Bundesärztekammer, Kassenärztliche Bundesvereinigung, Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF), 15. September 2022, (Dokumente der Version 6.0: Langfassung, Empfehlungsübersicht/Kurzfassung, weitere Formate). (PDF 2,8 MB). Abgerufen am 17. Mai 2024
- ↑ a b Manfred Dietel u. a. (Hrsg.): Harrisons Innere Medizin. Dt. Ausgabe der 15. Auflage. ABW Wissenschaftsverlag, Berlin 2003, ISBN 3-936072-10-8.
- ↑ Bethesda: NHLBI morbidity and mortality chartbook. National Heart, Lung, and Blood Institute, Mai 2002. nhlbi.nih.gov
- ↑ Europa in Zahlen – Eurostat-Jahrbuch 2006-07. (PDF; 12,1 MB)
- ↑ Todesursachen in Deutschland. Statistisches Bundesamt
- ↑ R. Ross: Atherosclerosis–an inflammatory disease. In: The New England Journal of Medicine. Band 340, Nummer 2, Januar 1999, S. 115–126, ISSN 0028-4793. doi:10.1056/NEJM199901143400207. PMID 9887164. (Review).
- ↑ J. Stamler u. a.: Is relationship between serum cholesterol and risk of premature death from coronary heart disease continuous and graded? Findings in 356,222 primary screenees of the multiple risk factor intervention trial. (MRFIT). In: JAMA. 256, 1986, S. 2823–2828.
- ↑ W. Verschuren u. a.: Serum total cholesterol and long-term coronary heart disease mortality in different cultures. Twenty-five-year follow-up of the seven countries study. In: JAMA. 274, 1995, S. 131–136.
- ↑ Koronare Herzkrankheit: Entzündungsmarker ebenso verantwortlich wie Bluthochdruck und LDL-Cholesterin. In: The Lancet. 30. April 2010.
- ↑ The Lp-PLA2 Studies Collaboration. Lipoprotein-associated phospholipase A2 and risk of coronary disease, stroke, and mortality: collaborative analysis of 32 prospective studies. In: The Lancet. 375, 2010, S. 1536. doi:10.1016/S0140-6736(10)60319-4
- ↑ A. Rieder: Epidemiologie der Herz-Kreislauf-Erkrankungen. (PDF; 796 kB) In: Journal für Kardiologie. 11 (Supplementum D), 2004, S. 3–4.
- ↑ Sarah C. Darby, Marianne Ewertz, Paul McGale, Anna M. Bennet, Ulla Blom-Goldman, Dorthe Brønnum, Candace Correa, David Cutter, Giovanna Gagliardi, Bruna Gigante, Maj-Britt Jensen, Andrew Nisbet, Richard Peto, Kazem Rahimi, Carolyn Taylor, Per Hall: Risk of Ischemic Heart Disease in Women after Radiotherapy for Breast Cancer. In: New England Journal of Medicine. Band 368, Ausgabe 11, 14. März 2013, S. 987–998, doi:10.1056/NEJMoa1209825.
- ↑ Nadine Eckert, Kathrin Gießelmann: Chronisches Koronarsyndrom. Zu wenige Ischämietests. In: Deutsches Ärzteblatt. Band 116, Heft 51–52, 23. Dezember 2019, S. B 1971–1973.
- ↑ Nadine Eckert, Kathrin Gießelmann: Chronisches Koronarsyndrom. Zu wenige Ischämietests. In: Deutsches Ärzteblatt. Band 116, Heft 51–52, 23. Dezember 2019, S. B 1971–1973, hier: S. B 1972.
- ↑ a b c d R. Dietz u. a.: Leitlinie zur Diagnose und Behandlung der chronischen koronaren Herzerkrankung der deutschen Gesellschaft für Kardiologie (DGK). In: Zeitschrift für Kardiologie. 92, 2003, S. 501–521, leitlinien.dgk.org (PDF)
- ↑ a b c C. A. Daly u. a.: Predicting prognosis in stable angina-results from the Euro heart survey of stable angina: prospective observational study. Online-Version. In: BMJ. 332 (7536), 2006, S. 262–267.
- ↑ Eur J Echocardiogr. 9(4), Jul 2008, S. 415–437.
- ↑ Büll, Schicha, Biersack, Knapp, Reiners, Schober: Nuklearmedizin. Stuttgart 2001, ISBN 3-13-128123-5, S. 213f.
- ↑ M. A. Pantaleo, A. Mandrioli u. a.: Development of coronary artery stenosis in a patient with metastatic renal cell carcinoma treated with sorafenib. (PDF; 287 kB) In: BMC Cancer. 12, 2012, S. 231 doi:10.1186/1471-2407-12-231 (Open Access)
- ↑ Kauffmann u. a.: Radiologie, 3. Auflage. Urban & Fischer, München/ Jena 2006, ISBN 3-437-44415-8.
- ↑ AS Agatston, WR Janowitz, FJ Hildner, NR Zusmer, M Viamonte, R Detrano: Quantification of coronary artery calcium using ultrafast computed tomography. In: J Am Coll Cardiol. Band 15, Nr. 4, 1990, S. 827–832, PMID 2407762.
- ↑ B. Hermanson u. a.: Beneficial six-year outcome of smoking cessation in older men and women with coronary artery disease. Results from the CASS registry. In: N Engl J Med. 319, 1988, S. 1365–1369
- ↑ L. Ignarro, M. Balestrieri, C. Napoli: Nutrition, physical activity, and cardiovascular disease: An update. In: Cardiovascular Research. 73, 2007, S. 326, doi:10.1016/j.cardiores.2006.06.030.
- ↑ K. D. Kolenda: Sekundärprävention der koronaren Herzkrankheit: Effizienz nachweisbar. (PDF) In: Deutsches Ärzteblatt. 102/2005, S. A1889.
- ↑ K. Wilson, N. Gibson, N. Willan, D. Cook: Effect of smoking cessation on mortality after myocardial infarction. In: Arch Int Med. 160, 2000, S. 939–944.
- ↑ a b L. M. Morrison: Diet in coronary atherosclerosis. In: JAMA. 173, 1960, S. 884–888.
- ↑ M. De Longeril, P. Salen, J. L. Martin, J. Monjaud, J. Delaye, N. Mamelle: Mediterranean diet, traditional risk factors, and the rate of cardiovascular complications after myocardial infarction. Final report of the Lyon Diet Heart Study. In: Circulation. 99, 1999, S. 779–785. PMID 9989963
- ↑ G. T. O’Connor, I. Buring, S. Yusuf u. a.: An overview of randomised trials of rehabilitation with exercise after myocardial infarction. In: Circulation. 80, 1989, S. 234–244.
- ↑ J. A. Blumenthal, W. Jiang, M. A. Babyatz u. a.: Stress management and exercise training in cardiac patients with myocardial ischemia. In: Arch Intern Med. 157, 1997, S. 2213–2223.
- ↑ Walter Willet: Nutritional Epidemiology. In: Oxford University Press. ISBN 978-0-19-997944-8, S. 30–35, doi:10.1093/acprof:oso/9780199754038.002.0005 (oup.com [abgerufen am 28. Januar 2024]).
- ↑ E. Giovannucci, Y. Liu u. a.: 25-hydroxyvitamin D and risk of myocardial infarction in men: a prospective study. In: Archives of internal medicine. Band 168, Nummer 11, Juni 2008, S. 1174–1180, ISSN 1538-3679. doi:10.1001/archinte.168.11.1174. PMID 18541825.
- ↑ H. Dobnig, S. Pilz u. a.: Independent association of low serum 25-hydroxyvitamin d and 1,25-dihydroxyvitamin d levels with all-cause and cardiovascular mortality. In: Archives of internal medicine. Band 168, Nummer 12, Juni 2008, S. 1340–1349, ISSN 1538-3679. doi:10.1001/archinte.168.12.1340. PMID 18574092.
- ↑ Zitiert nach Ärzte-Zeitung. 9. Juli 2008, S. 1.
- ↑ L. J. Rasmussen-Torvik, C. M. Shay, J. G. Abramson, C. A. Friedrich, J. A. Nettleton, A. E. Prizment, A. R. Folsom: Ideal Cardiovascular Health is Inversely Associated with Incident Cancer: The Atherosclerosis Risk in Communities Study. In: Circulation. doi:10.1161/CIRCULATIONAHA.112.001183.
- ↑ H. P. Wolff, T. R. Weihrauch: Internistische Therapie 2004–2005. 15. Auflage. Urban & Fischer-Verlag, München 2004, ISBN 3-437-21802-6.
- ↑ Hans H. Lauer: Geschichtliches zur Koronarsklerose. BYK Gulden, Konstanz 1971 (Aus dem Institut für Geschichte der Medizin der Universität Heidelberg), S. 6 f.
- ↑ J. Schmitt, M. Beeres: Geschichte der Medizintechnologie, Teil 3. In: MTDialog. Dez. 2004, S. 72–75. bvmed.de ( vom 31. Juli 2013 im Internet Archive)
- ↑ Hans H. Lauer: Geschichtliches zur Koronarsklerose. 1971. S. 8 f., 13 und 20 f.
- ↑ Martin Schrenk: Aus der Geschichte der Kardiopathologie: Die Heberden’sche Angina pectoris (1768). Mannheim/ Frankfurt am Main 1969.
- ↑ Hans H. Lauer: Geschichtliches zur Koronarsklerose. 1971, S. 20–31.
- ↑ R. Rullière: Geschichte der Kardiologie im 19. und 20. Jahrhundert. In: R. Toellner: Illustrierte Geschichte der Medizin. Band 3. Andreas Verlag, Salzburg 1992, ISBN 3-86070-204-1.
- ↑ Vgl. etwa Åke Senning: Coronararterienchirurgie. Pallative und direkte Verfahren. In: Chir. Band 42, 1971, S. 213 ff.
- ↑ Friedrich Wilhelm Hehrlein: Herz und große Gefäße. In: Franz X. Sailer, F. W. Gierhake (Hrsg.): Chirurgie historisch gesehen: Anfang – Entwicklung – Differenzierung. Dustri-Verlag, Deisenhofen bei München 1973, ISBN 3-87185-021-7, S. 164–185, hier: S. 176–178.
- ↑ S. Liu u. a.: Clinical and pathologic findings in dogs with atherosclerosis: 21 cases (1970–1983) In: J Am Vet Med Assoc., 189(2), 15. Jul 1986, S. 227–232. PMID 3744984
- ↑ D. Kelly: Arteriosclerosis of coronary arteries in Labradors with congestive heart failure. In: J Small Anim Pract., 33, 1992, S. 437.
- ↑ D. Detweiler: Spontaneous and induced arterial disease in the dog: pathology and pathogenesis. In: Toxicol Pathol., 17(1 Pt 2), 1989, S. 94–108. PMID 2665038
- ↑ V. Lucke: Renal disease in the domestic cat. In: J Pathol Bacteriol., 95(1), Jan 1968, S. 67–91. PMID 5689371
- ↑ C. Nimz: Pathologisch-anatomische und immunhistologische Untersuchungen des ischämischen Schweinemyokards. Vet.-med. Diss., München 2004, S. 1–10 uni-muenchen.de