Houben-Hoesch-Reaktion
Die Houben-Hoesch-Reaktion, auch bekannt als die Hoesch-Synthese, Hoesch-Reaktion, Houben-Hoesch-Acylierung oder Houben-Hoesch-Synthese, ist eine Namensreaktion der organischen Chemie. Die Reaktion wurde nach Kurt Hoesch (1882–1932), der sie 1915[1] veröffentlichte, und nach Josef Houben (1875–1940)[2] benannt (Veröffentlichung 1926).[3] Mit Hilfe der Reaktion können elektronenreiche Aromaten acyliert werden.
Übersichtsreaktion
[Bearbeiten | Quelltext bearbeiten]Elektronenreiche Aromaten, wie zum Beispiel Phenole mit mehreren Hydroxygruppen oder entsprechende Ether (hier beispielhaft mit Resorcin dargestellt), können in Gegenwart von Chlorwasserstoff und einer Lewis-Säure (wie AlCl3 oder ZnCl2) mit organischen Nitrilen [R = Organylgruppe (z. B. Alkylgruppe, Arylgruppe)] acyliert werden:[4]
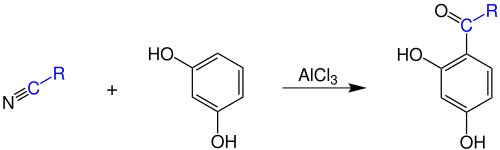
Mechanismus
[Bearbeiten | Quelltext bearbeiten]Der Mechanismus wird am Beispiel der Reaktion zwischen 1,3-Dihydroxybenzol (Resorcin) und einem organischen Nitril (R = Alkylgruppe, Arylgruppe) gezeigt. Als Lewis-Säure wird z. B. Aluminiumchlorid (AlCl3) genutzt:[5]
Zunächst bildet das Nitril 1 mit Aluminiumchlorid einen Komplex 2 und mit einem weiteren Aluminiumchlorid den Komplex 3. Dieser Komplex reagiert mit Resorcin im Zuge einer elektrophilen aromatischen Substitution über den Zwischenschritt 4 zu Molekül 5, wobei AlCl3 das Molekül verlässt. Zu dem Molekül 4 können noch weitere mesomere Grenzstrukturen gezeichnet werden, die den Grenzstrukturen im Verlaufe einer Polysubstitution entsprechen. Die Reaktion mit Wasser führt zu einer erneuten Abspaltung der Lewis-Säure Aluminiumchlorid. Das Molekül 6 reagiert schließlich mit Chlorwasserstoff zum Keton 7, im Beispiel ein acyliertes Resorcin.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Kurt Hoesch: Eine neue Synthese aromatischer Ketone. I. Darstellung einiger Phenol-ketone. In: Berichte der deutschen chemischen Gesellschaft. Band 48, Nr. 1, 1915, S. 1122–1133, doi:10.1002/cber.191504801156.
- ↑ Grete Ronge: Houben, Josef. In: Neue Deutsche Biographie (NDB). Band 9, Duncker & Humblot, Berlin 1972, ISBN 3-428-00190-7, S. 659 f. (Digitalisat).
- ↑ J. Houben: Über die Kern-Kondensation von Phenolen und Phenol-äthern mit Nitrilen zu Phenol- und Phenol-äther-Ketimiden und -Ketonen (I.). In: Berichte der deutschen chemischen Gesellschaft (A and B Series). Band 59, Nr. 11, 1926, S. 2878–2891, doi:10.1002/cber.19260591135.
- ↑ K. Schwetlick et al.: Organikum. 23. Auflage, Wiley-VCH, Weinheim 2009, ISBN 978-3-527-32292-3, S. 385.
- ↑ Z. Wang (Hrsg.): Comprehensive Organic Name Reactions and Reagents, 3 Volume Set. John Wiley & Sons, Hoboken, New Jersey 2009, ISBN 978-0-471-70450-8, S. 1496.
