Karpaltunnelsyndrom

| Klassifikation nach ICD-10 | |
|---|---|
| G56.0 | Karpaltunnel-Syndrom |
| ICD-10 online (WHO-Version 2019) | |
Das Karpaltunnelsyndrom (KTS, Synonyme unter anderem: Carpaltunnelsyndrom, CTS, Medianuskompressionssyndrom, Brachialgia paraesthetica nocturna) ist ein sehr häufiges Nervenkompressionssyndrom. Der durch den Karpaltunnel am Handgelenk verlaufende Nervus medianus wird an dieser Engstelle durch Druck geschädigt, wodurch es vor allem nachts zu Missempfindungen und Schmerzen, insbesondere im Daumen, Zeige- und Mittelfinger kommt. Im Verlauf ist auch eine Abnahme des Tastgefühls sowie eine Störung der vom Nervus medianus versorgten Muskulatur mit Lähmungserscheinungen und Muskelschwund (Atrophie) möglich. Die Verdachtsdiagnose wird mittels einer elektroneurografischen Untersuchung gesichert. Die Behandlung kann konservativ, insbesondere durch das Tragen von Handgelenksschienen, und operativ erfolgen.
Anatomie
[Bearbeiten | Quelltext bearbeiten]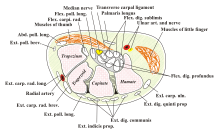

Der Karpaltunnel ist eine tunnelartige, bindegewebig fest umschlossene Röhre vom Unterarm zur Hand auf der Palmarseite (Handflächenseite) des Handgelenks. Der „Boden“ und die Seitenwände des Tunnels werden von den Handwurzelknochen gebildet (einem Teil des knöchernen Handskeletts), während das „Dach“ von einem breiten Band, dem Retinaculum flexorum, gebildet wird, das sich quer zwischen den Handwurzelknochen ausspannt. Durch den Tunnel verläuft – zusammen mit neun Beugesehnen (je vier des oberflächlichen und tiefen Fingerbeugers sowie die des langen Daumenbeugers) – der Nervus medianus, der unter anderem die Bewegungen der Finger und des Daumens steuert, Empfindungen rückmeldet und vegetative Funktionen an der Hand erfüllt.
Meist am distalen Ausgang des Karpaltunnels gibt der Nervus medianus zum Daumenballen hin einen kleinen motorischen Ramus palmaris ab. Allerdings gibt es zahlreiche Varianten mit proximalerem Abgang, oder direkt durch das Retinakulum. Auch der Mediannerv kann manchmal zweigeteilt sein oder sogar durch getrennte Retinakulumsepten laufen.
Ursachen
[Bearbeiten | Quelltext bearbeiten]Durch eine Einengung des Karpaltunnels wird der Nerv geschädigt. Zumeist entsteht das Karpaltunnelsyndrom bei vorbestehender relativer anatomischer Enge, wenn eine Gewebeschwellung durch eine mechanische Überlastung, eine Entzündung oder durch Allgemeinerkrankungen hinzukommt.
Zu einem Karpaltunnelsyndrom disponieren
- konstitutionelle Enge des Karpalkanals
- Arbeitshand meist stärker betroffen (beidseitiges Auftreten ist aber häufig)
- manuelle Arbeit
- Schwangerschaft
- Nierenschädigungen
- Handgelenk- oder distale Unterarmfrakturen und Narbenbildungen
- Diabetes mellitus
- Sehnenscheidenentzündung der Fingerbeuger
- verlängertes Muskelprofil der langen Fingerbeugemuskeln
- Schilddrüsenunterfunktion (Hypothyreose)
- chronische Polyarthritis
- Akromegalie
- Infektionen im Handbereich
- erhöhter venöser Druck, etwa am Shuntarm bei Dialysepatienten
- Alkoholmissbrauch
- Amyloidose
- Sklerodermie
- Fluorchinolone[1]
Frauen sind etwa dreimal häufiger davon betroffen als Männer.
Bei Kindern ist ein Karpaltunnelsyndrom praktisch unbekannt, es tritt jedoch bei Mukopolysaccharidosen vom Typ I, II und VI häufig bereits im Kindesalter auf. Typischerweise bestehen keine Schmerzen, und oft ist das Karpaltunnelsyndrom mit einem Triggerfinger assoziiert.[2]
Selten können auch Fehlbildungen des Handgelenkes wie die Madelung-Deformität ein Karpaltunnelsyndrom bereits in der Kindheit auslösen.[3]
Es gibt auch familiäre Formen:
- CTS1 mit Mutationen im TTR-Gen im Chromosom 18 an Genort q12.1 mit autosomal-dominantem Erbgang.[4]
- CTS2 mit Mutationen im COMP-Gen im Chromosom 19 an p13.11, gleichfalls autosomal-dominant.[5]
Symptome
[Bearbeiten | Quelltext bearbeiten]Typisches Erstsymptom sind Schmerzen oder Missempfindungen, die von der Hand in den Daumen, Zeigefinger und Mittelfinger einstrahlen können und anfangs oftmals nachts auftreten –, daher der klassische Name Brachialgia Nocturna. Später treten die Beschwerden auch zunehmend tagsüber auf, im fortgeschrittenen Stadium kann es zu einem Muskelschwund vor allem im Bereich des Daumenballens, Schwäche beim Greifen und zu einer Minderung des Tastgefühls (Taubheitsgefühl) kommen. Nicht selten kommt es auch zu vegetativen Störungen, zum Beispiel zu trophischen und vaskulären Störungen.
Wenn die Nervenschädigung fortschreitet, kommt es zu einer Zunahme der Schwäche typischer Handmuskeln und Minderung des Tastgefühls in einem umschriebenen Hautbereich. Insbesondere durch Funktionsminderung des Daumens kommt es zu einer Behinderung. Andererseits lassen aber in diesem Stadium die Schmerzen nach, da auch die Schmerzfasern zerstört werden.
Wenn die Feinmotorik und die Sensibilität vermindert sind, betrifft dies in der Regel Daumen, Zeigefinger und Mittelfinger entsprechend dem Versorgungsgebiet des Nervus medianus mit einer Hyp- und Parästhesie der drei Fingerkuppen und Atrophie der seitlichen (lateralen) Daumenballenmuskulatur im fortgeschrittenen Stadium.
Oft ist der Karpalkanal (Canalis carpi) gegen Druck und leichtes Beklopfen empfindlich (Hoffmann-Tinel-Zeichen). Bei Überstreckung (oder starker Beugung) des Handgelenks kommt es zu den typischen Missempfindungen im sensiblen Versorgungsgebiet des Nervus medianus (Phalen-Zeichen). Der Medianuskompressionstest ist nach circa einer Minute positiv.
Diagnostik
[Bearbeiten | Quelltext bearbeiten]Auch wenn Anamnese und der körperliche Untersuchungsbefund häufig für ein Karpaltunnelsyndrom charakteristisch sind, kann nur die Messung der Nervenleitgeschwindigkeiten die Diagnose sichern. Es wird die motorische Überleitungszeit („distale motorische Latenz“) des Nervus medianus zwischen dem Stimulationsort am Handgelenk und der von diesem Nerv innervierten Daumenballenmuskulatur gemessen. Als normal gelten Werte < 4,2 Millisekunden. Die Normwerte hängen dabei aber von der gewählten Technik ab und sind nicht unbedingt von Untersucher zu Untersucher gleich. Daher sollten immer beide Hände im Seitenvergleich gemessen werden und die ermittelten Werte auch mit den entsprechenden Werten des N. ulnaris verglichen werden. Typischerweise ist bei Vorliegen eines Karpaltunnelsyndroms auch die sensible Nervenleitgeschwindigkeit des Nervus medianus zwischen Zeigefinger- oder Mittelfingermittelgelenk und Handgelenk langsamer als die sensible Nervenleitgeschwindigkeit des zum Vergleich gemessenen Nervus ulnaris derselben Hand (sie liegt beim Gesunden für beide Nerven bei etwa 48 m/s). Oft zeigt sich, dass an einer beschwerdefreien Gegenhand elektrophysiologisch bereits (wenn auch geringer) auffällige Werte zu finden sind. Eine Antwort auf die Frage, ob es sich um eine (vorübergehende) Blockade der Nervenleitung (Neurapraxie) oder gar um einen aktuellen Nervenfaseruntergang (Axonotmesis) handelt, kann nur die Elektromyographie liefern.
Bei einer Diskrepanz zwischen Untersuchungsbefunden und gefundenen Messwerten kann die Messung der sensiblen Nervenleitgeschwindigkeit durch Reiz am Finger und Ableitung sowohl in der Hohlhand als auch jenseits des Karpaltunnels erfolgen, um die Leitgeschwindigkeit selektiv im Bereich des Karpaltunnels zu messen. Auch der Vergleich der Antworten des N. medianus und N. ulnaris nach Ringfingerreiz kann dann nützlich für die Diagnosestellung sein.
Falls keine Vergleichsmessungen vorgenommen werden, sollten bei den Messungen der Nervenleitgeschwindigkeiten die Hände ausreichend warm sein, da die Geschwindigkeit pro °C um etwa 2 m/s langsamer wird. Die ideale Messtemperatur liegt bei 34 °C.
Wegen der Kompression durch das Retinakulum kommt es zu einer eng lokalisierten Schwellung (Pseudoneurom) des N. medianus am Karpaltunneleingang. Diese kann mit einer Ultraschalluntersuchung beurteilt werden. Dabei wird die Nervenquerschnittsfläche an mehreren Stellen gemessen. Spezialisierte handchirurgische Zentren können in den meisten Fällen bereits hierdurch eine verlässliche Diagnose stellen, so dass in Verbindung mit einer entsprechenden klinischen Symptomatik auf die (häufig schmerzhafte) Messung der Nervenleitgeschwindigkeit verzichtet werden kann. Zusätzlich können bei der Ultraschalluntersuchung andere, in diesem Zusammenhang aber wichtige krankhafte Veränderungen erkannt werden wie Sehnenscheidenentzündungen, überlange Muskelbäuche oder Mittelarterien.
Differentialdiagnostisch kommen vor allem Schäden im Bereich der Halswirbelsäule in Betracht, die zu einer Irritation des Rückenmarks oder von Spinalnervenwurzeln führen (Cervicobrachialsyndrom, vor allem Nervenwurzel C6). Auch bei diesen Erkrankungen können Schmerzen und Missempfindungen über den Arm bis ins Handgelenk einstrahlen. Daneben kann der Nervus medianus weiter proximal komprimiert sein, als Pronator-teres-Syndrom. In Einzelfällen können auch Erkrankungen oder ein Kompressionssyndrom der arteriellen Gefäße entsprechende Beschwerden auslösen. Es sollte deshalb bei der Untersuchung nicht auf ein Tasten des Radialispulses und eine vergleichende Messung des Blutdrucks an beiden Armen verzichtet werden.
Konservative Therapie
[Bearbeiten | Quelltext bearbeiten]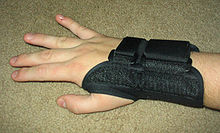
Im Anfangsstadium des Karpaltunnelsyndroms kann eine konservative Behandlung versucht werden.
Zumindest im Frühstadium lassen sich die Symptome durch „Ausschütteln“ und Reiben, Pumpbewegungen der Finger, Lageänderung, Halten unter kaltes Wasser usw. bessern oder beseitigen.[6]
Findet sich anamnestisch eine schwere mechanische, repetitive Überbelastung, so kann der Verzicht auf die beschwerdeauslösende Tätigkeit eine Besserung bringen. Das Tragen spezieller Nachtschienen oder auch das Anlegen von geformten Stützverbänden, die vom Sanitätsfachhandel auch für tagsüber angeboten werden, vermag die Beschwerden zumindest für eine Zeit lang zu beseitigen oder abzumildern. Die Nachtschiene verhindert dabei das nächtliche Abknicken der Hand, indem das Handgelenk ruhig gestellt wird.
Als unterstützende oder alternative Therapie können schmerzstillende und entzündungshemmende Medikamente eingesetzt werden, wie zum Beispiel nichtsteroidale Entzündungshemmer oder eine lokale Infiltration von Kortikoiden in den Karpaltunnel.[7] Ebenfalls angewandt werden Kältetherapie zur Senkung der Entzündungsaktivität oder Wärmetherapie zur Durchblutungsförderung.
Treten die Symptome im Zusammenhang mit einer Schwangerschaft auf, so ist zu erwarten, dass sie nach deren Ende abklingen.[8]
Operative Therapie
[Bearbeiten | Quelltext bearbeiten]Ein operativer Eingriff wird bei trotz konservativer Behandlung andauernden Beschwerden durchgeführt, damit bleibende Schäden vermieden werden. Er kann in der Regel ambulant durchgeführt werden.
Anästhesie
[Bearbeiten | Quelltext bearbeiten]Der Eingriff wird in der Regel in Regionalanästhesie durchgeführt. Eine Betäubung des ganzen Armes ist erforderlich, damit sich die Blutleere, die für die Operation benötigt wird, besser ertragen lässt. Sie kann als axilläre Blockade oder intravenöse Regionalanästhesie durchgeführt werden. Zur Herstellung der Blutleere wird das Blut mit einer straffen Binde aus dem Arm „gewickelt“ und das Zurückströmen des Blutes durch eine Blutsperrmanschette verhindert. Bei der intravenösen Regionalanästhesie wird dann durch die Auffüllung der Venen mit einem Lokalanästhetikum bewirkt, dass der gesamte Arm schmerzfrei ist. Bei der subaxillären Regionalanästhesie werden die zum Arm ziehenden Nerven in der Achselhöhle betäubt.
Auch eine Vollnarkose kommt in Betracht.
Offene Operationstechnik
[Bearbeiten | Quelltext bearbeiten]
Der Operateur arbeitet von außen mit direkter Sicht auf das Operationsfeld, teilweise mit optischer Vergrößerung. Der Hautschnitt kann in der ulnaren Verlängerung des Mittelfingers kurvenförmig parallel zur oder auf der Thenarfalte hin verlaufen. Die Handgelenksbeugefalte sollte man nicht überschreiten, um den Ramus palmaris nervi mediani und den Nervus ulnaris zu schützen. Weiters ist auch das Eröffnen des Canalis ulnaris (Guyon-Loge) auf der ulnaren Seite zu vermeiden.[9][10][11][12]
Eine Alternative ist die „Kurzschnitt-Technik“ mit einem Hautschnitt unmittelbar distal der Handgelenksbeugefalte[13] oder eine weiter körperfern gelegene „Mini-Inzision“[14][15] oder ein Doppelschnitt.[16]
Die Operation besteht in der vollständigen Durchtrennung des Retinaculum flexorum, jenes Bandes, das die Handwurzelknochen überspannt und den Karpaltunnel hohlhandwärts begrenzt. Der Nerv erholt sich in der Folge durch die erreichte Druckentlastung, sofern die Schädigung durch das Karpaltunnelsyndrom noch nicht zu lange bestanden hat. Entgegen früheren Gepflogenheiten empfehlen sich Maßnahmen direkt am Nerv nur in seltenen, gut begründeten Ausnahmefällen. Eine routinemäßige Eröffnung der Bindegewebshülle um den Nerven (Epineurotomie) ist bei Ersteingriffen in der Regel nicht notwendig,[17][18] eine operative Aufspaltung der einzelnen Nervenbündel (interfaszikuläre Neurolyse) führt zu schlechteren Ergebnissen und ist meist nicht angezeigt.[19][18] Die Darstellung des motorischen Thenarastes, der die Bewegung des Daumenballen steuert, ist meist nicht erforderlich, jedoch ist Vorsicht bei atypischem Abgang bzw. Normvarianten[20] geboten. Eine Entfernung der Schleimhaut (Synovialektomie) ist ebenfalls meist überflüssig[21] und nur bei auffallenden krankhaften Veränderungen wie beispielsweise bei vermehrter Schleimhautbildung oder entzündlich-rheumatischer Schleimhautentzündung (Synovialitis) und Amyloidose im Fall von Dialysepatienten notwendig. Eine Entfernung der Palmaris-longus-Sehne sollte nur bei anschließender autologer Transplantation erfolgen. Atypische Muskeln oder Sehnen innerhalb des Karpalkanals können im Einzelfall entfernt werden. Eine Rekonstruktion des Retinakulum (z. B. durch eine Z-Plastik) zur Verbesserung der Grobkraft nach Operation wurde vorgeschlagen, aber nur von einzelnen Chirurgen durchgeführt, wobei die Aussagen hierüber einander widersprechen.[22][23][24]
Der Eingriff gehört zu den häufigsten handchirurgischen Operationen, dauert wenige Minuten und ist sehr sicher, d. h. mit minimaler Komplikationsrate behaftet. Typische Probleme sind gelegentliche Narbenbeschwerden, die einer Abhärtungsbehandlung bedürfen, und eine Minderung der groben Kraft über einige Monate.
Endoskopische Operationstechnik
[Bearbeiten | Quelltext bearbeiten]Der Operateur arbeitet endoskopisch, also von innen her, mit instrumenteller Sicht auf das Operationsfeld.
Sonographisch geführte Operationstechnik
[Bearbeiten | Quelltext bearbeiten]Diese neue Option einer operativen Sanierung eines Karpaltunnelsyndromes wurde erstmals von Petrover[25] und – optimiert – durch das Team von Gruber[26] durchgeführt: Es erfolgt eine nur sehr kleine Stichinzision am Unterarm, durch welche, unter sonographischer Kontrolle, die gesamte Durchtrennung des strangulierenden transversalen Handwurzelbandes in lokaler Betäubung durchführt wird. Der große Vorteil besteht, bei vergleichbarem Effekt zur offenen OP, darin, dass die Hand unmittelbar wieder genutzt und im Wesentlichen voll belastet werden kann.
Ergebnisse und Komplikationen
[Bearbeiten | Quelltext bearbeiten]Der Therapieerfolg hängt wesentlich von Dauer und Ausmaß der bisherigen Nervschädigung ab. In unkomplizierten Fällen behebt die Karpaltunnelspaltung sofort sämtliche Beschwerden und beseitigt Schmerzen und nächtliche Missempfindungen. Sofern bereits Gefühlsstörungen, Missempfindungen und/oder Muskelschwäche bestanden haben, kann nicht in jedem Fall von sofortigem oder vollständigem Verschwinden ausgegangen werden.
Die allgemein möglichen Begleiterscheinungen chirurgischer Eingriffe (z. B. Nachblutung, Infektion, Schwellungen oder Verletzung von Nerven und Blutgefäßen) sind selten geworden. In Ausnahmefällen kann es unabhängig von der gewählten Operationstechnik zu einer langwierigen, unter Umständen sehr schmerzhaften Knochenentkalkung oder Weichteilschwellung kommen, die auch Gelenkversteifungen zur Folge haben kann (Morbus Sudeck).
Vergleich der offenen und endoskopischen Technik
[Bearbeiten | Quelltext bearbeiten]In einer amerikanischen Übersichtsarbeit wurden Daten von über 58.000 Eingriffen zwischen 2007 und 2014 ausgewertet, und es erfolgte in 86 % ein offenes Vorgehen gegen 14 % endoskopische Eingriffe. 60 % der Patienten waren Frauen, die größte Alterskohorte war die zwischen 65 und 69 Jahren.[27]
Die endoskopischen Verfahren haben gegenüber den offenen Techniken weder eindeutige Vor- noch Nachteile.[28] Die Operationsergebnisse sind insgesamt vergleichbar mit denen der offenen Operation,[29][30][31] auch im Vergleich zur Mini-Inzision.[32][33] Der höheren Patientenzufriedenheit bei unkompliziertem Verlauf[34] und dem geringeren Narbenschmerz bei endoskopischen Verfahren stehen eine höhere Komplikationsrate[35][36][37][31] und schlechtere Langzeitergebnisse gegenüber als bei der offenen Operation. Vor allem sind die unvollständige Spaltung des Retinakulums und eine Verletzung des motorischen Thenarastes[38][39] möglich. Der endoskopische Eingriff ist mit einem höheren Materialaufwand, höheren technischen Schwierigkeit und längeren Operationszeit verbunden. Die Revisionsrate, d. h. die Notwendigkeit, erneut zu operieren, ist ebenfalls höher. Ebenso sind die OP-Kosten und die Krankenhauskosten höher, jedoch die Kosten für anschließende Krankengymnastik niedriger.[27]
Beim offenen Eingriff ebenso wie bei endoskopischem Vorgehen kann es vorkommen, dass das Retinakulum unvollständig gespalten wird oder der N. medianus und seine Äste, aber auch der N. ulnaris geschädigt werden.[40][41]
In einer Nachuntersuchung nach durchschnittlich 13 Jahren waren von 113 Patienten, die „offen“ in Massachusetts/U.S.A. operiert wurden, 74 % komplett beschwerdefrei (davon 80 % der Frauen und nur 59 % der Männer) und 88 % zufrieden bis sehr zufrieden. Nur zweimal (1,8 %) musste eine erneute Operation durchgeführt werden. Alle Patienten ohne Begleiterkrankungen waren komplett beschwerdefrei, während das Ergebnis umso schlechter war, je mehr Begleiterkrankungen vorlagen. Besonders bei Diabetes, Polyneuropathie, Rheuma und Arthrose waren Funktion und Zufriedenheit postoperativ seltener gut bis sehr gut.[42]
Nachbehandlung
[Bearbeiten | Quelltext bearbeiten]Für die ersten Tage ist ein Watteverband oder ein Verband mit leichter Kompression im Wundgebiet ohne Einschnürung erforderlich. Manchmal wird auch eine kurzzeitige Ruhigstellung des Handgelenks durch eine Handgelenksorthese oder eine Gipsschiene durchgeführt. Bei Bedarf kann eine schmerzlindernde Medikation erfolgen. Postoperative Kältepacks können schmerzlindernd wirken. Spezielle „Narbensalben“ sind nicht erforderlich, allenfalls kann eine fetthaltige Salbe zur Narbenbehandlung empfohlen werden.
Eine frühe funktionelle Behandlung mit selbständigen Bewegungsübungen der Finger ohne oder nur mit geringer Belastung bereits am ersten postoperativen Tag beugt einem Handödem und einer Fingersteife vor und führt zu einer früheren Gebrauchsfähigkeit der Hand im täglichen Leben und im Beruf.[43]
Die Narbe ist meist nach sechs Monaten annähernd unsichtbar verheilt. Die Dauer der Arbeitsunfähigkeit beträgt je nach Tätigkeitsfeld wenige Tage bis einige Wochen.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Literatur
[Bearbeiten | Quelltext bearbeiten]- S3-Leitlinie Karpaltunnelsyndrom, Diagnostik und Therapie der Deutschen Gesellschaft für Handchirurgie (DGH). In: AWMF online (Stand 2012)
- Hans Assmus, G. Antoniadis: Nervenkompressionssyndrome. Steinkopff, Berlin 2008, ISBN 978-3-7985-1818-6, S. 46 f. eingeschränkte Vorschau in der Google-Buchsuche
- K. Giersiepen, M. Spallek: Karpaltunnelsyndrom als Berufskrankheit. In: Deutsches Ärzteblatt. Band 108, Nr. 14, 2011, S. 238–242. (aerzteblatt.de)
- Riccardo Luchetti, P. Amadio (Hrsg.): Carpal Tunnel Syndrome. Springer-Verlag, Berlin 2007, ISBN 978-3-540-22387-0.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Jasmine Z. Cheng, Mohit Sodhi, Mahyar Etminan, Bruce C. Carleton: Fluoroquinolone Use and Risk of Carpal Tunnel Syndrome: A Pharmacoepidemiologic Study. In: Clinical Infectious Diseases. Band 65, Nr. 4, 15. August 2017, ISSN 1058-4838, S. 684–686, doi:10.1093/cid/cix362 (oup.com [abgerufen am 10. März 2018]).
- ↑ N. Williams, D. Calloumas, D. Ketteridge, P. J. Cundy. D. M. Eastwood: The mucopolysaccharidoses. In: The Bone & Joint Journal. Band 99-B, 2017, S. 1132–1139, doi:10.1302/0301-620X.99B9.BJJ-2017-0487
- ↑ J. Carls, P. Mailänder: Kindliches beiderseitiges Karpaltunnelsyndrom bei Madelung – Deformität. In: Springer Verlag (Hrsg.): Monatsschrift Kinderheilkunde. Band 147, Nr. 3. Springer, März 1999, S. 269–274.
- ↑ Carpal tunnel syndrome, familial. In: Online Mendelian Inheritance in Man. (englisch)
- ↑ Carpal tunnel syndrome 2. In: Online Mendelian Inheritance in Man. (englisch)
- ↑ Karpaltunnelsyndrom – Diagnostik und Therapie (Langfassung). (PDF) AWMF, Juli 2012, abgerufen am 14. Oktober 2019. S. 6.
- ↑ Diagnostik und Behandlung des Karpaltunnelsyndroms. ( vom 3. September 2013 im Internet Archive) (PDF) Deutsche Gesellschaft für Handchirurgie
- ↑ A. Zyluk: Carpal tunnel syndrome in pregnancy: a review. In: Pol Orthop Traumatol. Band 78, 7. Okt 2013, S. 223–227. PMID 24104526.
- ↑ S. Ariyan, H. K. Watson: The palmar approach for the visualization and release of the carpal tunnel. An analysis of 429 cases. In: Plast Reconstr Surg. Band 60, 1977, S. 539–547. PMID 909963.
- ↑ H. Nigst: The carpal tunnel syndrome. Operative technique for surgical decompression. In: Orthop and Traumat. Band 1, 1992, S. 122–129.
- ↑ R. H. Gelberman, E. R. North: Carpal tunnel release. Open release of transverse carpal ligament. In: R. H. Gelberman (Hrsg.): Operative nerve repair and reconstruction. JB Lippincott, Philadelphia 1991, S. 899–912.
- ↑ W. B. Connolly: Treatment for carpal tunnel syndrome. Wolfe, London 1984.
- ↑ J. H. Huang, E. L. Zager: Mini-open carpal tunnel decompression. In: Neurosurgery. Band 54, Nr. 2, Feb 2004, S. 397–399; discussion 399–400. PMID 14744287
- ↑ G. S. Bromley: Minimal-incision open carpal tunnel decompression. In: J Hand Surg Am. Band 19, Nr. 1, Jan 1994, S. 119–120. PMID 8169355.
- ↑ W. Schmidt, A. A. Gruber, R. Hammer: [Results of different incisions in treatment of carpal tunnel syndrome]. In: Handchirurgie, Mikrochirurgie, plastische Chirurgie. Band 32, Nummer 1, Januar 2000, S. 67–69, doi:10.1055/s-2000-19242. PMID 10763132.
- ↑ K. M. Wilson: Double incision open technique for carpal tunnel release: an alternative to endoscopic release. In: J Hand Surg Am. Band 19, Nr. 6, Nov 1994, S. 907–912. PMID 7876487
- ↑ Borisch und Haussmann 2003.
- ↑ a b Scholten 2004.
- ↑ Chapell u. a. 2003.
- ↑ Lanz 1977.
- ↑ Shum u. a. 2002.
- ↑ Karlsson u. a. 1997.
- ↑ Netscher u. a. 1997.
- ↑ Rosenbaum u. Ochoa 2002.
- ↑ D. Petrover, J. Silvera, T. De Baere, M. Vigan, A. Hakimé: Percutaneous Ultrasound-Guided Carpal Tunnel Release: Study Upon Clinical Efficacy and Safety. In: Cardiovascular and interventional radiology. Band 40, Nummer 4, April 2017, S. 568–575, doi:10.1007/s00270-016-1545-5, PMID 28028577, PMC 5336536 (freier Volltext)
- ↑ A. Loizides, S. Honold, E. Skalla-Oberherber, L. Gruber, W. Löscher, B. Moriggl, M. Konschake, H. Gruber: Ultrasound-Guided Minimal Invasive Carpal Tunnel Release: An Optimized Algorithm. In: Cardiovascular and interventional radiology. Band 44, Nummer 6, Juni 2021, S. 976–981, doi:10.1007/s00270-021-02789-2, PMID 33629135, PMC 8172390 (freier Volltext).
- ↑ a b Steven Zhang, Molly Vora, Alex H. S. Harris, Laurence Baker, Catherine Curtin, Robin N. Kamal: Cost-minimization analysis of open and endoscopoc carpal tunnel release. In: The Journal of Bone & Joint Surgery. Band 98-A, Ausgabe 23, 7. Dezember 2016, S. 1970–1977. doi:10.2106/JBJS.16.00121
- ↑ Scholten 2004.
- ↑ Antoniadis u. a. 1997.
- ↑ Ferdinand u. MacLean 2002.
- ↑ a b Thoma u. a. 2004.
- ↑ Hallock u. Lutz 1995.
- ↑ Wong u. a. 2003.
- ↑ Trumble u. a. 2001.
- ↑ Brown u. a. 1993.
- ↑ Einhorn u. Leddy 1996.
- ↑ Shinya u. a. 1995.
- ↑ Concannon u. a. 2000.
- ↑ MacDermid u. a. 2003.
- ↑ Hunt u. Osterman 1994.
- ↑ Assmus u. a. 2006.
- ↑ Dexter L. Louie, Brandon E. Earp, Jamie E. Collins, Elena Losina, Jeffrey N. Katz, Eric M. Black, Barry P. Simmons, Philip E. Blazar: Outcomes of open carpal tunnel release at a minimum of ten years. In: The Journal of Bone & Joint Surgery. Band 95-Am, Ausgabe 12, 19. Juni 2013, S. 1067–1073. doi:10.2106/JBJS.L.00903.
- ↑ Cook u. a. 1995.