Lungenembolie
| Klassifikation nach ICD-10 | |
|---|---|
| I26 | Lungenembolie |
| O88 | Embolie während der Gestationsperiode |
| O08.2 | Embolie nach Abort, Extrauteringravidität und Molenschwangerschaft |
| ICD-10 online (WHO-Version 2019) | |
Eine Lungenembolie (kurz: LE) oder Lungenarterienembolie (kurz: LAE) ist eine Verstopfung (Embolie) eines Blutgefäßes in der Lunge bzw. dem Lungenkreislauf. Sie wird meistens durch einen Blutpfropfen (Blutgerinnsel), den sogenannten Thrombus (dann wird sie auch Lungenthrombembolie, pulmonale Thromboembolie oder Pulmonalarterienthrombembolie genannt), seltener durch Gasbläschen, beispielsweise bei einem Tauchunfall oder durch während einer Operation angesaugte Luft, oder durch Fett (Fettembolie, etwa durch Fett aus dem Fettmark bei Knochenbrüchen) verursacht. Da eine Lungenembolie potentiell lebensbedrohlich ist, sind Maßnahmen zur Ersten Hilfe immer erforderlich. Der sinkende Blutdruck (Hypotonie) kann zum obstruktiven Schock mit Kreislaufstillstand führen.
Typische Symptome sind akute Luftnot (Dyspnoe) und/oder Brustschmerz beim Einatmen. Der Mangel an Sauerstoff (Hypoxie) verursacht einen Ruhepuls von über 100/min (Tachykardie), der von einer hohen Atemfrequenz (Tachypnoe) begleitet wird. Die weitere Symptomatik ist sehr variabel und kann Husten (lat.: Tussis), Blut im Auswurf (Hämoptyse) sowie Herzrhythmusstörungen beinhalten. Bei einer zusätzlich (Komorbidität) bestehenden tiefen Beinvenenthrombose (Tiefe Venenthrombose – TVT) ist das betroffene Bein meist angeschwollen und schmerzt. Wegen des erhöhten Pumpwiderstandes im Lungenkreislauf (pulmonale Hypertonie) wird die rechte Herzkammer stärker belastet (Cor pulmonale), was zu einer Herzinsuffizienz führen kann.
Neben der bedarfsweisen Zufuhr von Sauerstoff wird eine Lysetherapie zur Auflösung des Thrombus durchgeführt. Zur Hemmung der Blutgerinnung (Antikoagulation) dient intravenös appliziertes Heparin. Nach Abklingen der akuten Symptome ist zur Vermeidung erneuter Thrombosen meist eine längerzeitige Therapie mit peroral verabreichten Antikoagulanzien (siehe Medizinische Maßnahmen) erforderlich.
In Deutschland sterben jährlich zwischen 40.000 und 100.000 Menschen an einer Lungenembolie. Sie ist damit nach Herzinfarkt und Schlaganfall die dritthäufigste zum Tode führende Herz-Kreislauf-Erkrankung.[1]
Entstehung
[Bearbeiten | Quelltext bearbeiten]
Ein eine Lungenembolie auslösendes Blutgerinnsel entsteht in bis zu 80 % aller Fälle in den tiefen Bein- oder Beckenvenen und gelangt über die untere Hohlvene, den rechten Vorhof und Ventrikel des Herzens in beide Pulmonalarterien. Im Verlauf bleibt der Thrombus stecken und verschließt das Gefäß. Je größer der Thrombus, desto größer ist das dahinter nicht mehr durchblutete Lungengebiet. Oft handelt es sich um mehrere Thromben, die gleichzeitig oder auch in zeitlichem Abstand Lungengefäße ganz oder teilweise verstopfen.
Auch können beide Lungenflügel eines Patienten betroffen sein. Unter der Geburt kann es auch zu Fruchtwasserembolien, bei Brüchen der langen Röhrenknochen (z. B. Femur) zu Fettembolien kommen. Selbst Knochenmarksembolien sind in der Lunge möglich. Weiter können bei Verletzungen oder ärztlichen Maßnahmen Luft oder andere Gase (beispielsweise CO2 im Rahmen einer Laparoskopie) ins venöse Gefäßsystem gelangen.
Die Lungenembolie gehört zu den am häufigsten übersehenen Todesursachen.[2]
Die Letalität einer unbehandelten schweren Lungenembolie ist mit 30 % sehr hoch. Eine sofortige Behandlung kann die Sterblichkeit auf 2–8 % senken.[3]
Pathophysiologie
[Bearbeiten | Quelltext bearbeiten]Der Embolus verstopft einen oder mehrere Äste der Lungenarterien. Dies wiegt umso schwerer, je größer der Innendurchmesser des betroffenen Gefäßes ist. Der Blutstau vor dem Thrombus führt zu einer mehr oder weniger starken Druckerhöhung im Lungenkreislauf (Pulmonale Hypertonie) und damit zur Belastung des rechten Teils des Herzens, wodurch es teilweise oder sogar ganz versagen kann. Versagt die rechte Herzhälfte nicht, so ist dennoch zumindest die Blutmenge vermindert, die die Lunge passieren und zur linken Herzhälfte gelangen kann. Die linke Herzhälfte kann jedoch nur soviel Blut weiterpumpen, wie bei ihr ankommt. Die Folge der herabgesetzten Fördermenge ist eine verminderte Sauerstoffversorgung der wichtigen Organe.[4] Es kann zum (kardiogenen) Schock kommen. In Abhängigkeit von der Ausdehnung kann es zu einem geringeren Sauerstoffgehalt des Blutes – einer Hypoxämie – kommen.
Eine plötzlich auftretende schwere Lungenembolie wird als fulminant bezeichnet. Führend in der Symptomatik ist hierbei das Versagen des rechten Herzens (Rechtsherzversagen), begleitet von einer schweren Hypoxämie.
Auch kleinere Lungenembolien können zu Rechtsherzproblemen führen. Hier ist die Drucksteigerung im kleinen Kreislauf nicht so schwerwiegend, die akute Überlebensrate der Patienten auch daher deutlich höher. Die Thromben werden in den meisten Fällen abgebaut und das Gefäßsystem dadurch wieder frei. Trotzdem kann sich im weiteren Verlauf bei einigen Patienten (vor allem mit immer wiederkehrenden kleineren Lungenembolien) ein chronischer Lungenhochdruck entwickeln. Es kann sich dann um eine CTEPH handeln.
Nachfolgend zum akuten Ereignis kann eine Infektion des nicht mehr ausreichend versorgten Lungengewebes zu einer sogenannten Infarktpneumonie führen. Das hinter dem Embolus gelegene Lungenareal kann insbesondere nach größerer Embolie mit Zerstörung eines Teils des bindegewebigen Lungengrundgerüstes infarzieren. Trotz der an sich hohen Regenerationskraft des Lungengewebes sterben dann ganze Bereiche dauerhaft ab. Übersteht dies der Organismus, entstehen funktionslose Narben. Bei Befall größerer Bereiche mit entsprechender Funktionseinbuße kommt es zu Kurzatmigkeit, reduzierter Belastbarkeit und oft dauerhaftem Husten. Die erleichterte Invasion von Keimen in das anfangs nekrotische, anschließend fibrotisch veränderte – und für Antibiotika weitgehend unzugängliche – narbige Gewebe führt auch später häufiger zu Lungenentzündungen. Die fibrotischen Umbauprozesse erhöhen geringfügig auch das Risiko für späteren Lungenkrebs. Es gibt eine hohe Rate der Spätkomplikationen, insbesondere bei erneuten Embolien.
Ursachen und Auslöser
[Bearbeiten | Quelltext bearbeiten]Es gibt bestimmte Risikopatienten, die zu Thrombosen und damit zu Lungenembolien neigen.
Disponierende Faktoren sind in der Vorgeschichte des Patienten: Fraktur (Hüfte oder Bein), Hüft- oder Knie-Totalendoprothese, große Operation, Lungenerkrankung, Hormonersatztherapie, bösartiger Tumor, orale Kontrazeption, Schlaganfall, Schwangerschaft, Phase kurz nach der Geburt, vorangegangene venöse Embolie, Störung der Blutgerinnung, hohes Alter, hohe Homocysteinspiegel.
Bei entsprechender Prädisposition kann dann jede Immobilisierung –, besonders der unteren Gliedmaßen –, zum Auslöser werden, die durch Stase des Blutes das Anwachsen eines Thrombus (ähnlich „Kondensation“) begünstigen: Blutstauung bei lange angewinkeltem Knie, etwa bei langen Busfahrten oder beim Langstreckenfliegen, Reisethrombose, nach Brüchen und Verstauchungen sowie Bettlägerigkeit jeder Art.
Den Zeitpunkt des akuten Eintritts bestimmt dagegen erst das spätere Ablösen eines Thrombus und dessen Einschwemmen in die Lunge. Das geschieht typisch durch Mobilisierung nach dem Ruhen, also teilweise deutlich nach dem Aufstehen, beim Pressen (Stuhlgang) und anderen ersten körperlichen Anstrengungen danach. Ihnen allen ist die plötzliche Blutdruckänderung im venösen System mit einer Dilatation der Gefäße nach Inaktivität gemeinsam. (Quellen unter[5])
Symptomatik
[Bearbeiten | Quelltext bearbeiten]Typische Anzeichen einer Lungenembolie sind akute Luftnot und/oder Brustschmerz beim Einatmen. Die weitere Symptomatik ist sehr variabel und oft gekennzeichnet durch die Erhöhung von Ruhepuls (über 100/min, Tachykardie mit Herzrhythmusstörungen) und Atemfrequenz (Tachypnoe). Auftretender Husten ist vereinzelt mit Blut im Auswurf verbunden. Der niedrige Blutdruck (Hypotonie) kann zum Schock führen.
Bei 20 bis 55 % der Fälle von Lungenembolie besteht ein Pleuraerguss.[6]
Führt eine plötzlich einsetzende (fulminante) Lungenembolie zum Kreislaufstillstand, dann sind im Rahmen von Reanimationsmaßnahmen häufig gestaute Halsvenen (als Zeichen einer oberen Einflussstauung bei bestehendem „Vorwärtsversagen“ des Herzens) erkennbar. Bedingt durch die Unterversorgung des Blutes mit Sauerstoff wird klassisch die sogenannte „Kranzzyanose“ (oder auch „schwedischer Kragen“) erkennbar: Hals und Dekolleté wirken dunkel marmoriert.
Schweregradeinteilung
[Bearbeiten | Quelltext bearbeiten]Nach Grosser
[Bearbeiten | Quelltext bearbeiten]| Schweregrad I | Schweregrad II | Schweregrad III | Schweregrad IV | |
|---|---|---|---|---|
| Klinik | diskret, in 80 % klinisch stumm | Akute Dyspnoe, Tachypnoe, thorakaler Schmerz, Angst, Hämoptysen, Fieber, Pleuraerguss (durch Transsudat oder Exsudat) | Zusätzlich Schocksymptomatik | |
| Blutdruck | normal | evtl. leicht erniedrigt | erniedrigt | stark erniedrigt |
| Gefäßverschluss | periphere Äste | Segmentarterien | PA-Ast oder mehrere Lappenarterien | Ein PA-Ast und mehrere Lappenarterien |
Nach ESC (Europäische Gesellschaft für Kardiologie) 2008
[Bearbeiten | Quelltext bearbeiten]| Frühsterblichkeit | |||
|---|---|---|---|
| niedrig (< 1 %) | mittel (3–15 %) | hoch (> 15 %) | |
| Schock oder Hypotonie | nein | nein | ja (triggert Therapie) |
| RV-Dysfunktion | nein | nein/ja* | möglich |
| Troponin erhöht | nein | nein/ja* | möglich |
| *mind. eines der beiden Kriterien | |||
| Therapie | frühe Entlassung | Krankenhausbehandlung | Thrombolyse oder Embolektomie |
PESI
[Bearbeiten | Quelltext bearbeiten]Der PESI (Pulmonary Embolism Severity Index) ist ein Scoring-System zur Risikostratifizierung nicht-massiver Lungenembolien (systolischer Blutdruck > 90 mmHg). Anhand von 11 Kriterien werden die Patienten in fünf Risikoklassen eingeteilt. Bei einer PESI-Risikoklasse von I oder II ist die Sterblichkeitsrate niedrig und eine ambulante Therapie kann in Erwägung gezogen werden.
| Prädiktor | Punkte |
|---|---|
| Alter | Anzahl Jahre |
| männliches Geschlecht | 10 |
| Krebs | 30 |
| Herzinsuffizienz | 10 |
| Puls ≥ 110/min | 20 |
| systolischer Blutdruck < 100 mmHg | 30 |
| Atemfrequenz ≥ 30/min | 20 |
| Temperatur < 36 °C | 20 |
| verminderter Bewusstseinszustand | 60 |
| Sauerstoffsättigung < 90 % | 20 |
| PESI-Risikoklasse | Punkte |
| I | ≤ 65 |
| II | 66–85 |
| III | 86–105 |
| IV | 106–125 |
| V | ≥ 125 |
Diagnostik
[Bearbeiten | Quelltext bearbeiten]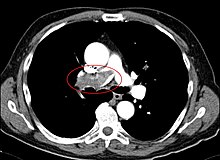
Bei klinischem Verdacht auf eine Lungenembolie, der sich nach sorgfältiger Anamnese und Hilfestellung durch den Wells-Score oder Geneva-Score ergibt, kann die Diagnose am schnellsten mit einer kontrastmittelverstärkten Computertomographie gesichert werden. Im konventionellen Röntgenbild gibt es zwar beschriebene Röntgenzeichen für eine Lungenembolie (Hampton hump, Westermark- und Fleishner-Zeichen), jedoch sind diese eher selten vorhanden und oft nicht eindeutig.
Eine Lungenembolie lässt sich laborchemisch bei unauffälligen Dimeren mit hoher Sicherheit ausschließen. Erhöhte D-Dimere lassen keine Aussage zu, da sie leicht falsch positiv werden. So sind die D-Dimere nach Operationen, Sport oder Unfällen oft erhöht.
Rechtsherzbelastungszeichen als indirekte Zeichen einer Lungenembolie lassen sich im EKG (sog. SIQIII-Typ) und in der Echokardiographie nachweisen. In der Blutgasanalyse zeigt sich ein vermindertes pO2 bei einem gleichzeitig verminderten pCO2 als Folge der Hyperventilation bei Hypoxämie.
Kleinere Embolien, die der CT entgehen könnten, lassen sich mittels Lungenszintigraphie nachweisen. Dieses Verfahren kommt jedoch wegen der geringen Verfügbarkeit und der im Verhältnis zu modernen CT langen Untersuchungsdauer seltener zum Einsatz. In vielen Fällen kann die Nuklearmedizin mit der Lungenperfusions- und -inhalationsszintigraphie allerdings einen wertvollen Beitrag zur Diagnose einer Lungenembolie leisten: Bei Patienten mit Kontrastmittelallergie, mit Überfunktion der Schilddrüse oder mit schlechten Nierenwerten (erhöhtes Kreatinin) kann eine Computertomographie mit Kontrastmittel nicht durchgeführt werden; in diesen Fällen kann die exakte Diagnose nur nuklearmedizinisch gestellt werden. Die Lungenperfusionszintigrafie zeigt auf, ob der in eine Vene applizierte radioaktive Tracer regelmäßig in beiden Lungen dargestellt wird oder ob es keilförmige Abschwächungen bis Defekte in der Lunge gibt, was Hinweis für eine Lungenembolie sein kann. Bei der Inhalationsszintigraphie wird der Tracer eingeatmet und anschließend verglichen, ob die Darstellungen beider Untersuchungen gleich sind (gleich: kein Hinweis auf Lungenembolie) oder ob ein Unterschied besteht (Unterschied zwischen Perfusions- und Inhalationsszintigraphie: Beweis für eine Lungenembolie).
Auch die Magnetresonanztomografie (MRT) bietet die Möglichkeit zur Diagnostik der Lungenembolie. Diese kommt jedoch bei der gegenwärtigen Verbreitung geeigneter Geräte nur selten mit dieser Fragestellung zum Einsatz.
Die früher häufig durchgeführte konventionelle Angiografie der Lungenstrombahn liefert gute Ergebnisse. Sie wird jedoch wegen des damit verbundenen technischen Aufwandes, der erheblichen Belastung des Patienten und des Risikos, das mit der Einführung eines Katheters in den Lungenkreislauf des Patienten verbunden ist, seltener durchgeführt.
Erschwert wird die Symptombeurteilung und Diagnostik oft, weil mehrere, auch kleine Thromben in zeitlichen Abständen beteiligt sein können. Eine Hilfe bei der Diagnostik ist der Wells-Score, ein Punktesystem für die Wahrscheinlichkeit einer Embolie, der gut mit dem Ergebnis des D-Dimer-Tests kombiniert werden kann.
Differentialdiagnose
[Bearbeiten | Quelltext bearbeiten]Bei den Leitsymptomen einer schwerwiegenden Lungenembolie (Luftnot, Brustschmerz, Kreislaufinstabilität) kommt als Differentialdiagnose in erster Linie der Herzinfarkt in Frage, eventuell auch eine Lungenentzündung, ein Pneumothorax oder eine Aortendissektion.
Therapie
[Bearbeiten | Quelltext bearbeiten]Erste Hilfe
[Bearbeiten | Quelltext bearbeiten]Die Prognostizierung einer Lungenembolie für einen Ersthelfer ist meist recht schwierig und erfordert Vorwissen. Wenn man jedoch einen Verdacht auf eine solche hat, muss man als Ersthelfer schnell handeln. Maßnahmen, die man als Ersthelfer durchführen kann, sind:
- Sofort den Rettungsdienst über die Rufnummer 112 (in Europa) oder eine andere örtliche Notrufnummer alarmieren
- Den Erkrankten mit erhöhtem Oberkörper lagern
- Den Patienten beruhigen und zur ruhigen Atmung auffordern
- Den Erkrankten keine körperliche Anstrengung vornehmen lassen
- Für frische Luft sorgen und beengende Kleidungsstücke öffnen
- Weiter allgemeine Maßnahmen im Rahmen der Ersten Hilfe[7]
Medizinische Maßnahmen
[Bearbeiten | Quelltext bearbeiten]Eine Lungenembolie kann lebensbedrohlich sein. Kleine Lungenembolien bei stabilen Patienten können unter Umständen aber auch ambulant behandelt werden.
Neben der Sauerstoffzufuhr wird in jedem Fall eine Lysetherapie mit intravenös appliziertem Heparin zur Hemmung der Blutgerinnung (Antikoagulation) durchgeführt. Nach Abklingen akuter Symptome wird längerzeitig eine Thromboseprophylaxe mit direkten oralen Antikoagulanzien (DOAK) zur Vermeidung erneuter Thrombosen durchgeführt. Entsprechende Präparate sind Apixaban (Handelsname Eliquis; Hersteller: Bristol-Myers Squibb/Pfizer), Rivaroxaban (Handelsname Xarelto; Hersteller: Bayer) oder Dabigatran (Handelsname Pradaxa; Hersteller: Boehringer Ingelheim). Bereits sehr viel länger auf dem Markt sind die Cumarinpräparate Phenprocoumon (Handelsnamen Marcumar bzw. Falithrom) und Warfarin (Handelsname Coumadin).
Bei schweren Lungenembolien mit Schocksymptomen und beschriebener schwerer Rechtsherzbelastung sind Kreislaufstabilisierung und rasch „rekanalisierende“ Maßnahmen nötig. Neben der Lysetherapie werden als akut lebensrettende Maßnahme dann kathetertechnische mechanische „Zertrümmerung“ von lokalisierten Thromben wie auch eine operative Entfernung (Embolektomie) zu erwägen sein. Bei der operativen Ausräumung des Embolie-Materials existieren Verfahren ohne Einsatz der Herz-Lungen-Maschine und solche mit deren Einsatz. Gegebenenfalls erfolgt die Operation unter andauernder Wiederbelebung des Patienten als sogenannte Ultima Ratio (eine hochriskante, aber vielleicht lebensrettende Maßnahme).
Wenn eine künstliche Beatmung des Patienten wegen Sauerstoffmangels im Blut notwendig wird, sollte am Beatmungsgerät ein möglichst geringer Druck in der Ausatmungsphase (PEEP) sowie in der Einatmungsphase eingestellt werden. Ein zu hoher Beatmungsdruck würde den bereits durch die Lungenembolie belasteten rechten Teil des Herzens zusätzlich belasten.[8]
Die gerinnungshemmenden Stoffe müssen nach einer Lungenembolie für einige Monate, in manchen Fällen (bei bestimmten angeborenen Störungen des Gerinnungssystems sowie bei rezidivierenden Lungenembolien) lebenslang eingenommen werden, um erneute Thrombosen und Lungenembolien zu vermeiden.
Die beste Schutzmaßnahme ist die Thromboseprophylaxe, die vor allem bei bettlägerigen Patienten und postoperativ angewendet wird. Hierbei erhält der Patient ein gerinnungshemmendes Medikament (meist ein sogenanntes niedermolekulares Heparin) in das Unterhautfettgewebe gespritzt oder in Tablettenform verabreicht. Auch das Tragen von Kompressionsstrümpfen hat sich bewährt. Wichtig für die Prophylaxe ist auch eine rasche Mobilisation der Patienten.
Gesundheitsökonomie
[Bearbeiten | Quelltext bearbeiten]Die Zahl der durch Lungenembolien verursachten Todesfälle innerhalb der Europäischen Union wird auf rund 370.000 jährlich geschätzt. Die geschätzten Kosten der Behandlung für durch tiefe Beinvenenthrombosen verursachte Lungenembolien werden auf rund drei Milliarden Euro europaweit geschätzt.[9]
Literatur und Quellen
[Bearbeiten | Quelltext bearbeiten]- S2k-Leitlinie Diagnostik und Therapie der Venenthrombose und Lungenembolie
- Hannah C. Kulka et al.: Akute Lungenarterienembolie. Diagnostik und Therapie aus multidisziplinärer Sicht. In: Deutsches Ärzteblatt. Band 118, Nr. 37, 17. September 2021, S. 618–628. Digitalisat
- Deutsche Gesellschaft für Angiologie – Gesellschaft für Gefäßmedizin: Diagnostik und Therapie der Venenthrombose und der Lungenembolie. (PDF) Januar 2005, abgerufen am 13. Juli 2015.
- Europäische Gesellschaft für Kardiologie: Guidelines on the diagnosis and management of acute pulmonary embolism. (PDF; 1,1 MB) 2008, abgerufen am 5. Juli 2009 (englisch).
- Alexander Schellhaaß, Andreas Walther, Stavros Konstantinides, Bernd W. Böttiger: Diagnostik und Therapie bei akuter Lungenembolie. In: Dtsch Arztebl Int. Nr. 107 (34–35), 2010, S. 589–595 (Abstract).
- Drahomir Aujesky: Die ambulante Behandlung der Lungenembolie. In: PrimaryCare. Nr. 2, 2013, S. 30–31 (Online [PDF]).
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Deutsche Gesellschaft für Angiologie – Gesellschaft für Gefäßmedizin e. V.: Kampagne Risiko Thrombose. Berlin 2015, [1]
- ↑ nach: W. Huckenbeck (Institut für Rechtsmedizin, Universität Düsseldorf): Rechtsmedizinische Aspekte der Kausalkette Thrombose – Lungenembolie – Tod. In: Phlebologie. Heft 6, 1998, ISSN 0939-978X, S. 181–209 (Zusammenfassung auf: Schattauer.de ( vom 17. Dezember 2013 im Internet Archive)).
- ↑ Diedrich Bühler, Vera Wittenberg: Was ist eine Lungenembolie? In: Medizintexte der TK. Techniker Krankenkasse, 7. März 2019, abgerufen am 7. April 2019.
- ↑ Herbert Lippert: Lehrbuch Anatomie. 4. Auflage. Verlag Urban & Schwarzenberg, S. 190.
- ↑ A. Rahimtoola, J. D. Bergin: Acute pulmonary embolism: an update on diagnosis and management. In: Current problems in cardiology. 2005 Feb;30(2), S. 61–114.
- ↑ Berthold Jany, Tobias Welte: Pleuraerguss des Erwachsenen – Ursachen, Diagnostik und Therapie. In: Deutsches Ärzteblatt. Band 116, Nr. 21, (Mai) 2019, S. 377–385, hier: S. 377–381 und 383.
- ↑ Österreichisches Rotes Kreuz Generalsekretariat: Sanitätshilfe Ausbildung. 7. Auflage, Version März 2016, ISBN 978-3-902332-18-9.
- ↑ Guidelines on the diagnosis and management of acute pulmonary embolism. The Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC). In: European Heart Journal. (2008), 29, S. 2276–2315, doi:10.1093/eurheartj/ehn310.
- ↑ Samuel Z. Goldhaber: Deep Venous Thrombosis and Pulmonary Embolism. In: Dan L. Longo, Anthony S. Fauci, Dennis L. Kasper, Stephen L. Hauser, J. Larry Jameson: Harrisons’s Principles of Internal Medicine. Band 2, New York 2012, S. 2170.