Mimivirus
| Mimivirus | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

EM-Aufnahme eines Virions der Gattung Mimivirus, links oben der Vertex (Virologie) (siehe Stargate).[5] | ||||||||||||||||||
| Systematik | ||||||||||||||||||
| ||||||||||||||||||
| Taxonomische Merkmale | ||||||||||||||||||
| ||||||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||||||
| Mimivirus | ||||||||||||||||||
| Links | ||||||||||||||||||
|
Mimivirus ist eine Gattung von Viren aus der Familie Mimiviridae,[6][1][7] denen Amöben als natürliche Wirte dienen. Mit der Familie Mimiviridae gehört Mimivirus zu den Riesenviren im Phylum Nucleocytoviricota (auch englisch Nucleocytoplasmic large DNA viruses, NCLDV, nach einem früheren Vorschlag auch als Ordnung „Megavirales“ (s. l.) bezeichnet[8][5]).
Ursprünglich hatte das International Committee on Taxonomy of Viruses (ICTV) mit der Familie Mimiviridae die Gattung Mimivirus mit nur einer einzigen Spezies (Art), Acanthamoeba polyphaga mimivirus (ApMV oder APMV, heute wissenschaftlich Mimivirus bradfordmassiliense) bestätigt.[9]
Im Laufe der Zeit wurden in der nahen oder näheren phylogenetischen Verwandtschaft dieser Spezies viele weitere Kandidaten großer Viren gefunden, wobei sich im Wesentlichen zunächst drei Linien abzeichneten: Linie A (mit APMV – die heutige Gattung Mimivirus bradfordmassiliense), Linie B (nun Gattung Moumouvirus) und Linie C (nun Gattung Megavirus), später kamen noch die Linie der Tupanviren (nun Gattung Tupanvirus) sowie Cotonvirus hinzu. Diese Linien – zumindest die Linien A, B und C – wurden ursprünglich als Subkladen der sehr weit gefassten Gattung Mimivirus angesehen.
Mit der Reorganisation der Mimivirus-Ordnung Imitervirales im April 2023 hat das ICTV diese Linien in den Rang eigener Gattungen erhoben, in der Gattung Mimivirus wurde dabei nur eine einzige weitere Spezies bestätigt, Mimivirus lagoaense.[6] In der Umgangssprache und in älterer Literatur wird APMV üblicherweise nur als Mimivirus bezeichnet, umgekehrt werden oder wurden nicht nur Mitglieder der oben genannten Linien, sondern auch andere mehr oder weniger nahe Verwandte Stämme der Familie Mimiviridae oder gar Ordnung Imitervirales.[A. 1]
Entdeckung und Forschungsgeschichte
[Bearbeiten | Quelltext bearbeiten]Das Mimivirus ApMV wurde 1992 bei Forschungsarbeiten über die Legionärskrankheit (Legionellose) in einem Industriekühlturm in Bradford (England) entdeckt, wobei man feststellte, dass es sich in der Amöbe Acanthamoeba polyphaga repliziert (vermehrt). Im Jahr 2003 wurde es an der Université de la Méditerranée in Marseille von einer Arbeitsgruppe um Didier Raoult identifiziert.[14] Mit einem Durchmesser von 400 nm haben die Viruspartikel (Virionen) von ApMV die Größe von kleinen Bakterien.[15]
Wegen dieser Größe und der äußeren Ähnlichkeit mit kugelförmigen Bakterien (Kokken) sowie der Gram-Färbungseigenschaften hielt man es zunächst für ein grampositives Bakterium und vergab dafür die Gattungsbezeichnung Bradfordcoccus. Nachdem der Irrtum erkannt wurde, benannte man das neu entdeckte Virus in Anspielung auf seine Größe und Färbungseigenschaften Mimicking Virus („täuschendes Virus“). Schließlich wurde daraus die Gattungsbezeichnung Mimivirus, ein Kofferwort mit dem Namensteil mimi als eine Abkürzung für englisch mimicking microbe. Im Oktober 2004 wurde dann von Didier Raoult et al. die Struktur seines Erbguts in der Fachzeitschrift Science veröffentlicht.[16] Mimivirus blieb übrigens nicht das einzige Riesenvirus, bei dem sich ein solcher Irrtum ereignete: Ein weiteres Beispiel ist das „Misannotatedvirus“, das zunächst für ein Rickettsia-Bakterium gehalten wurde, und nun für ein Mitglied einer möglichen Riesenvirusfamilie „Pithoviridae“ gehalten wird.[17] Das gleiche Team, das das ApMV entdeckte, entdeckte später ein etwas größeres Virus, das „Acanthamoeba castellanii mamavirus“ (AcMV) zusammen mit dem Sputnik-Virophagen, der es infiziert. AcMV und ApMV sind so nahe verwandt, dass sie heute nicht nur in dieselbe Gattung Mimivirus,[18] sondern sogar in dieselbe Spezies Mimivirus bradfordmassiliense gestellt werden.[1]
Bis 2013, als ein noch größeres Virus, vorgeschlagen als „Pandoravirus“, beschrieben wurde, wiesen die Viren der Gattung Mimivirus den größten Kapsiddurchmesser aller bekannten Viren auf;[19] inzwischen wird es aber auch von nahen Verwandten Megavirus chilense, Tupanvirus, „Platanovirus“, „Satyrvirus“[2] (alle Mimiviridae), sowie anderen Riesenviren wie „Pithovirus“ übertroffen.
Wirte
[Bearbeiten | Quelltext bearbeiten]Der erste bekannte Mimivirus-Wirt ist die Amöbe Acanthamoeba polyphaga (Gattung Acanthamoeba, Amoebozoa). Bisher konnten labormäßig nur Vertreter dieser Gattung (außer A. polyphaga noch A. castellanii und A. mauritaniensis) als Wirte dieses Virus eingesetzt werden, keine Zellen anderer einzelliger oder mehrzelliger Organismen.[20] Die natürlichen Wirte sind unbekannt (Stand 2015).[21]
Aufbau
[Bearbeiten | Quelltext bearbeiten]
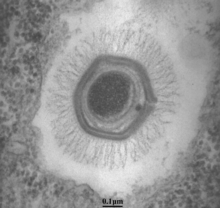
Die Kapside der Virionen (Viruspartikel) von ApMV erscheinen unter einem Elektronenmikroskop sechseckig, daher ist die Kapsidgeometrie ikosaedrisch.[23]
Bei Mimivirus besteht das Hauptkapsidprotein aus zwei Domänen vom Biskuitrollen-Typ (englisch Jelly roll fold). Dieses Protein bildet homotrimere Kapsomere als Organisationseinheit der Kapside. Die Kapsomere sind hexagonal in Form von „Gänseblümchen“ gepackt: Sechs Kapsomere umgeben eine Vertiefung zwischen ihnen.[23][24] Die Virionen (Viruspartikel) von Mimivirus ApMV haben einen Kapsiddurchmesser von 400 nm. Es scheint keine äußere virale Hülle zu geben, was darauf hindeutet, dass das Virus die Wirtszelle nicht durch Exozytose verlässt.[20]
Fibrillen
[Bearbeiten | Quelltext bearbeiten]
B: AFM-Aufnahme von zwei abgelösten Oberflächenfasern eines Mimivirus.
C: Cryo-EM-Bild eines Mimivirus nach teilweisem Abbau der Fibrillen mittels Bromelain.
D: AFM-Bild von inneren Fasern eines Mimivirus.
Das Kapsid des Wildtyps ApMV ist dagegen mit einer kompakten Schicht von Fibrillen bedeckt (Tegument). Die aus der Oberfläche des Kapsids herausragenden Proteinfilamente (Fibrillen) haben eine Länge von etwa 100 nm (80–125 nm) und bringen damit die Gesamtlänge eines Virions auf 600 nm.[5][21] Abweichungen in der wissenschaftlichen Literatur lassen die Zahlen als sehr ungenau erscheinen, wenn zum Beispiel die ‚Größe’ des Virions gelegentlich als irgendwo zwischen 400 und 800 nm angegeben wird. Abgesehen von Unterschieden zwischen den einzelnen Virusstämmen in der Spezies Mimivirus bradfordmassiliense ist manchmal die Gesamtgröße mit Filamenten, und manchmal der reine Kapsiddurchmesser angegeben.
Untersuchungen dieser Filamente von Klose et al. (2010) unter Verwendung eines Rasterkraftmikroskops ergeben, dass diese häufig an einer gemeinsamen Tragstruktur befestigt sind. Im Jahr 2009 konnte jedoch noch nicht herausgefunden werden, an welchen Teilen der Kapsidoberfläche diese Träger befestigt sind.[23] Jede Fibrille endet mit einer kleinen kugeligen Kappe aus einem Protein mit unbekannter Funktion.[21][23] Die Proteinfilamente erwiesen sich als resistent gegen Proteasen, außer sie wurden mit Lysozym behandelt. Die Filamente schienen deshalb mit Peptidoglycan beschichtet zu sein. Das war alles in guter Übereinstimmung mit der Tatsache, dass sich das Mimivirus-Virion durch die Gram-Methode anfärben lässt.[25]
Die Filamente spielen mit ihrer stark glykosylierten Oberfläche offenbar eine wichtige Rolle bei der Annäherung an die Wirtsamöben und der nachfolgenden Infektion.[25][21] Der Hauptbestandteil der Fasern ist das Protein R135 (neben L725 und L829). Seine Struktur ähnelt Proteinen aus der Familie der Glucose-Methanol-Cholin-Oxidoreduktasen (GMC-Oxidoreduktasen), die eine N-terminale FAD-Bindungsdomäne und eine C-terminale Substraterkennungsdomäne aufweisen. Das R135 am nächsten kommende Homolog ist eine Arylalkohol-Oxidase[A. 2], die am biologischen Ligninabbau von Pflanzenzellwänden beteiligt ist. Somit könnte R135 an der Perforation der Zellwand ihrer natürlichen Wirte, insbesondere ligninhaltiger Algen, beteiligt sein.[21] Unter Laborbedingungen ist aber keines der drei genannten Proteine für die Infektiosität unbedingt erforderlich.[21]
Stargate
[Bearbeiten | Quelltext bearbeiten]
Auffällig ist die fünfeckige, sternförmige Struktur an einer der Ecken des Kapsids, das so genannte ‚Stargate‘ (auch star-gate,[26] englisch für „Sternentor“, deutsch auch ‚Sternstruktur‘ oder ‚Seesternstruktur‘ genannt).[27] Blickt man direkt auf diesen Eckpunkt oder Vertex (den Mittelpunkt des Sterns), so scheinen zwischen dessen Strahlen fünf dreieckige Flächen zu liegen. Die Strahlen haben eine Breite von ungefähr 50 nm, eine Dicke von 40 nm und eine Länge von 200 nm; sie erreichen fast die benachbarten Eckpunkte der ikosaedrischen Kapsids. Das Stargate ist selbst nicht von Fibrillen bedeckt.[21] Das Vorhandensein dieser Struktur verändert die Geometrie des Kapsids, die dadurch von der idealen „isometrischen“ Ikosaederform abweicht: Tatsächlich verläuft bei genauer Betrachtung nur eine einzige Achse mit Fünfstrahlsymmetrie durch das Virion, die durch den Mittelpunkt des Sterns (genannt Scheitelpunkt) verläuft.[23][28]
Die Symmetrie des Kapsids wird unterschiedlich angegeben mit einer Triangulationszahl T=972–1141 oder T=1200.[7]
Da auf der Oberfläche der Sternstruktur keine hexagonal geordneten Vertiefungen zu beobachten sind, wird vermutet, dass es sich bei dieser um ein Protein handelt, das sich vom Hauptkapsidprotein unterscheidet.[23]
Das Stargate spielt eine besondere Rolle bei der Infektion der Wirtszelle: Während der Infektion öffnet sich der „Verschluss“ am Scheitelpunkt und es erfolgt die Freisetzung des viralen Kerns (mit DNA und vorgefertigten Proteinen) aus dem Kapsid in das Zytosol der Wirtszelle (per Phagocytose). Das ist der Grund, warum die Sternstruktur als „Sternentor“ (englisch stargate) bezeichnet wird.[29]
Nukleokapsid
[Bearbeiten | Quelltext bearbeiten]Die Gattung Mimivirus hat mehrere morphologische Merkmale mit den Mitgliedern des Phylums Nucleocytoviricota (NCLDV) gemeinsam. Unmittelbar unter dem Kapsid des Mimivirus befinden sich beispielsweise zwei elektronendichte Schichten, die als Membranen gedeutet werden.[25] Unter diesen Membranen befindet sich eine etwa 7 nm dicke Proteinhülle, in der die lineare doppelsträngige DNA (dsDNA) des Virus eingeschlossen ist. Dieser kondensierte Zentralkern des Virions erscheint unter dem Elektronenmikroskop als dunkler Bereich, das sogenannte ‚Nukleokapsid‘. In diesem Bereich befindet sich das große Genom des Virus, daneben auch mRNAs und vorgefertigte Proteine. Da alle anderen NCLDVs eine interne Lipidschicht besitzen, die den zentralen Kern umgibt, vermutet man das auch bei der Gattung Mimivirus. Die Wände des Nukleokapsids liegen etwa 30 nm hinter den Wänden des Kapsids zurück, im Bereich der Sternstruktur (dem Stargate) ist die Oberfläche des Nukleokapsids zusätzlich abgesenkt.[23] Es wird angenommen, dass der Raum zwischen der Spitze der Sternstruktur und dem Nukleokapsid mit hydrolytischen Enzymen gefüllt ist, die für das Eindringen des Virus in die Wirtszelle erforderlich sind. Zwischen dem Kapsid und dem Nukleokapsid wurden interne Proteinstränge entdeckt, die anscheinend die gegenseitige räumliche Positionierung der beiden Teile zueinander stabilisieren.[25]
Genom
[Bearbeiten | Quelltext bearbeiten]Der Referenzstamm Mimivirus bradfordmassiliense ApMV hat damit im Vergleich zu den meisten anderen Viren ein großes und komplexes Genom, das aus einem einzelnen linearen DNA-Doppelstrang (dsDNA) besteht. Die Genomlänge des APMV Wildtyps (Ausgangsvariante Mimivirus M1) wurde von Didier Raoult et al. (2004) mit 1.181.404 bp angegeben,[16] dieser Wert wurde durch Disa Bäckström et al. (2019) leicht korrigiert auf 1.181.594 bp.[30] Das entspricht etwa 800 nm. Die aus diesem Wildtyp gezüchtete fiberlose Variante Acanthamoeba polyphaga mimivirus M4 hat nur 0,993 Mbp, dazwischen liegen M2 mit 1.10 Mbp und M3 mit 1,10 Mbp.[31] Der GC-Gehalt von ApMV liegt bei 28 %. Es gibt bei ApMV 1260 Offene Leserahmen (ORFs, englisch open reading frames),[16] darunter vorhergesagt 979 kodierende Gene.[30][21][32] Dies geht weit über die Mindestausstattung von 4 Genen hinaus, die für ein Virus erforderlich sind (wie etwa bei den Phagen MS2 und Qβ).[33] Detaillierte Studien zum Genom korrigieren immer wieder Sequenzfehler und entdecken unter Umständen neue Leserahmen.[34]
Der Anteil von nichtcodierender DNA beträgt damit bei ApMV nur etwa 9,5 bis 10 %. Offene Leserahmen sind durch Lücken von ungefähr 157 Nukleotidpaaren getrennt. Zwei DNA-Abschnitte mit der Bezeichnung R (englisch right – rechts) und L (englisch left – links) kodieren ungefähr die gleiche Anzahl von Genen (450 bzw. 465, gemäß Daten von 2010). Der GC-Gehalt ist mit 28 % niedrig. In der Nähe der Enden des DNA-Moleküls wurden ‚Invertierte Wiederholungen‘ (englisch inverted repeats) mit 617 Nukleotidpaaren gefunden. Es wird vermutet, dass die gegenseitige Wechselwirkung dieser Stellen zur Bildung einer Q-Struktur führen kann – zirkuläre DNA mit zwei kleinen Fortsätzen.[34]
Bei der Analyse stieß man auf mindestens 21 Gene mit Homologie zu bekannten Proteinen, darunter solche, die man bis dato von keinem anderen Virus, sondern nur von zellulären Organismen kannte, inklusive Aminoacyl-tRNA-Synthetase.[16][14][35] 43 Gene sind homolog zu solchen anderer Riesenviren (NCLDVs).[21] Wie andere Riesenviren enthält Mimivirus mehrere Gene für den Zucker-, Lipid- und Aminosäurestoffwechsel. Es gab auch Stoffwechselgene, die zuvor in keinem anderen Virus gefunden wurden.[20]
Aus gereinigten Virionen konnten mehrere mRNA-Transkripte gewonnen werden. Wie schon bei anderen Nucleocytoviricota (NCLDVs) wurden insbesondere Transkripte für DNA-Polymerase, ein Kapsidprotein und ein TFII-ähnlicher Transkriptionsfaktor gefunden werden. Es wurden jedoch auch drei verschiedene Aminoacyl-tRNA-Synthetase-Transkripte und vier unbekannte mRNA-Moleküle gefunden, die für Mimivirus spezifisch sind. Diese vorverpackten Transkripte können ohne virale Genexpression translatiert werden und sind wahrscheinlich für die Replikation von Mimivirus erforderlich. Andere DNA-Viren, wie das Humane Cytomegalievirus und das Herpes-simplex-Virus Typ 1, enthalten ebenfalls gepackte mRNA-Transkripte.[20]
Mimivirus ist eines der wenigen dsDNA-Viren, in deren Genom eine Intein-kodierende Sequenz nachgewiesen wurde. Inteine sind Proteindomänen, die ihre eigene Entfernung von einem Trägermolekül und die anschließende Verknüpfung der gebildeten Enden katalysieren. Eine solche Sequenz ist im Mimivirus-Gen für DNA-Polymerase B vorhanden.[36]
Auf Grund der außergewöhnlich komplexen genetischen Ausstattung des Virus sehen einige Wissenschaftler die Frage neu gestellt, wo die Grenze zwischen belebter und unbelebter Natur verlaufe, also wie „Lebewesen“ zu definieren ist.
Replikationszyklus
[Bearbeiten | Quelltext bearbeiten]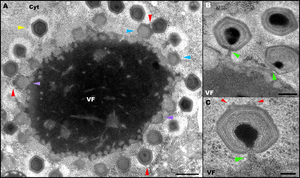
A) TEM-Aufnahme einer intrazellulären Virusfabrik, mit Viruspartikeln (Virionen) von Mimivirus in verschiedenen Montagestadien
- VF: Virusfabrik (Viroplasma)
- Cyt: Zytoplasma
- violette Pfeile: leere, noch faserlose Virionen im Anfangsstadium der Zusammensetzung, in unmittelbarer Nähe zur Peripherie der Virusfabrik auftretend
- blaue Pfeile: Teilweise montierte leere, faserlose Virionen
- gelbe Pfeile: reife, faserbedeckte Virionen, die sich jetzt weiter von der Virusfabrik entfernt befinden als die unreifen Partikel
- rote Pfeile: bei mehreren Viruspartikeln ist ein ‚Stargate’, das sich regelmäßig an der distalen Stelle der Fabrik befindet, zu erkennen
B) und C) TEM-Aufnahme der Mimivirus-Partikel
- grüne Pfeile: Mimivirus-Partikel im Stadium des ‚DNA-Packaging’ (DNA-Verpackung)
- rote Pfeile: zwei Kanten eines Stargates gegenüber der Stelle der DNA-Verpackung

Die Einzelheiten und die verschiedenen Stadien im Replikationszyklus von Mimivirus, wie die offensichtliche Bindung an die Zelloberfläche und den Eintritt in die Zelle, die Freisetzung des Viruskerns, die DNA-Replikation, die Transkription, die Translation, und schließlich den Zusammenbau und die Freisetzung von Tochter-Virionen, sind noch nicht ausreichend bekannt (Stand 2010). Die Wissenschaftler haben jedoch den oben angegebenen allgemeinen Überblick anhand elektronenmikroskopischer Aufnahmen infizierter Zellen erstellt. Alle Stadien des Vermehrungszyklus verlaufen im Zytoplasma der Wirtszelle.[37]
Die Infektion der Amöbe mit einem Mimivirus erfolgt vermutlich nach folgendem Szenario:
- Die Mimivirus-Virionen ähneln in ihrer Größe und dem Vorhandensein charakteristischer Polysaccharide auf der Oberfläche Bakterien (siehe Gram-Färbung, Name). Sie werden daher von der Amöbe als Nahrung während eines Endozytoseprozesses absorbiert. Die Polysaccharide fungieren dabei als chemischer Rezeptor und leiten die Anlagerung ein. Als Ergebnis der Endozytose befinden sich die Virionen in Endosomen innerhalb der Zelle.
- Die Proteinfilamente werden in den Endosomen teilweise lysiert, wodurch das Kapsid mit der Endosomenmembran in Wechselwirkung treten kann.
- Etwa 2 Stunden nach der Infektion: Das Kapsid öffnet sich im Bereich der Sternstruktur (Stargate), die innere Membran fusioniert mit der Endosomenmembran und der Inhalt des Kapsids wird in das Zytoplasma freigesetzt.
- Nachdem das Kernteilchen (der innere Teil des Nukleokapsids) ins Zytoplasma ausgetreten ist, beginnt aufgrund der Anwesenheit des viralen Transkriptionsapparats die Synthese der viralen mRNA. Diese mRNAs reichern sich im Inneren des Kernpartikels in Form von Granula an.[37] Äußerlich betrachtet scheint das Virus verschwunden und alles in der Zelle sieht normal aus (Dunkelphase, englisch eclipse phase).
- 4–5 Stunden nach der Infektion: Die virale DNA verlässt das Kernteilchen und wird entpackt, so dass die Replikation beginnen kann. Infolgedessen entsteht neben der leeren Hülle des Kernpartikels eine sogenannte „Virusfabrik“ – ein Ort für die Synthese der einzelnen Komponenten der Virionen und ihren anschließenden Zusammenbau. Wenn mehrere Viruspartikel in die Zelle gelangt sind, verschmelzen die von ihnen gebildeten „Fabriken“ beim Wachstum zu einer einzigen. Man erkennt jetzt kleine Ansammlungen in einigen Bereichen der Zelle.
- 6–9 Stunden nach der Infektion: Zusammensetzung (Assemblierung) der Kapside mit gleichzeitiger DNA-Packung an der Peripherie der Virusfabriken. Eine ungewöhnliche Eigenschaft von Mimivirus ist, dass DNA gepackt ist.[29] Ein merkwürdiges Phänomen bei der Gattung Mimivirus ist dabei, dass nach der Bildung des vollständigen Kapsids das Genom durch das dem Stargate gegenüberliegende Eckportal in das Kapsid gelangt und dann im Inneren sich verdichtet (kondensiert), woraufhin dieses Eintrittsportal versiegelt wird.[38] Die Mimivirus-Virionen werden in der Zelle deutlich sichtbar.
- 14–24 Stunden nach der Infektion: Die Amöbenzellen werden lysiert, d. h. sie platzen auf und die Virionen werden freigesetzt. Pro Wirtszelle werden so mehr als 300 Einheiten erzeugt.[34][20]
Zusammenbau des Kapsids und die Einlagerung des Genoms erfolgen also nacheinander in einer ganz bestimmten Reihenfolge.[38]
Die Übertragung geschieht durch passive Diffusion.[7]
Mögliche Pathogenität
[Bearbeiten | Quelltext bearbeiten]Es wurde spekuliert, dass Vertreter der Gattung Mimivirus (oder naher Verwandter) Erreger bestimmter Formen von Lungenentzündung (Pneumonia) sein könnte. Dies beruht hauptsächlich auf indirekten Nachweisen in Form von Antikörpern gegen das bei Lungenentzündungspatienten entdeckte Virus.[39] Aufgrund der wenigen bisherigen Veröffentlichungen ist die Einstufung von Mimivirus als möglicher Krankheitserreger derzeit jedoch schwierig. Ein großer Teil der Fälle von Lungenentzündung verläuft ohne feststellbare Ursache.[40] Zwar wurde das Virus bei einer an Lungenentzündung leidenden Tunesierin isoliert,[41] und es gibt aus Zellkulturen Hinweise darauf, dass Mimivirus-Arten Makrophagen infizieren können und darin repliziert werden.[42] So wurde unter experimentellen Bedingungen beobachtet, dass Mimivirus-Arten humane Makrophagen infizieren können, d. h. via Phagocytose in die Zellen eindringen, und sich dort replizieren können.[43][42] Außerdem wurden in mehreren Studien bei einer kleinen Anzahl von Patienten mit Lungenentzündung Antikörper gegen das Mimivirus gefunden.[39][44] Es wurde auch ein Einzelfall einer Lungenentzündung eines Laborassistenten beschrieben, der mit Kulturen dieses Virus arbeitete. Der Gehalt an Antikörpern gegen Mimivirus in seinem Blut war ebenfalls erhöht.[45] Das Vorhandensein von Antikörpern gegen das Virus an sich ist jedoch kein Hinweis auf seine Pathogenität. Es ist möglich, dass das Mimivirus-Arten nur einfach starke immunogene Eigenschaften aufweist, d. h. eine deutliche Immunantwort auslöst.[34] Auch war es in keinem der registrierten Fälle möglich, das Virus in seiner reinen Form aus Proben von Flüssigkeiten zu isolieren, die von Patienten erhalten wurden.[46]
Die Fiberproteine R135 und L829 wurden als Hauptantigene des Mimivirus identifiziert: Die faserlose Variante Mimivirus M4 zeigte jedoch keine Reaktivität mit Seren von menschlichen Patienten, was bestätigt, dass diese Proteine in M4 fehlen.[21]
Resistenzeigenschaft
[Bearbeiten | Quelltext bearbeiten]Das Zamilon-Virus ist ein Satellitenvirus, das Mimiviridae der Linien B (Moumouvirus) und C (Megavirus) befällt, nicht aber die Mimiviridae der Linie A (Mimivirus). Diese weisen nämlich eine MIMIVIRE, englisch mimivirus virophage resistance element, genannte Resistenz auf, die ähnlich funktioniert wie das CRISPR/Cas-System.[47][48]
Im Übrigen wurde nachgewiesen, dass es nicht nur einen horizontalen Gentransfer zwischen den amöboid Wirten und Riesenviren als intrazellulären viralen Endocytobionten (Organismen, die in den Zellen anderer Organismen leben oder sich vermehren) gibt,[49] sondern sogar zwischen den Viren und gleichzeitig vorhandenen bakteriellen Endocytobionten.[50][31][A. 3]
Systematik
[Bearbeiten | Quelltext bearbeiten]Die Gattung Mimivirus und einige andere vom ICTV im April 2023 bestätigte genetisch ähnliche Gattungen und Spezies der Familie Mimiviridae, wie Megavirus, Moumouvirus, Tupanvirus und Cotonvirus eine als Gruppe I bezeichnete Klade (Unterfamilie Megamimivirinae inklusive Mimivirus).[6][1][2]
Entgegen dem Vorschlägen von Aylward et al. (2021)[1] und Schulz et al. (2018)[2] hat das ICTV im April 2023 die Gattung Mimivirus selbst nicht in die Unterfamilie Megamimivirinae aufgenommen (obwohl die Phylogenie nach Aylward et al. dafür spricht),[1] sondern ohne Unterfamilienzuordnung in den Mimiviridae belassen. Der Name „Megavirinae“[51] (nach der Gattung Megavirus) ist damit ein veraltetes Synonym für Megamimivirinae. Eine eigene Unterfamilie für die Gattung Mimivirus, etwa „Mimivirinae“,[52] bleibt zunächst nicht ausgeschlossen.
Die folgende Systematik basiert auf der Master Species List #38 des International Committee on Taxonomy of Viruses (ICTV)[6][1] vom 8. April 2023, ergänzt um eine Reihe in diesem Release (noch) nicht offiziell anerkannter Vorschläge, insbesondere nach den NCBI-Taxonomie (die den ersten Fund beinhaltenden Gruppen sind fett wiedergegeben):




Familie Mimiviridae
- Klade (ehemals „Aquavirinae“, „Aquaviren“)[55][51]
- Unterfamilie Aliimimivirinae (Mimiviridae-Gruppe II)
- Gattung Rheavirus (früher Cafeteriavirus)
- Unterfamilie Klosneuvirinae (Klosneuviren)
- Gattungen Fadolivirus, Theiavirus (mit BsV), Yasminevirus
- Unterfamilie Aliimimivirinae (Mimiviridae-Gruppe II)
- Unterfamilie Megamimivirinae (Mimiviridae-Gruppe I)
- Gattung Mimivirus (Linie A, veraltetes Synonym: Bradfordcoccus)
- Spezies Mimivirus bradfordmassiliense (Acanthamoeba-polyphaga-Mimivirus, en. Acanthamoeba polyphaga mimivirus, ApMV oder APMV) mit den Stämmen bzw. Isolaten
- Acanthamoeba polyphaga mimivirusT (Referenzstamm)
- Acanthamoeba polyphaga mimivirus Oyster (OYTV),[58][5][A. 7]
- Acanthamoeba polyphaga mimivirus strain Amazonia (alias Mimivirus amazonia, Amazonia-Virus, AMAV, en. „Amazonian virus“),[59][58][60][5][58][61][5][A. 8]
- Acanthamoeba polyphaga mimivirus ViralProj60053,
- Mimivirus terra2 (alias Terravirus 2 oder Terra2-Virus),[62][63][61][5][A. 9] – vgl. Terravirus2 TAO-TJA[64]
- Mimivirus Bombay isolate 1 (MVB, alias Bombay-Virus),[56][5][61][65][66][67][A. 10]
- Hirudovirus strain Sangsue,[68][69][66][5][A. 11]
- Niemeyer virus (NYMV)[53][54][70][71][5][A. 12]
- Samba virus (SMBV),[56][59][72][5][73][61][A. 13]
- Acanthamoeba castellanii mimivirus kasaii (alias Mimivirus kasaii oder Kasaii-Virus),[5][74][66][A. 14]
- Acanthamoeba castellanii mimivirus shirakomae (alias Mimivirus shirakomae, Shirakomae-Virus),[66][5][74][A. 15]
- Acanthamoeba castellanii mamavirus Hal-V (kurz AcMV, AMaV oder ACMaV),[75][76][77][5][A. 16]
- „Acanthamoeba castellanii mamavirus MAMA_R546“,[78][A. 17]
- Spezies Mimivirus lagoaense mit dem Stamm
- Spezies „Mimivirus argentum“[81][82]
- Spezies „Mimivirus battle6“[83][61]
- Spezies „Mimivirus battle7“[84][61]
- Spezies „Mimivirus battle19“[85][61]
- Spezies „Mimivirus battle27“[86][61]
- Spezies „Mimivirus battle57“[87][61]
- Spezies „Mimivirus battle66“[88][61]
- Spezies „Mimivirus battle83“[89][61]
- Spezies „Mimivirus battle86“[90][64]
- Spezies „Mimivirus Cher“ (alias „Mimiviridae Cher“)[91][64]
- Spezies „Mimivirus fauteuil“ (alias „Fauteuil-Virus“)[92][63][5][61] – mit Fauteuil virus FD[93]
- Spezies „Mimivirus dakar4“[94][61]
- Spezies „Mimivirus huitre A06“[95][61]
- Spezies „Mimivirus lentille“ (alias „Lentille-Virus“, „Acanthamoeba polyphaga lentillevirus“)[96][63][61][76] – vgl. Lentille virus CL[97]
- Spezies „Mimivirus lactour“ (alias Lactours-Virus oder „Mimiviridae Lactours“).[61][98][63] – vgl. Lactours virus LT2[99]
- Spezies „Mimivirus longchamps“ (alias „Longchamps-Virus“ oder „Mimiviridae Longchamps“)[100][63][5][61] – vgl. Longchamps virus FPL[101]
- Spezies „Mimivirus marais“ (alias „Marais-Virus“)[102][63][61]
- Spezies „Mimivirus montadette2“[103][64]
- Spezies „Mimivirus pointerouge1“ (alias „Mimiviridae Pointerouge1“)[104] – vgl. Pointerouge virus 1[105][5][61][5][A. 19]
- Spezies „Mimivirus pointerouge2“ (alias „Mimiviridae Pointerouge2“)[106] – vgl. Pointerouge virus 2 (alias Pointe-Rouge 2 virus)[107][5][61][5][A. 20]
- Spezies Mimivirus SR1 (alias „Mimivirus-like virus SR1“)[108][A. 21]
- Spezies Mimivirus SR4 (alias „Mimivirus-like virus SR4“)[109][A. 22]
- Spezies „Mimivirus SR9“ (alias „Mimivirus-like virus SR9“)[110][A. 23]
- Spezies „Mimivirus sp. styx“[111][A. 24]
- Spezies „Mimivirus T2“[112][61]
- Spezies „Mimivirus T3“[113][61]
- Spezies „Mimivirus univirus“[114][64]
- Spezies Mimivirus bradfordmassiliense (Acanthamoeba-polyphaga-Mimivirus, en. Acanthamoeba polyphaga mimivirus, ApMV oder APMV) mit den Stämmen bzw. Isolaten
- Gattungen Moumouvirus (Linie B), Megavirus (Linie C), Tupanvirus, Cotonvirus, „Platanovirus“, „Satyrvirus“[2]
- Gattung Mimivirus (Linie A, veraltetes Synonym: Bradfordcoccus)
Anm.:
- Bei den Spezies (bzw. Stämmen) der drei Gattungen Mimivirus, Moumouvirus und Megavirus kann zur Unterscheidung dem abgekürzten Gattungsnamen der tiefer gestellte Buchstabe der jeweiligen Linie (A, B bzw. C) beigefügt werden: MA. für Mimivirus, MB für Moumouvirus und MC für Megavirus.[115]
- T – bei Namensgleichheit mit der Spezies deutet ein hochgestelltes ‚T‘ einen Typus- oder Referenzstamm an.
- Die hier genannten Vorschläge können (nach Reorganisation der Ordnung Imitervirales) durch das ICTV auch in andere Gattungen, Unterfamilien oder Familien dieser Ordnung zu klassifizieren sein. Die Bezeichnung als Mimivirus wurde in der Vergangenheit teilweise in einem sehr weiten Sinn verstanden und kann sich im äußersten Fall einfach nur auf eine Zugehörigkeit zu dieser Ordnung beziehen.[A. 1]
Die genauen Verwandtschaftsverhältnisse sind aber möglicherweise noch in der Diskussion, nach Schulz et al. (2018) steht z. B. die Linie A (Gattung Mimivirus) basal in der Gruppe I, nicht die Tupanviren (Gattung Tupanvirus).[2]
Kladogramm
[Bearbeiten | Quelltext bearbeiten]Die Phylogenie der Mimiviridae-Gruppe I, d. h. der Unterfamilie Megamimivirinae inkl. der Gattung Mimivirus * (Mimiviren s. l.) ist nach Aylward et al. (2021), ergänzt um Abrahão et al. (2018, Fig. 4) wie folgt:[1][116]
| Mimiviridae-Gruppe I |
| ||||||||||||||||||||||||||||||||||||
Im Jahr 2018 hatten Abrahão et al. zuvor einen phylogenetischen Baum der Mimiviridae-Gruppe I angegeben, der einige weitere Stämme umfasst:[116]
| Mimiviridae-Gruppe I |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Da nach den neueren Angaben von Aylward et al. (2021) das Kroon-Virus zur Spezies Mimivirus lagoaense, Acanthamoeba polyphaga mimivirus und Niemeyer-Virus aber zur Spezies Mimivirus bradfordmassiliense gehören,[1] erscheint letztere in der hier zugrundeliegenden älteren Phylogenie nicht monophyletisch.
Anmerkungen
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Beispiele sind „Mimivirus LCMiAC01“[10] und „Mimivirus LCMiAC02“[11] (Klosneuvirinae), sowie „gvSAG AB-566-O17“[12] alias „Mimivirus AB-566-O17“[13] (basal in Mimiviridae oder Schwesterklade) – siehe Imitervirales §Systematik
- ↑ siehe auch Vanillylalkohol-Oxidase
- ↑ Eine Homologie zwischen CRISPR und MIMIVIRE scheint damit nicht unmöglich, bedarf aber sicher weiterer Untersuchungen.
- ↑ natürliche Ursprungsvariante
- ↑ a b M2 und M3 sind Zwischenformen zwischen M1 und M4 mit kürzeren Fibrillen als der Wildtyp (M1)
- ↑ M4 ist die fiberlose Variante, wird nach Boyer et al. (2011) nicht vom Sputnik-Virophagen befallen.
- ↑ Fundort der OYTVs: in Austern, Florianópolis, Brasilien. Laut Assis et al. (2015) gibt es dort aber eine ganze Reihe von in Austern gefundenen Mimiviren: OY SC7, OY SC9, OY RN35, OY SC3, OY RN33, OY RN27, OY SC1, OY RN40, OY RN30, OY BA28, OY SC5, OY RN29, OY BA23, OY SC6, OY SC2 und OY BA29.[59]
- ↑ Fundort: Rio Negro, Brasilien
- ↑ Fundort: Marseille, Frankreich
- ↑ Fundort: Mumbai, Indien
- ↑ Fundort: In einem Medizinischen Blutegel (Hirudo medicinalis), Tunesien.
- ↑ Fundort: Pampulha-See, Belo Horizonte, Brasilien, benannt zu Ehren des Architekten Oscar Niemeyer, der am Ufer des Sees die Kirche des Heiligen Franz von Assisi entworfen hat.
- ↑ Fundort: Rio Negro, Brasilien
- ↑ Fundort: Arakawa (Fluss), Tokio, Japan
- ↑ Fundort: Shirakoma Pond, Nagano, Japan. Infiziert nach Takemura et al. (2016) Acanthamoeba castellanii und A. culbertsoni, nicht aber A. comandoni oder Vermamoeba vermiformis.
- ↑ Fundort: Paris, Frankreich.
- ↑ Fundort: Wasser aus einem Kühlturm, Les Halles, Paris, Frankreich
- ↑ Fundort nach NCBI Nucleotide: Städtischer See in Lagoa Santa, Minas Gerais, Brasilien.
- ↑ Fundort: Marseille, Frankreich.
- ↑ Fundort: Marseille, Frankreich.
- ↑ Fundort: Serendah village, Malaiische Halbinsel – Wasserfallref name="TYF2018"/>
- ↑ Fundort: Serendah village, Malaiische Halbinsel – Mitte zw. Wasserfall und Dorf[77]
- ↑ Fundort: Serendah village, Malaiische Halbinsel – Mündung des Zuflusses in den See[77]
- ↑ Fundort: Boden an einem Ufer des Flusses Arakawa bei der gleichnamigen Bahnbrücke im Osten von Tokyo, Japan (Motohiro Akashi und Masaharu Takemura).
Literatur
[Bearbeiten | Quelltext bearbeiten]- Stefanie Reinberger: Revolution der Riesenviren. In: Spektrum der Wissenschaft. Spektrum der Wissenschaft Verlagsgesellschaft, Heidelberg 2012, S. 14–16.
- Graziele Oliveira, Bernard La Scola, Jônatas Abrahão: Giant virus vs amoeba: fight for supremacy. In: Virol J, 16, 126, 4. November 2019, doi:10.1186/s12985-019-1244-3, researchgate.net (PDF)
- Ana Cláudia dos S. P. Andrade, Thalita S. Arantes, Rodrigo A. L. Rodrigues, Talita B. Machado, Fábio P. Dornas, Melissa F. Landell, Cinthia Furst, Luiz G. A. Borges, Lara A. L. Dutra, Gabriel Almeida, Giliane de S. Trindade, Ivan Bergier, Walter Abrahão, Iara A. Borges, Juliana R. Cortines, Danilo B. de Oliveira, Erna G. Kroon, Jônatas S. Abrahão: Ubiquitous giants: a plethora of giant viruses found in Brazil and Antarctica. In: Virology Journal, Band 15, Nr. 22, 24. Januar 2018, doi:10.1186/s12985-018-0930-x
- Philippe Colson, Bernard La Scola, Anthony Levasseur, Gustavo Caetano-Anollés,& Didier Raoult: Mimivirus: leading the way in the discovery of giant viruses of amoebae. In: Nature Reviews Microbiology, Band 15, S. 243–254, 27. Februar 2017, doi:10.1038/nrmicro.2016.197
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Jean-Michel Claverie (Hrsg.): Bilder des Mimivirus. Structural & Genomic Information Laboratory CNRS UPR, Marseille
- Referenzsequenz NC_006450. NCBI
- David R. Wessner: Discovery of the Giant Mimivirus. Nature Masterclasses
- Scinexx: Riesenviren an der Grenze zum Leben, vom 28. Februar 2018
- Andreas Jahn: Das Virus-Virus, auf: Spektrum.de vom 6. August 2008
- Biologie Seite: Mimivirus
- Iddo: Size matters. Life is live., auf: Byte Size Biology, Blog vom 1. Mai 2009, mit Bild vom sich öffnenden Stargate, identisch mit Zaubermann et al. (2008), Fig. 5.[29]
- Adrian De Novato: New study shines light on mysterious giant viruses. phys.org, 8. Mai 2020 (die Abbildung zeigt offenbar einen typischen Vertreter der Gattung Mimivirus mit Stargate (Öffnung für DNA) und Tegument (Hülle aus Fibrillen).
- Nicoletta Lanese: Giant viruses spew their DNA through a ‘stargate’. Now, scientists know what triggers them. LiveScience, 26. Mai 2020
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j
Frank O. Aylward, Jônatas S. Abrahão, Corina P. D. Brussaard C, Matthias G. Fischer, Mohammad Moniruzzaman, Hiroyuki Ogata, Curtis A. Suttle: Create 3 new families, 3 subfamilies, 13 genera, and 20 new species within the order Imitervirales (phylum Nucleocytoviricota) and rename two existing species (zip:docx). Vorschlag 2022.004F an das ICTV vom Oktober 2021.
Anm.: Entgegen Vorschlag (Tbl. 1) wurde die Gattung Mimivirus nicht in die Unterfamilie Megamimivirinae aufgenommen. Phylogenetische Analysen zeigten zu deren Mitgliedern einen größeren Abstand als diese untereinander. - ↑ a b c d e f Frederik Schulz, Lauren Alteio, Danielle Goudeau, Elizabeth M. Ryan, Feiqiao B. Yu, Rex R. Malmstrom, Jeffrey Blanchard, Tanja Woyke: Hidden diversity of soil giant viruses. In: Nature Communications. volume 9, Article number: 4881 (2018), 19. November 2018, doi:10.1038/s41467-018-07335-2
- ↑ a b ICTV Taxon Details: Genus: Mimivirus.
- ↑ a b c d e ICTV: ICTV Taxonomy history: Acanthamoeba polyphaga mimivirus, EC 51, Berlin, Germany, July 2019; Email ratification March 2020 (MSL #35).
- ↑ a b c d e f g h i j k l m n o p q r s t u v Jan Diesend, Janis Kruse, Monica Hagedorn, Christian Hammann: Amoebae, Giant Viruses, and Virophages Make Up a Complex, Multilayered Threesome, in: Frontiers in Cellular and Infection Microbiology 7, Januar 2018, doi:10.3389/fcimb.2017.00527, via ResearchGate, Fig. 1 (NCLDVs und ‚Megavirales‘ werden in dieser Arbeit nicht ganz korrekt als ‚Familien‘ bezeichnet, gemeint sind ‚Gruppen‘).
- ↑ a b c d e ICTV: Master Species Lists § ICTV Master Species List 2022 MSL38 v1 (xlsx), 8. April 2023.
- ↑ a b c ViralZone: Mimivirus. Expasy, abgerufen am 8. Juli 2019 (englisch).
- ↑ ICTV: Master Species List 2018b.v2. Abgerufen am 6. August 2019 (englisch). MSL #34v.
- ↑ NCBI Taxonomy Browser: Mimivirus LCMiAC01 (species). Nucleotide: MAG: Mimivirus LCMiAC01….
- ↑ NCBI Taxonomy Browser: Mimivirus LCMiAC02 (species). Nucleotide: MAG: Mimivirus LCMiAC02….
- ↑ William H. Wilson, Ilana C. Gilg, Mohammad Moniruzzaman, Erin K. Field, Sergey Koren, Gary R. LeCleir, Joaquín Martínez Martínez, Nicole J. Poulton, Brandon K. Swan, Ramunas Stepanauskas, Steven W. Wilhelm: Genomic exploration of individual giant ocean viruses. In: ISME Journal, 11(8), August 2017, S. 1736–1745, doi:10.1038/ismej.2017.61, PMC 5520044 (freier Volltext), PMID 28498373, nature, PDF (746 kB) Associated Data (Supplements): Supplementary Dataset 1 (gvSAG AB-572-A11), Fig. 2 (gvSAG AB-566-O17).
- ↑ NCBI Taxonomy Browser: Mimivirus AB-566-O17 (Acronym: gvSAG AB-566-O17, gvSAG_O17) (species).
- ↑ a b Bernard La Scola, S. Audic, Catherine Robert, L. Jungang, X. de Lamballerie, M. Drancourt, R. Birtles, Jean-Michel Claverie, Didier Raoult: A giant virus in amoebae. In: Science. 299, 2003, S. 2033. PMID 12663918
- ↑ Laurie O’Keefe: Sizing Up Viruses. (PDF; 103 kB) The Scientist. Illustration zu Didier Raoult: Viruses Reconsidered, ebenda vom 28. Februar 2014.
- ↑ a b c d Didier Raoult, S. Audic, Catherine Abergel, P. Renesto, H. Ogata, Bernard La Scola, M. Suzan, Jean-Michel Claverie: The 1.2-megabase genome sequence of Mimivirus. In: Science. 306(5700), 19. November 2004, S. 1344–1350, doi:10.1126/science.1101485. PMID 15486256
- ↑ Amina Cherif Louazani, Sarah Aherfi, Rania Francis, Rodrigo Rodrigues, Ludmila Santos Silva, Dehia Sahmi, Said Mougari, Nisrine Chelkha, Meriem Bekliz, Lorena Silva, Felipe Assis, Fábio Dornas, Jacques Yaacoub Bou Khalil, Isabelle Pagnier, Christelle Desnues, Anthony Levasseur, Philippe Colson, Jônatas Abrahão, Bernard La Scola: Discovery and Further Studies on Giant Viruses at the IHU Mediterranee Infection That Modified the Perception of the Virosphere. In: Viruses, Band 11, Nr. 4, März/April 2019, pii: E312; doi:10.3390/v11040312, PMC 6520786 (freier Volltext), PMID 30935049.
- ↑ H. Pearson: 'Virophage' suggests viruses are alive. In: Nature. Band 454, Nr. 7205, 2008, S. 677–677, doi:10.1038/454677a, bibcode:2008Natur.454..677P.
- ↑ World's biggest virus found in sea off Chile. A virus found in the sea off Chile is the biggest in the world, harbouring more than 1,000 genes. In: The Telegraph, 11. Oktober 2011. Memento im Webarchiv vom 7. Oktober 2019.
- ↑ a b c d e M. Suzan-Monti, B. La Scola, D. Raoult: Genomic and evolutionary aspects of Mimivirus. In: Virus Research. Band 117, Nr. 1, April 2006, S. 145–155, doi:10.1016/j.virusres.2005.07.011, PMID 16181700.
- ↑ a b c d e f g h i j k Thomas Klose, Dominik A. Herbst, Hanyu Zhu, Joann P. Max, Hilkka I. Kenttämaa, Michael G. Rossmann: A Mimivirus Enzyme that Participates in Viral Entry, in: Structure Band 23, Nr. 6, 2. Juni 2015, S. 1058–1065, doi:10.1016/j.str.2015.03.023
- ↑ a b c ICTV: Mimiviridae – Figures. In: ICTV 9th Report (2011).
- ↑ a b c d e f g h Xiao C., Kuznetsov Y. G., Sun S., Hafenstein S. L., Kostyuchenko V. A., Chipman P. R., Suzan-Monti M., Raoult D., McPherson A., Rossmann M. G.: Structural studies of the giant mimivirus. In: PLoS Biol. Band 7, Nr. 4, 2009, S. e92, doi:10.1371/journal.pbio.1000092, PMID 19402750, PMC 2671561 (freier Volltext).
- ↑ Jean-Michel Claverie, Chantal Abergel, Hiroyuki Ogata: Mimivirus. In: Curr Top Microbiol Immunol. Band 328, 2009, S. 89–121, doi:10.1007/978-3-540-68618-7_3, PMID 19216436.
- ↑ a b c d Thomas Klose, Y. G. Kuznetsov, C. Xiao, S. Sun, A. McPherson, M. G. Rossmann: The three-dimensional structure of Mimivirus. In: Intervirology. Band 53, Nr. 5, 2010, S. 268–273, doi:10.1159/000312911, PMID 20551678, PMC 2895761 (freier Volltext).
- ↑ Chuan Xiao, Matthias G. Fischer, Duer M. Bolotaulo, Nancy Ulloa-Rondeau, Gustavo A. Avila & Curtis A. Suttle: Cryo-EM reconstruction of the Cafeteria roenbergensis virus capsid suggests novel assembly pathway for giant viruses. In: Nature Scientific Reports, Band 7, Nr. 5484, 14. Juli 2017, doi:10.1038/s41598-017-05824-w.
- ↑ James L. van Etten: Giant Viruses. In: American Scientist, Band 99, Nr. 4, Juli/August 2011, S. 304; doi:10.1511/2011.91.304. Siehe insbes. Fig. 3.
- ↑ In der Physik ist dieses geometrische Prinzip als Symmetriebrechung (Brechung einer diskreten Symmetrie) bekannt.
- ↑ a b c d Autor=Nathan Zauberman, Y. Mutsafi, D. B. Halevy, E. Shimoni, E. Klein, C. Xiao, S. Sun, A. Minsky: Distinct DNA exit and packaging portals in the virus Acanthamoeba polyphaga mimivirus. In: PLoS Biol. Band 6, Nr. 5, 2008, S. e114, doi:10.1371/journal.pbio.0060114, PMID 18479185, PMC 2430901 (freier Volltext).
- ↑ a b Disa Bäckström, Natalya Yutin, Steffen L. Jørgensen, Jennah Dharamshi, Felix Homa, Katarzyna Zaremba-Niedwiedzka, Anja Spang, Yuri I. Wolf, Eugene V. Koonin, Thijs J. G. Ettema; Richard P. Novick (Hrsg.): Virus Genomes from Deep Sea Sediments Expand the Ocean Megavirome and Support Independent Origins of Viral Gigantism. in: mBio Vol. 10, Nr. 2, März–April 2019, S. e02497–e18, doi:10.1128/mBio.02497-18, PMC 6401483 (freier Volltext). PMID 30837339.
- ↑ a b c d e f Mickaël Boyer, Saïd Azza, Lina Barrassi, Thomas Klose, A. Campocasso, I. Pagnier, G. Fournous, A. Borg, C. Robert, X. Zhang, C. Desnues, B. Henrissat, M. G. Rossmann, B. La Scola, D. Raoult: Mimivirus shows dramatic genome reduction after intraamoebal culture. in: Proc Natl Acad Sci (PNAS) USA 108(25), 21. Juni 2011, S. 10296–10301, doi:10.1073/pnas.1101118108, PMID 21646533, PMC 3121840 (freier Volltext).
- ↑ David M. Needham, Susumu Yoshizawa, Toshiaki Hosaka, Camille Poirier, Chang Jae Choi, Elisabeth Hehenberger, Nicholas A. T. Irwin, Susanne Wilken, Cheuk-Man Yung, Charles Bachy, Rika Kurihara, Yu Nakajima, Keiichi Kojima, Tomomi Kimura-Someya, Guy Leonard, Rex R. Malmstrom, Daniel R. Mende, Daniel K. Olson, Yuki Sudo, Sebastian Sudek, Thomas A. Richards, Edward F. DeLong, Patrick J. Keeling, Alyson E. Santoro, Mikako Shirouzu, Wataru Iwasaki, Alexandra Z. Worden: A distinct lineage of giant viruses brings a rhodopsin photosystem to unicellular marine predators. In: PNAS, 23. September 2019, ISSN 0027-8424; doi:10.1073/pnas.1907517116, inklusive Supplement 1 (xlsx).
- ↑ Lansing M. Prescott: Microbiology. Wm. C. Brown Publishers, Dubuque, IA 1993, ISBN 0-697-01372-3.
- ↑ a b c d Jean-Michel Claverie, Chantal Abergel: Mimivirus and its virophage. In: Annu Rev Genet. Band 43, Nr. 49–66, 2009, doi:10.1146/annurev-genet-102108-134255, PMID 19653859.
- ↑ Jean-Michel Claverie, Hiroyuki Ogata, Stéphane Audic, Chantal Abergel, Pierre-Edouard Fournier, Karsten Suhre: Mimivirus and the emerging concept of 'giant’ virus. In: Virus Research. Band 117, Nr. 1, 2006, S. 133–144, doi:10.1016/j.virusres.2006.01.008, PMID 16469402, arxiv:q-bio/0506007.
- ↑ Hiroyuki Ogata, Didier Raoult, Jean-Michel Claverie: A new example of viral intein in Mimivirus. In: Virol J. Band 2, Nr. 8, 2005, PMID 15707490, PMC 549080 (freier Volltext).
- ↑ a b Y. Mutsafi, N. Zauberman, I. Sabanay, A. Minsky.: Vaccinia-like cytoplasmic replication of the giant Mimivirus. In: Proc Natl Acad Sci USA (PNAS). Band 107, Nr. 13, 2010, S. 5978–5982, doi:10.1073/pnas.0912737107, PMID 20231474, PMC 2851855 (freier Volltext).
- ↑ a b Leena Hussein Bajrai, Saïd Mougari, Julien Andreani, Emeline Baptiste, Jeremy Delerce, Didier Raoult, Esam Ibraheem Azhar, Bernard La Scola, Anthony Levasseur: Isolation of Yasminevirus, the First Member of Klosneuvirinae Isolated in Coculture with Vermamoeba vermiformis, Demonstrates an Extended Arsenal of Translational Apparatus Components. In: ASM Journals: Journal of Virology, Band 94, Nr. 1, 12. Dezember 2019; doi:10.1128/JVI.01534-19 , PMID 31597770, PMC 6912108 (freier Volltext), ResearchGate, Epub Oktober 2019.
- ↑ a b Bernard La Scola, T. J. Marrie, J. P. Auffray, Didier Raoult: Mimivirus in pneumonia patients. In: Emerg Infect Dis. 11. Jahrgang, Nr. 3, 2005, S. 449–452, PMID 15757563, PMC 3298252 (freier Volltext) – (englisch).
- ↑ T. J. Marrie, H. Durant, L. Yates: Community-Acquired Pneumonia Requiring Hospitalization: 5-Year Prospective Study. In: Reviews of Infectious Diseases. 11. Jahrgang, Nr. 4, 1989, S. 586–99, doi:10.1093/clinids/11.4.586, PMID 2772465 (englisch).
- ↑ Hanene Saadi, Isabelle Pagnier, Philippe Colson, Jouda Kanoun Cherif, Majed Beji, Mondher Boughalmi, Saïd Azza, Nicholas Armstrong, Catherine Robert, Ghislain Fournous, Bernard La Scola, Didier Raoult: First isolation of Mimivirus in a patient with pneumonia. In: Clinical Infectious Diseases. 57. Jahrgang, Nr. 4, August 2013, S. e127–34, doi:10.1093/cid/cit354, PMID 23709652 (englisch).
- ↑ a b E. Ghigo, J. Kartenbeck, P. Lien, L. Pelkmans, C. Capo, J. L. Mege, Didier Raoult: Ameobal pathogen mimivirus infects macrophages through phagocytosis. In: PLoS pathogens. Band 4, Nummer 6, Juni 2008, S. e1000087, doi:10.1371/journal.ppat.1000087, PMID 18551172, PMC 2398789 (freier Volltext).
- ↑ Vincent A., La Scola B., Papazian L.: Advances in Mimivirus pathogenicity. In: Intervirology. Band 53, Nr. 5, 2010, S. 304–309, doi:10.1159/000312915, PMID 20551682.
- ↑ P. Berger, L. Papazian, M. Drancourt, Bernard La Scola, J. P. Auffray, Didier Raoult: Ameba-associated microorganisms and diagnosis of nosocomial pneumonia. In: Emerg Infect Dis. 12. Jahrgang, Nr. 2, 2006, S. 248–255, PMID 16494750, PMC 3373093 (freier Volltext) – (englisch).
- ↑ Didier Raoult, P. Renesto, P. Brouqui: Laboratory infection of a technician by mimivirus. In: Ann Intern Med. 144. Jahrgang, Nr. 9, 2006, S. 702–703, PMID 16670147 (englisch, annals.org).
- ↑ M. J. Vanspauwen et al.: Infections with mimivirus in patients with chronic obstructive pulmonary disease. In: Respiratory Medicine. 106. Jahrgang, Nr. 12, 2012, S. 1690–1694, doi:10.1016/j.rmed.2012.08.019 (englisch, sciencedirect.com).
- ↑ Anthony Levasseur, Meriem Bekliz, Eric Chabrière, Pierre Pontarotti, Bernard La Scola, Didier Raoult: MIMIVIRE is a defence system in mimivirus that confers resistance to virophage. In: Nature, 2016, doi:10.1038/nature17146.
- ↑ Ewen Callaway: CRISPR-like 'immune' system discovered in giant virus. In: Nature: News, 29. Juni 2016; doi:10.1038/nature.2016.19462.
- ↑ Nisrine Chelkha, Anthony Levasseur, Pierre Pontarotti, Didier Raoult et al.: A Phylogenomic Study of Acanthamoeba polyphaga Draft Genome Sequences Suggests Genetic Exchanges With Giant Viruses, in: Frontiers in Microbiology 9:2098, September 2018; doi:10.3389/fmicb.2018.02098
- ↑ Patrick L. Scheid: Free-Living Amoebae and Their Multiple Impacts on Environmental Health. In: Reference Module in Earth Systems and Environmental Sciences, 27. Februar 2018, doi:10.1016/B978-0-12-409548-9.10969-8]
- ↑ a b List of the main “giant” viruses known as of today. (PDF) Centre national de la recherche scientifique, Université d’Aix-Marseille, März 2019.
- ↑ Christoph M. Deeg, Cheryl-Emiliane T. Chow, Curtis A. Suttle: The kinetoplastid-infecting Bodo saltans virus (BsV), a window into the most abundant giant viruses in the sea…, in: eLife Sciences 7, März 2018, doi:10.7554/eLife.33014
- ↑ a b Paulo V. M. Boratto, Thalita S. Arantes, Lorena C. F. Silva, Felipe L. Assis, Erna G. Kroon, Bernard La Scola, Jônatas S. Abrahão: Niemeyer Virus: A New Mimivirus Group A Isolate Harboring a Set of Duplicated Aminoacyl-tRNA Synthetase Genes. In: Front Microbiol. Band 6, 2015, S. 1256. doi:10.3389/fmicb.2015.01256, PMC 4639698 (freier Volltext). PMID 26635738.
- ↑ a b c Gabriel Augusto Pires de Souza, Victória Fulgêncio Queiroz, Maurício Teixeira Lima, Erik Vinicius de Sousa Reis, Luiz Felipe Leomil Coelho, Jônatas Santos Abrahão: Virus goes viral: an educational kit for virology classes. In: Virology Journal, Band 17, Nr. 13, 31. Januar 2020, doi:10.1186/s12985-020-1291-9
- ↑ List of the main “giant” viruses known as of today. (PDF) Centre national de la recherche scientifique, Université d’Aix-Marseille, 18. April 2018.
- ↑ a b c NCBI Taxonomy Browser: Acanthamoeba polyphaga mimivirus, Detail: Acanthamoeba polyphaga mimivirus (spezies).
- ↑ Clara Rolland, Julien Andreani, Amina Cherif Louazani, Sarah Aherfi, Rania Francis, Rodrigo Rodrigues, Ludmila Santos Silva, Dehia Sahmi, Said Mougari, Nisrine Chelkha, Meriem Bekliz, Lorena Silva, Felipe Assis, Fábio Dornas, Jacques Yaacoub Bou Khalil, Isabelle Pagnier, Christelle Desnues, Anthony Levasseur, Philippe Colson, Jônatas Abrahão, Bernard La Scola: Discovery and Further Studies on Giant Viruses at the IHU Mediterranee Infection That Modified the Perception of the Virosphere. In: Viruses, 11(4), März/April 2019, pii: E312, doi:10.3390/v11040312, PMC 6520786 (freier Volltext), PMID 30935049.
- ↑ a b c d Felipe L. Assis, Leena Bajrai, Jonatas S. Abrahao, Erna G. Kroon, Fabio P. Dornas, Kétyllen R. Andrade, Paulo V. M. Boratto, Mariana R. Pilotto, Catherine Robert, Samia Benamar, Bernard La Scola, Philippe Colson: Pan-Genome Analysis of Brazilian Lineage A Amoebal Mimiviruses, in: Viruses 7(7), 2015, S. 3483–3499, doi:10.3390/v7072782. Die hier abgehandelten Kandidaten stellen nach den Autoren eine Verwandtschaftsgruppe dar, wobei aus den anderen Quellen hervorgeht, dass Samba- und Kroon-Virus zur Spezies APMV gehören. Das gilt dann für die beiden anderen.
- ↑ a b c d Kétyllen R. Andrade, Paulo P. V. M. Boratto, Felipe P. Rodrigues, Lorena C. F. Silva, Fábio P. Dornas, Mariana R. Pilotto, Bernard La Scola, Gabriel M. F. Almeida, Erna G. Kroon, Jônatas S. Abrahão: Oysters as hot spots for mimivirus isolation. In: Archives of Virology, Band 160, Februar 2015, S. 477–482; doi:10.1007/s00705-014-2257-2, PMID 25344898. Siehe insbes. Fig. 2.
- ↑ NCBI Taxonomy Browser: Mimivirus amazonia (species).
- ↑ a b c d e f g h i j k l m n o p q r s t u v Didier Raoult, Anthony Levasseur, Bernard La Scola: PCR Detection of Mimivirus, in: Emerging Infectious Diseases, Juni 2017, Band 23, Nr. 6, S. 1044–1045, doi:10.3201/eid2306.161896
- ↑ NCBI Taxonomy Browser: Mimivirus terra2, equivalent: Mimiviridae Terra2 (spezies).
Anm.: Die Spezies wurde von ICTV mit MSL#38 im April 2023 der Spezies Mimivirus bradfordmassiliense (Mimivirus bradfordmassiliense, ApMV) zugeordnet. - ↑ a b c d e f Christelle Desnues, Bernard La Scola, Natalya Yutin, Ghislain Fournous et al.: Provirophages and transpovirons as the diverse mobilome of giant viruses, in: PNAS 109(44), 30. Oktober 2012, S. 18078–18083, doi:10.1073/pnas.1208835109
- ↑ a b c d e Anirvan Chatterjee, Thomas Sicheritz-Pontén, Rajesh Yadav, Kiran Kondabagil: Isolation and complete genome sequencing of Mimivirus bombay, a Giant Virus in sewage of Mumbai, India. In: Genomics Data. 9(C), Mai 2016; doi:10.1016/j.gdata.2016.05.013, Fig. 2.
- ↑ Hansika Chhabra: Giant viruses found in water samples from Mumbai, in: BusinessLine: Science, Bangalore, 9. Mai 2019
- ↑ a b c d Sailen Barik: A Family of Novel Cyclophilins, Conserved in the Mimivirus Genus of the Giant DNA Viruses, in: Computational and Structural Biotechnology Journal, Band 16, Juli 2018, S. 231–236, doi:10.1016/j.csbj.2018.07.001.
- ↑ Anirvan Chatterjee, Thomas Sicheritz-Pontén, Rajesh Yadav, Kiran Kondabagil: Genomic and metagenomic signatures of giant viruses are ubiquitous in water samples from sewage, inland lake, waste water treatment plant, and municipal water supply in Mumbai, India. In: Scientific Reports, Band 9, Nr. 3690, 6. März 2019; doi:10.1038/s41598-019-40171-y, PMID 30842490, PMC 6403294 (freier Volltext).
- ↑
NCBI Taxonomy Browser: Hirudovirus strain sangsue (species), Nucleotide: Hirudovirus strain Sangsue …
Anm.: Die Spezies wurde von ICTV mit MSL#38 im April 2023 der Spezies Mimivirus bradfordmassiliense (Mimivirus bradfordmassiliense, ApMV) zugeordnet. - ↑ Mondher Boughalmi, Isabelle Pagnier, Sarah Aherfi, Philippe Colson, Didier Raoult, Bernard La Scola: First Isolation of a Giant Virus from Wild Hirudo medicinalis Leech: Mimiviridae isolation in Hirudo medicinalis] (PDF) in: Viruses 2013, 5, S. 2920–2930, doi:10.3390/v5122920.
- ↑
NCBI Taxonomy Browser: Niemeyer virus (species).
Anm.: Die Spezies wurde von ICTV mit MSL#38 im April 2023 der Spezies Mimivirus bradfordmassiliense (Mimivirus bradfordmassiliense, ApMV) zugeordnet. - ↑ Elton Alisson: New giant virus found in Brazil, bei: Agência FAPESP, Brasilien, 4. Juni 2014.
- ↑ Rafael K Campos, Paulo V Boratto, Felipe L Assis, Eric RGR Aguiar, Lorena CF Silva, Jonas D Albarnaz, Fabio P Dornas, Giliane S Trindade, Paulo P Ferreira, João T Marques, Catherine Robert, Didier Raoult, Erna G Kroon, Bernard La Scola, Jônatas S Abrahão: Samba virus: a novel mimivirus from a giant rain forest, the Brazilian Amazon. in: Virology Journal 2014 11:95, doi:10.1186/1743-422X-11-95.
- ↑
Jason R. Schrad, Jônatas S. Abrahão, Juliana R. Cortines, Kristin N. Parent: Structural and Proteomic Characterization of the Initiation of Giant Virus Infection. In: Cell, 8. Mai 2020; doi:10.1016/j.cell.2020.04.032, PDF. Dazu:
- Jason R. Schrad, Jônatas S. Abrahão, Juliana R. Cortines, Kristin N. Parent: Boiling Acid Mimics Intracellular Giant Virus Genome Release. Auf: bioRxiv, 20. September 2019; doi:10.1101/777854 (Preprint).
- Mysterious Giant Viruses: Gargantuan in Size and Complexity. Auf: SciTechDaily, 9. Mai 2020, Quelle: Michigan State University.
- ↑ a b Masaharu Takemura, Tatsuya Mikami, Shingo Murono: Nearly Complete Genome Sequences of Two Mimivirus Strains Isolated from a Japanese Freshwater Pond and River Mouth, in: Genome Announc. 4(6), November/Dezember 2016, e01378-16, doi:10.1128/genomeA.01378-16, PMC 5146454 (freier Volltext). PMID 27932662. Die beiden Viruslinien sind nac Angaben der Autoren eng mit Mimivirus Bombay verwandt, gehören also ebenfalls zur Spezies APMV.
- ↑
NCBI Taxonomy Browser: Acanthamoeba castellanii mamavirus (species).
Anm.: Die Spezies wurde von ICTV mit MSL#38 im April 2023 der Spezies Mimivirus bradfordmassiliense (Mimivirus bradfordmassiliense, ApMV) zugeordnet. - ↑ a b
Julien Guglielmini, Anthony C. Woo, Mart Krupovic, Patrick Forterre, Morgan Gaia: pnas.org, in: PNAS 116(39), 10./24. September 2019, S. 19585–19592, doi:10.1073/pnas.1912006116. PMID 31506349, Fig. 2. Dazu:
Julien Guglielmini, Anthony Woo, Mart Krupovic, Patrick Forterre, Morgan Gaia: Diversification of giant and large eukaryotic dsDNA viruses predated the origin of modern eukaryotes, auf: bioRxiv vom 29. Oktober 2018 (Preprint), doi:10.1101/455816 - ↑ a b c Yeh Fong Tan, Chai Ying Lim, Chun Wie Chong, Patricia Kim Chooi Lim, Ivan K. S. Yap, Pooi Pooi Leong, Kenny Voon: Isolation and Quantification of Mimivirus-Like and Marseillevirus-Like Viruses from Soil Samples in An Aboriginal (Orang asli) Village in Peninsular Malaysia. In: Intervirology, Band 61, Nr. 2, August 2018, S. 1–4; doi:10.1159/000491602, ResearchGate, Medscape, PDF (PDF; 523 kB) Fig. 2 – SR1, SR4 und SR9 sind untereinander nahe verwandt, stehen aber den anderen Kandidaten der Linie A viel näher als dem Saudi moumouvirus (Linie B). Die Zuordnung zur Linie A ist daher wahrscheinlich.
- ↑
NCBI Nucleotide: Acanthamoeba castellanii mamavirus MAMA_R546 …
Anm.: Lait NCBI Nucleitide zu Acanthamoeba castellanii mamavirus. Diese Spezies wurde von ICTV mit MSL#38 im April 2023 der Spezies Mimivirus bradfordmassiliense (Mimivirus bradfordmassiliense, ApMV) zugeordnet. Diese Zuordnung wird hier für MAMA_R546 übernommen. - ↑ Paulo Victor Miranda Boratto, Fábio Pio Dornas, Lorena Christine Ferreira da Silva, Rodrigo Araújo Lima Rodrigues, Graziele Pereira Oliveira, Juliana Reis Cortines, Betânia Paiva Drumond, Jônatas Santos Abrahão: Analyses of the Kroon Virus Major Capsid Gene and Its Transcript Highlight a Distinct Pattern of Gene Evolution and Splicing among Mimiviruses. in: J Virol. 92(2), 15. Januar 2018, e01782-17, doi:10.1128/JVI.01782-17, PMC 5752926 (freier Volltext), PMID 29118120.
- ↑ NCBI Nucleotide: UNVERIFIED: Acanthamoeba polyphaga mimivirus strain Kroon, …
- ↑ NCBI Taxonomy Browser: Mimivirus argentum (species)
- ↑ Bruna Luiza de Azevedo, João Pessoa Araújo Júnior, Leila Sabrina Ullmann, Rodrigo Araújo Lima Rodrigues, Jônatas Santos Abrahão: The Discovery of a New Mimivirus Isolate in Association with Virophage-Transpoviron Elements in Brazil Highlights the Main Genomic and Evolutionary Features of This Tripartite System. In: MDPI: Viruses, Band 14, Nr. 2, Section General Virology, 21. Januar 2022, S. 206; doi:10.3390/v14020206.
- ↑ NCBI Taxonomy Browser: Mimivirus battle6 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus battle7 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus battle19 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus battle27 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus battle57 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus battle66 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus battle83 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus battle86 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus Cher (species)
- ↑ NCBI Taxonomy Browser: Mimivirus fauteuil (species).
- ↑ NCBI Taxonomy Browser: Fauteuil virus FD (species).
- ↑ NCBI Taxonomy Browser: Mimivirus dakar4 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus huitre A06 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus lentille (species).
- ↑ NCBI Taxonomy Browser: Lentille virus CL (species)
- ↑ NCBI Taxonomy Browser: Mimivirus lactour, equivalent: Mimiviridae Lactours (species).
- ↑ NCBI Taxonomy Browser: Lactours virus LT2 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus longchamps (species).
- ↑ NCBI Taxonomy Browser: Longchamps virus FPL (species).
- ↑ NCBI Taxonomy Browser: Mimivirus marais (species).
- ↑ NCBI Taxonomy Browser: Mimivirus montadette2 (species).
- ↑ NCBI Taxonomy Browser: Mimivirus pointerouge1 (species).
- ↑ NCBI Taxonomy Browser: Pointerouge virus 1 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus pointerouge2 (species).
- ↑ NCBI Taxonomy Browser: Pointerouge virus 2 (species)
- ↑ NCBI Taxonomy Browser: Mimivirus SR1 (species).
- ↑ NCBI Taxonomy Browser: Mimivirus SR4 (species).
- ↑ NCBI Taxonomy Browser: Mimivirus SR9 (species).
- ↑ NCBI Taxonomy Browser: Mimivirus sp. styx (species).
- ↑ NCBI Taxonomy Browser: Mimivirus T2 (species).
- ↑ NCBI Taxonomy Browser: Mimivirus T3 (species).
- ↑ NCBI Taxonomy Browser: Mimivirus univirus (species).
- ↑ Sandra Jeudy, Lionel Bertaux, Jean-Marie Alempic, Audrey Lartigue, Matthieu Legendre, Lucid Belmudes, Sébastien Santini, Nadège Philippe, Laure Beucher, Emanuele G. Biondi, Sissel Juul, Daniel J. Turner, Yohann Couté, Jean-Michel Claverie, Chantal Abergel: Exploration of the propagation of transpovirons within Mimiviridae reveals a unique example of commensalism in the viral world. In: The ISME Journal, Band 14, S. 727–739, 10. Dezember 2019; doi:10.1038/s41396-019-0565-y, PMID 31822788, PMC 7031253 (freier Volltext).
- ↑ a b Jônatas Abrahão, Lorena Silva, Ludmila Santos Silva, Jacques Yaacoub Bou Khalil, Rodrigo Rodrigues, Thalita Arantes, Felipe Assis, Paulo Boratto, Miguel Andrade, Erna Geessien Kroon, Bergmann Ribeiro, Ivan Bergier, Herve Seligmann, Eric Ghigo, Philippe Colson, Anthony Levasseur, Guido Kroemer, Didier Raoult, Bernard La Scola: Tailed giant Tupanvirus possesses the most complete translational apparatus of the known virosphere. In: Nature Communications. Band 9, Nr. 1, 2018, S. 749, doi:10.1038/s41467-018-03168-1, PMID 29487281. Siehe insbes. Fig. 4.
![TEM-Aufnahme eines Mimivirus-Virions (ApMV) mit Stargate und Filamenten.[22]](http://upload.wikimedia.org/wikipedia/commons/thumb/4/4f/F21-01-9780123846846_mimivirus_particle_stargate.png/175px-F21-01-9780123846846_mimivirus_particle_stargate.png)
