Ytterbium(II)-bromid
| Kristallstruktur | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
| _ Yb2+ _ Br− | |||||||
| Allgemeines | |||||||
| Name | Ytterbium(II)-bromid | ||||||
| Andere Namen |
Ytterbiumdibromid | ||||||
| Verhältnisformel | YbBr2 | ||||||
| Kurzbeschreibung |
hellgelber Feststoff[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 332,84 g·mol−1 | ||||||
| Aggregatzustand |
fest[1] | ||||||
| Schmelzpunkt | |||||||
| Siedepunkt |
1140 °C[1] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Ytterbium(II)-bromid ist eine anorganische chemische Verbindung des Ytterbiums aus der Gruppe der Bromide.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Ytterbium(II)-bromid kann durch Reduktion von Ytterbium(III)-bromid mit Wasserstoff bei 500 °C bis 600 °C gewonnen werden.[1]
Ebenfalls möglich ist die Reaktion von Ytterbium mit Ammoniumbromid in flüssigem Ammoniak bei −78 °C. Man erhält zunächst das Ammoniakat von Ytterbium(II)-bromid, das dann bei etwa 200 °C im Hochvakuum abgebaut werden kann.[1]
Ytterbium(II)-bromid kann auch durch Reduktion von Ytterbium(III)-bromid mit Ytterbium im Vakuum bei 960 °C gewonnen werden.[3]
Eigenschaften
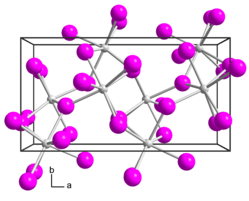
[Bearbeiten | Quelltext bearbeiten]Ytterbium(II)-bromid ist ein hellgelber Feststoff. Die Verbindung ist äußerst hygroskopisch und kann nur unter sorgfältig getrocknetem Schutzgas oder im Hochvakuum aufbewahrt und gehandhabt werden. An Luft oder bei Kontakt mit Wasser geht er unter Feuchtigkeitsaufnahme in Hydrate über, die aber instabil sind und sich mehr oder weniger rasch unter Wasserstoff-Entwicklung in Oxidbromide verwandeln. Die Verbindung besitzt eine orthorhombische Kristallstruktur vom Strontium(II)-iodid (Raumgruppe Pbca (Raumgruppen-Nr. 61))[3] oder Calciumchlorid-Typ mit der Raumgruppe Pnnm (Nr. 58). Die Gitterparameter letzterer Form sind a = 6,63 Å, b = 6,93 Å und c = 4,37 Å.[1][4] Sie wird jedoch nur beobachtet, wenn die Probe mit dreiwertigem Yb kontaminiert ist.[3]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1081.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c Christine A. Voos-Esquivel, Harry A. Eick: Synthesis of YbBr2 and YbCl2 and an x-ray diffraction study of the system YbBr2—YbCl2. In: Journal of Solid State Chemistry. 67, 1987, S. 291–296, doi:10.1016/0022-4596(87)90366-5.
- ↑ Horst. P. Beck, H. Bärnighausen: Zur Kristallchemie der Ytterbium(II)-Halogenide YbCl2 und YbBr2. In: Zeitschrift für anorganische und allgemeine Chemie. 386, 1971, S. 221–228, doi:10.1002/zaac.19713860214.


