Brustkrebs

| Klassifikation nach ICD-10 | |
|---|---|
| C50 | Mammakarzinom |
| C50.0 | Brustwarze und Warzenhof |
| C50.1 | Zentraler Drüsenkörper der Brustdrüse |
| C50.2 | Oberer innerer Quadrant der Brustdrüse |
| C50.3 | Unterer innerer Quadrant der Brustdrüse |
| C50.4 | Oberer äußerer Quadrant der Brustdrüse |
| C50.5 | Unterer äußerer Quadrant der Brustdrüse |
| C50.6 | Recessus axillaris der Brustdrüse |
| C50.8 | Brustdrüse, mehrere Teilbereiche überlappend |
| C50.9 | Brustdrüse, nicht näher bezeichnet |
| ICD-10 online (WHO-Version 2019) | |

Brustkrebs oder Mammakarzinom (von lateinisch mamma „Zitze, Brust; weibliche Brustdrüse“) ist der häufigste bösartige Tumor der Brustdrüse des Menschen. Er kommt hauptsächlich bei Frauen vor; nur etwa jede hundertste dieser Krebserkrankungen tritt bei Männern auf.[1] In den westlichen Staaten ist Brustkrebs die häufigste Krebsart bei Frauen. Am Brustkrebs sterben mehr Frauen als an irgendeiner anderen Krebserkrankung. Die meisten Erkrankungen treten sporadisch (zufällig) auf, es gibt aber sowohl erbliche als auch erworbene Risikofaktoren. Neben der Heilung sind der Erhalt der betreffenden Brust und vor allem der Lebensqualität erklärtes Ziel der medizinischen Behandlung.
Die Therapie besteht in der Regel in einer an das Erkrankungsstadium angepassten Kombination aus Operation sowie Zytostatika-, Hormon- und Strahlentherapie. Neue Ansätze aus dem Gebiet der Krebsimmuntherapie werden außerdem durch monoklonale Antikörper (wie z. B. durch die Verabreichung von Trastuzumab oder Pertuzumab) ermöglicht. Das medizinische Vorgehen basiert in hohem Maß auf Erfahrungen aus Studien, folgt oft der evidenzbasierten Medizin und ist in weltweit akzeptierten Leitlinien standardisiert. Zahlreiche nationale und internationale Programme zur Früherkennung und zur strukturierten Behandlung sollen die Letalität (Sterblichkeit) künftig senken.
Epidemiologie
[Bearbeiten | Quelltext bearbeiten]

Brustkrebs bei der Frau
[Bearbeiten | Quelltext bearbeiten]In Deutschland ist das Mammakarzinom mit einem Anteil von 32 % aller Krebsneuerkrankungen die häufigste Krebserkrankung bei Frauen. Das Lebenszeitrisiko wird mit 12,9 % angegeben, d. h. etwa jede achte Frau erkrankt im Laufe ihres Lebens an Brustkrebs.[2] Dies sind in Deutschland etwa 71.900 Neuerkrankungen pro Jahr (2019) oder 171 Fälle pro 100.000 Einwohner und Jahr.[3]
Die Weltgesundheitsorganisation (WHO) gab zum Weltkrebstag im April 2021 bekannt, dass im Jahr 2020 weltweit 19,3 Millionen Menschen an Krebs erkrankten. Als häufigste Krebsart sei Brustkrebs registriert worden, gefolgt von Lungenkrebs. Die Zahl von derzeit rund 20 Millionen Krebs-Neuerkrankungen könnte laut WHO bis 2040 auf etwa 30 Millionen weltweit ansteigen. Für Deutschland prognostizierte die Deutsche Krebshilfe einen Anstieg auf rund 600.000 Krebsfälle im Jahr 2030.[4] Auf Basis von aktuellen Erkrankungszahlen und der erwarteten demografischen Entwicklung haben Wissenschaftler der Internationalen Agentur für Krebsforschung (IARC) und von anderen Instituten im Fachmagazin The Breast eine Prognose für die globale Häufigkeit der Erkrankung aufgestellt: Bis 2040 werde die Krankheitslast weiter zunehmen. Die Autoren gehen dann von über drei Millionen Neuerkrankungen (+40,8 % im Vergleich zu 2020) und einer Million Todesfällen (+51,9 %) pro Jahr aus – allein schon wegen der wachsenden und immer älter werdenden Weltbevölkerung.[5]
Bei internationalen Vergleichen muss die unterschiedliche Altersverteilung der nationalen Bevölkerungen berücksichtigt werden. Die nach dem sogenannten Europastandard (ESR) altersstandardisierte Inzidenz (Neuerkrankungsrate) lag in Deutschland im Jahr 2010 für Frauen bei 119,6/100.000.[3] Die brustkrebsbedingte Sterberate (Mortalität) betrug im selben Jahr altersstandardisiert 24,0/100.000 nach dem ESR.[3] Seit 1970 haben sich die Erkrankungszahlen verdoppelt, während die Mortalität eher rückläufig ist.[6]
Brustkrebs ist weltweit die häufigste invasive Tumorerkrankung bei Frauen. Weltweit gibt es nach Schätzungen der WHO (2003) etwa 1.050.000 neue Erkrankungsfälle pro Jahr, davon 580.000 in den Industriestaaten. Vergleichsweise seltener ist die Erkrankung in Afrika und Asien. Weltweit starben 1998 circa 412.000 Frauen an Brustkrebs, das sind 1,6 % aller gestorbenen Frauen.[7] Damit ist Brustkrebs weltweit die häufigste krebsbedingte Todesursache bei Frauen. In der westlichen Welt ist Brustkrebs bei Frauen zwischen dem 30. und 60. Lebensjahr die häufigste Todesursache überhaupt.
In Deutschland schätzt man etwa 17.460 brustkrebsbedingte Todesfälle pro Jahr[3] und in den Vereinigten Staaten etwa 40.200. In Deutschland beträgt die durchschnittliche Fünfjahresüberlebensrate zurzeit 86–90 %.[3][8] Während jedoch in den reichen Ländern die Sterberate sinkt, ist sie in den ärmeren Ländern hoch. Dies hängt zum einen mit der immer höheren Lebenserwartung zusammen, zum anderen mit den schlechteren diagnostischen und therapeutischen Möglichkeiten in den ärmeren Ländern. WHO-Angaben zufolge starben 2007 etwa 72 Prozent aller an Krebs erkrankten Menschen in Ländern mit mittlerem und niedrigem Einkommen.[9] Dennoch gab es 2013 in den Vereinigten Staaten das Phänomen von steigenden Brustkrebsraten bei jungen Frauen, für die es bisher keine zufriedenstellende Erklärung gibt.[10]
| Anzahl der in Deutschland am Mammakarzinom verstorbenen Frauen nach Altersgruppen[11] | ||||
| Alter | 2003 | 2004 | 2005 | 2006 |
|---|---|---|---|---|
| 0–30 | 16 1 | 20 2 | 16 | 13 |
| 30–40 | 348 | 318 | 294 | 294 |
| 40–50 | 1.271 | 1.296 | 1.283 | 1.176 |
| 50–60 | 2.493 | 2.404 | 2.419 | 2.489 |
| 60–70 | 4.158 | 4.441 | 4.252 | 4.035 |
| 70–80 | 4.140 | 4.354 | 4.273 | 4.283 |
| >80 | 4.747 | 4.759 | 4.918 | 4.996 |
| Gesamt | 17.173 | 17.592 | 17.455 | 17.286 |
|
1 Ein Mädchen 5–10 Jahre 2 Ein Mädchen 10–15 Jahre | ||||
| Anteil der Todesursache „Mammakarzinom“ in Prozent nach Altersgruppen (nur Frauen, Deutschland)[11] | ||||
| Alter | 2003 | 2004 | 2005 | 2006 |
|---|---|---|---|---|
| 0–30 | 0,4 | 0,5 | 0,5 | 0,4 |
| 30–40 | 10 | 11 | 10 | 11 |
| 40–50 | 13 | 14 | 14 | 13 |
| 50–60 | 14 | 14 | 13 | 14 |
| 60–70 | 9 | 10 | 10 | 10 |
| 70–80 | 4 | 5 | 4 | 5 |
| >80 | 2 | 2 | 2 | 2 |
Brustkrebs beim Mann
[Bearbeiten | Quelltext bearbeiten]Männer erkranken seltener an Brustkrebs. In Uganda sind fünf Prozent aller Mammakarzinompatienten männlich, in Sambia liegt der Anteil sogar bei 15 Prozent.[12] Nach aktueller Statistik 2019 sind es in Deutschland jährlich etwa 700 Männer.[13] Das Verhältnis von Erkrankungen bei Männern zu Frauen liegt bei 1:100.[14] Die standardisierten globalen Inzidenzraten für Brustkrebs betrugen bei Männern 0,40 pro 105 Personenjahre (66,7 pro 105 bei Frauen). Die Diagnosestellung erfolgt bei Männern in einem höheren medianen Alter (69,6 Jahre). Männliche Patienten weisen zwar eine schlechtere relative 5-Jahres-Überlebensrate auf als Frauen (0,72 [95 % KI: 0,70–0,75] bzw. 0,78 [95 % KI: 0,78-0,78]), was einem relativen erhöhten Mortalitätsrisiko von 1,27 (95 % KI: 1,13–1,42) entspricht, sie zeigen jedoch nach Anpassung um Alter und Jahr der Diagnosestellung, Stadium und Therapie ein signifikant besseres relatives Brustkrebs-assoziiertes Überleben als Patientinnen.[15] Die Mortalität bei Männern liegt bei rund 200 Todesfällen pro Jahr. Eine Studie der European Organisation for Research and Treatment of Cancer (EORTC) zusammen mit anderen Fachverbänden aus Europa und Nordamerika soll die Ursachen für diese Geschlechterdifferenz detailliert aufklären.[12]
- Risikofaktoren für Brustkrebs bei Männern
Die Häufigkeit von Brustkrebs bei Männern wird durch demographische, genetische, umweltbedingte und endokrine Faktoren gesteigert[16]:
| Gruppe | Risikofaktor |
|---|---|
| Demographie | höheres Alter |
| Afroamerikaner | |
| familiäres Risiko | |
| Genetik | BRCA2 |
| BRCA1 | |
| CHEK2 | |
| PALB2 | |
| Umwelt | Strahlenexposition |
| Endokrine Faktoren | Östradiol im Serum erhöht |
| Klinefelter-Syndrom | |
| Gynäkomastie | |
| Leberfunktionsstörung | |
| Adipositas | |
| Störung der Hodenfunktion |
Anmerkungen: CHEK2 ist an der DNA-Reparatur beteiligt. Das Gen kodiert eine Zellzyklus-Checkpoint-Kinase. PALB2 wird Partner und Lokalisierer von BRCA2 genannt. Das Gen kodiert ein Protein, welches mit dem Brustkrebsrisikofaktor BRCA2 interagiert.
Den Aufbau und die Betreuung des 2010 in der Bundesrepublik gebildeten ersten Selbsthilfe-Netzwerks „Netzwerk Männer mit Brustkrebs e. V.“ hat die bundesweite Frauenselbsthilfe nach Krebs (FSH) in Bonn unter dem Patronat der Stiftung Deutsche Krebshilfe übernommen. Neben dem Netzwerk Männer mit Brustkrebs[17] und dem Infonetz Krebs bietet auch der Krebsinformationsdienst[18] Informationen zu diesem Thema.
Symptome für eine Erkrankung sind Flüssigkeitsabsonderung aus der Brustwarze, kleine Entzündungen oder Wunden, die nicht abheilen oder eine Einziehung der Brusthaut an einer Stelle oder der Brustwarze.
Zur Behandlung können in einer Operation sowohl tumorverdächtige Bereiche wie auch benachbarte Lymphknoten aus der Achselhöhle entnommen werden. Über solche Lymphknoten können sich Tumorzellen am ehesten im Körper ausbreiten. Möglich ist auch eine Strahlentherapie der Brustwand und eventuell eine Chemotherapie. Auch bei Männern kann eine antihormonelle Therapie sinnvoll sein, wenn ihr Tumor östrogenabhängig wächst, und/oder eine Therapie mit Antikörpern, die sich gegen besondere Merkmale mancher Brustkrebszellen richten. Männer bilden auch das Hormon Östrogen, jedoch in sehr viel geringerem Maße als Frauen.
Ursachen und Risikofaktoren
[Bearbeiten | Quelltext bearbeiten]Genetische Risikofaktoren
[Bearbeiten | Quelltext bearbeiten]Etwa 5 bis 10 % der Brustkrebserkrankungen können erblich bedingt sein.[19] Nur bei einer kleinen Gruppe von Frauen (etwa 1 pro 500) findet man definierte, krankheitsverursachende Mutationen. Wesentlich häufiger sind genetische Veränderungen, die die Suszeptibilität (Empfänglichkeit) für Brustkrebs auf äußere Faktoren erhöhen.
Die höchste Wahrscheinlichkeit, an der erblichen Form des Brustkrebs zu erkranken, besteht bei Frauen mit Mutation in den Genen BRCA1 und BRCA2 (BRCA1/2 = Breast Cancer Gene 1/2). Es kommt bereits bei einer Mutation in einem Allel dieser Gene zur Erkrankung (man spricht von sogenannten Tumorsuppressorgenen mit autosomal-dominantem Erbgang). Die Wahrscheinlichkeit, im Laufe des Lebens an Brustkrebs zu erkranken, wird für Trägerinnen des mutierten BRCA1 mit 65 %, für Trägerinnen des mutierten BRCA2 mit 45 % angegeben.[20]
Mutationen im p53-Gen, einem der Tumorsuppressorgene, werden autosomal-dominant vererbt (Li-Fraumeni-Syndrom). Weitere Genveränderungen, die das Risiko erhöhen, betreffen Mutationen von PTEN (Cowden-Syndrom), STK11 (Peutz-Jeghers-Syndrom) und CDH1 (E-Cadherin); deren Häufigkeit und Risikoerhöhung für die Brustkrebserkrankung ist jedoch nicht genau bekannt. Mäßig erhöht ist die Wahrscheinlichkeit bei Bestehen der seltenen genetischen Veränderungen mit mittlerer Penetranz, diese betreffen unter anderem die folgenden Gene: ATM (Ataxia teleangiectatica), CHK2 (checkpoint kinase 2) und BRIP-1.[21] Insgesamt lassen sich nicht mehr als fünf Prozent der Brustkrebserkrankungen auf diese Genveränderungen mit hohem oder mittlerem Risiko zurückführen.[22]
Die wesentlich häufigeren Allelveränderungen mit geringer Penetranz erhöhen das Brustkrebsrisiko höchstens auf das 1,25-fache bei heterozygoten Veränderungen und auf das 1,65-fache bei homozygoten Veränderungen. Dazu gehören insbesondere Veränderungen von FGFR2 (fibroblast growth factor receptor 2) und auf dem Chromosom 2q. Es wird geschätzt, dass solche Mutationen mit geringer Penetranz bei 58 % der Brustkrebserkrankungen eine Rolle spielen.[23]
Die Wahrscheinlichkeit, selbst zu erkranken, steigt statistisch nachweisbar ab zwei an Brustkrebs Erkrankten in der direkten Verwandtschaft an.[24] Familien, in denen mehrere Personen an Brust- oder Eierstockkrebs erkrankt sind, wird eine tumorgenetische Beratung in einem Beratungszentrum, beispielsweise aus dem Verbundprojekt familiärer Brustkrebs der Deutschen Krebshilfe empfohlen.[25]
Bei Frauen mit einer entsprechenden Prädisposition (hohe Wahrscheinlichkeit des Krankheitsauftretens) kann auf Wunsch eine beidseitige prophylaktische Mastektomie (Brustamputation) und/oder eine Eierstockentfernung vorgenommen werden: Einen gewissen Schutz vor einer Brustkrebserkrankung scheint die weitgehende Unterbindung der Östrogenproduktion durch die Entfernung beider Eierstöcke zu bieten. Verschiedene Autoren berichten von einer Verringerung des Erkrankungsrisikos von 50 bis 70 %, wenn in der Familie bereits Brustkrebs auftrat.[26]
Hormonelle Faktoren
[Bearbeiten | Quelltext bearbeiten]Menschliche Körperzellen, auch Tumorzellen, tragen Rezeptoren für die Sexualhormon-Gruppen Estrogene[27] und Gestagene. Mammakarzinome mit Estrogen- und/oder Gestagen-Rezeptoren können durch eine endokrine Therapie, z. B. Tamoxifen, in ihrem Wachstum gebremst werden[28]. Es wird diskutiert, ob Estrogene und Gestagene die Entstehung von Brustkrebs beeinflussen. Durch eine Blockierung des Estrogen-Rezeptors mit Tamoxifen konnte die Häufigkeit von Brustkrebserkrankungen (Inzidenz) gesenkt werden.[29] Es wurde nur die Häufigkeit von Mammakarzinomen mit Rezeptoren gesenkt. Rezeptor-negative Karzinome wurden nicht beeinflusst. Neben Tamoxifen könnten auch Raloxifen und Exemestane die Inzidenz von Brustkrebs senken. Für den klinischen Einsatz müssen Risiken und Nebenwirkungen sorgfältig abgewogen werden[30]. Eine mehrjährige Hormonersatztherapie gegen Wechseljahresbeschwerden mittels östrogen- und gestagenhaltiger Medikamente kann das Erkrankungsrisiko um bis zu 45 % erhöhen.[31] In der Women’s Health-Initiative war das relative Brustkrebsrisiko 1,26 (Vertrauensbereich 1,00-1,59) nach postmenopausaler Einnahme von Östrogenen und Gestagenen[32]. Auch Frauen mit früher Menarche (erstes Auftreten der Regelblutung in der Pubertät)[33] und später Menopause (Ende der Menstruation, „Wechseljahre“)[34] tragen ein etwas höheres Erkrankungsrisiko. Frauen, die früh Kinder bekommen[35] und lange stillen, haben dagegen ein niedrigeres Risiko.[36]
Inwieweit die Antibabypille das Risiko erhöht, ist ebenso substanz- und dosisabhängig wie bei Hormonersatztherapien und daher nicht allgemein bezifferbar. Die Nurses’ Health Study und weitere Studien konnten jedoch eine typische Erhöhung des Risikos auf das 1,2- bis 1,4-fache nach einer Einnahme der Pille über mehr als fünf Jahre zeigen.
Schwangerschaftsabbrüche erhöhen das Brustkrebsrisiko einer Metaanalyse aus dem Jahr 2004 zufolge nicht.[37] Auch in anderen Studien mit hohen Fallzahlen konnte man einen solchen Zusammenhang nicht nachweisen.[38][39][40]
Linkshändigkeit
[Bearbeiten | Quelltext bearbeiten]Eine Studie,[41] in der festgestellt wurde, dass Linkshänderinnen ein bis zu doppelt so hohes Risiko haben, vor der Menopause an Brustkrebs zu erkranken als Rechtshänderinnen, sorgte im September 2005 für erhöhtes öffentliches Interesse.[42][43] Schon fünf Jahre zuvor war eine andere Studie zu einem ähnlichen Ergebnis gekommen (Risikozunahme +42 %).[44] Eine Studie aus dem Jahr 2007 kommt sogar auf eine um den Faktor 2,59 erhöhte Brustkrebswahrscheinlichkeit bei Linkshänderinnen.[45]
Die Mechanismen für das erhöhte Brustkrebsrisiko bei Linkshänderinnen sind noch weitgehend ungeklärt. Eine in Fachkreisen diskutierte Hypothese besagt, dass eine pränatale Einwirkung von erhöhten Dosen von Sexualhormonen auf den Embryo die Ursache ist. Die Sexualhormone bewirken dabei – so die Hypothese – zum einen, dass das Kind linkshändig wird und zum anderen, dass sich das Brustgewebe verändert und anfälliger für eine Krebserkrankung wird.[44] Die Linkshändigkeit ist dabei gewissermaßen ein Indikator für erhöhte Konzentrationen an Steroiden in der Gebärmutter. Die Hypothese, dass die Grundlage für die Entstehung von Brustkrebs durch die Einwirkung von Sexualhormonen im embryonalen Stadium gebildet werden kann, wird schon seit 1990 diskutiert[46] und basiert auf dem Geschwind-Behan-Galaburda-Modell. Dass Sexualhormone – insbesondere Testosteron – in utero einen Einfluss auf die Ausbildung der Händigkeit haben können, wurde bereits 1985 gezeigt.[47][48]
Linke Brust häufiger als rechte Brust
[Bearbeiten | Quelltext bearbeiten]Statistisch gesehen ist die linke Brust, sowohl bei Frauen als auch Männern, häufiger von Brustkrebs betroffen als die rechte.[49] Davon sind alle Populationen betroffen.[50] Mit zunehmendem Alter wird der Unterschied noch größer.[51] Diese für die linke Brust erhöhte Rate trifft offensichtlich nicht für Tumoren zu, die ihren Entstehungsort im oberen äußeren Quadranten haben.[52] Die Wahrscheinlichkeit, dass die linke Brust an Krebs erkrankt, ist – je nach Studie – um fünf bis sieben Prozent höher als bei der rechten.[49] Bei Männern liegt dieser Wert sogar bei zehn Prozent.[53]
Die Ursachen für dieses Phänomen sind noch weitgehend unklar.[54] Diskutiert werden unter anderem Schlafgewohnheiten,[55] Händigkeit,[44][56] Unterschiede in der Brustgröße und den Gehirnstrukturen sowie Präferenzen beim Stillen.[55] Eine andere Hypothese sieht in der embryonalen Entwicklung des auf der linken Körperseite befindlichen Herzens eine mögliche Ursache.[57]
Bei anderen Organen, wie beispielsweise der Lunge und den Hoden, ist eine ähnliche statistische Häufung zu beobachten. Bei diesen beiden Organen ist die Wahrscheinlichkeit, dass die rechte Hälfte des Organs betroffen ist, um 13 % höher. In diesen Fällen erklärt man sich diesen Unterschied durch das meist kleinere Gewebevolumen der linken Organhälfte.[49]
Weitere Faktoren
[Bearbeiten | Quelltext bearbeiten]Einige weitere Faktoren scheinen einen Effekt auf die Brustkrebsentwicklung zu haben:
- Ionisierende Strahlung in jungen Jahren erhöht das spätere Brustkrebsrisiko.[58] Mammographie-Untersuchungen bei Frauen über 40 Jahren führen zu keiner bedeutsamen Risikosteigerung.[59]
- Starkes und langdauerndes Zigarettenrauchen erhöht die Erkrankungswahrscheinlichkeit um 30 %.[60]
- Patientinnen mit Brustkrebs gaben 2017 bei einer Befragung deutlich häufiger als Frauen in einer (gesunden) Kontrollgruppe Symptome an, die in ihrer Häufung charakteristisch für ein Flammer-Syndrom sind, vor allem kalte Extremitäten, Schmerzempfindlichkeit, gestörte Wärmeregulation (sie frieren leicht), niedriger Blutdruck und rötliche Hautflecken.[61]
- Seit einigen Jahren wird außerdem eine aktive Rolle von Endothelin und Endothelin-konvertierendem Enzym (ECE) im Rahmen der Brustkrebsentstehung und insbesondere der Metastasierung von Brustkrebszellen diskutiert.[62]
- Durch Bewegungsmangel steigt die Erkrankungswahrscheinlichkeit bei Frauen um etwa 25 %.[63]
Brustkrebsauslösung durch eine Infektion („Brustkrebsvirus“) wurde bisher nicht nachgewiesen. Brustimplantate verursachen keinen Brustkrebs,[64] ebenso wenig wie das Tragen von Büstenhaltern.[64]
Einfluss der Ernährung
[Bearbeiten | Quelltext bearbeiten]Deutlich übergewichtige Frauen erkranken 2,5 mal so häufig wie normalgewichtige.[65]
Längere Beobachtungsstudien zeigten für Omega-3-Fettsäuren aus fetthaltigen Fischen zwar einen protektiven Effekt,[66][67] in einer neuen Studie wird jedoch klar, dass die Protektion nur geringgradig ist.[68]
Phytoöstrogene sind Pflanzeninhaltsstoffe mit östrogenartiger Wirkung. Es wurde daher spekuliert, ob Ernährungsformen, die reich an solchen Stoffen sind (etwa auf Sojabasis), das Erkrankungsrisiko beeinflussen.[69][70] Es gibt verschiedene denkbare Wege, wie Isoflavone aus Soja schützend wirken könnten. Etwa indem sie den Menstruationszyklus verlängern, eine Veränderung des Hormonhaushaltes bewirken oder ein Einfluss auf Tumoren haben, die in Abhängigkeit zu Östrogenrezeptoren stehen.[71] In Studien zeigte Sojakonsum sowohl einen präventiven Effekt als auch positive Auswirkungen nach einer Brustkrebsdiagnose.[72][73] Eine Studie unter chinesischen Frauen zeigte dabei einen Dosiseffekt: 10 mg mehr Soja-Isoflavone am Tag reduzierten das Risiko an Brustkrebs zu erkranken um 3 %.[74] Das Deutsche Krebsforschungszentrum sah 2019 keine ausreichende Grundlage, um von einer schützenden Wirkung von Soja gegenüber Brustkrebs sprechen zu können.[75]
Frauen, die täglich mindestens 20 g Alkohol trinken, tragen ein um 30 % erhöhtes Risiko, an einem Mammakarzinom zu erkranken, möglicherweise wegen des höheren Sexualhormonspiegels.[65]
Geringe Iodaufnahme könnte ebenfalls eine Rolle spielen. In Ländern mit hohem Iodgehalt in der Nahrung (z. B. Japan) kommt es zu erheblich weniger Brustkrebsfällen als in Iodmangelgebieten. Neben dieser Korrelation werden auch konkretere Stoffwechselzusammenhänge vermutet.[76]
Ein weiterer Risikofaktor könnte Sonnen- bzw. Vitamin-D-Mangel sein.[77] Wenn (postmenopausale) Frauen zur Vorbeugung gegen Knochenbrüche Calcium und Vitamin D einnehmen, scheint deren Erkrankungsrisiko stark zu sinken.[78] Diese Studien werden sehr kontrovers diskutiert.[79] In einigen Fällen scheint es klare Anzeichen eines Publikationsbias zu geben.[80] In einer 2013 durchgeführten Metastudie konnte kein signifikanter Zusammenhang zwischen der Einnahme von Vitamin D und einem reduzierten Brustkrebsrisiko bei postmenopausalen Frauen festgestellt werden.[81]
Auch wer im jungen Erwachsenenalter viel rotes Fleisch zu sich genommen hat, hat einer Kohortenstudie zufolge ein erhöhtes Brustkrebsrisiko.[82]
Eine Metastudie aus dem Jahr 2017 kommt zu dem Schluss, dass der Konsum von gesättigten Fetten die Überlebenschance bei Brustkrebs negativ beeinflusst.[83]
Früherkennung und Screening
[Bearbeiten | Quelltext bearbeiten]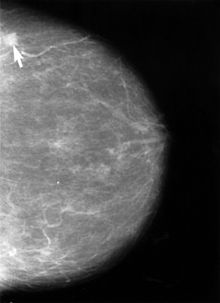

Etwa 80 bis 90 % aller Geschwulste in der weiblichen Brust wurden bisher von den Frauen selbst zufällig entdeckt. Diese tast- und sichtbaren Tumoren sind bei ihrer Entdeckung oft schon relativ groß und sind deshalb meist mit einer schlechten Prognose verbunden. Durch konsequente Früherkennung kleinerer, nicht tastbarer Tumoren könnte die Sterblichkeit großen Studien zufolge um 25 % gesenkt werden. Zur Früherkennung dienen Programme zur systematischen Selbstuntersuchung und der Mammasonographie sowie die Screening-Mammographie. Der medizinische Nutzen der Früherkennung ist umstritten. Eine 2013 veröffentlichte Meta-Studie in der Cochrane-Bibliothek von über 600.000 Frauen ergab keinen Überlebensvorteil für Frauen, die an der Früherkennung teilnahmen. Dies wurde auch in einer kanadischen Studie von 2014 an 45.000 Frauen, die 25 Jahre beobachtet wurden, bestätigt.[84]
Selbstuntersuchung
[Bearbeiten | Quelltext bearbeiten]Systematische Schulungen der Frauen zur Brust-Selbstuntersuchung sind in ihrem Nutzen umstritten. Nicht jede Brustkrebserkrankung führt zu einer tastbaren Geschwulst. Umgekehrt ist nur etwa jede zwölfte selbst ertastete Veränderung bösartig.[85] Studien zufolge senkt die systematische Selbstuntersuchung der Brust die Sterblichkeit nicht.[86][87] Die US-amerikanische Preventive Services Task Force (USPSTF) gibt wegen der unzureichenden Datenlage keine Empfehlung für oder gegen die Brustselbstuntersuchung.[88] Die kanadische Task Force on Preventive Health Services gab 2001 eine Empfehlung gegen die Selbstuntersuchung ab,[89] weil die Entdeckungsrate schlecht und falsch positive Befunde häufig seien.
Zum Erlernen der Selbstuntersuchung gibt es Brustmodelle aus Silikon, die verschiedene Knotentypen enthalten; beigefügt sind Begleitvideo und Anleitung. Jedoch ist dies in Deutschland keine Leistung der gesetzlichen Kranken- oder Pflegeversicherung.[90]
In Deutschland wird die Selbstuntersuchung von den medizinischen Fachgesellschaften empfohlen,[91] weil sie zur Bewusstseinsbildung der Frauen beitrage und so die eigentliche Früherkennung durch apparative Verfahren begünstige. Die Selbstuntersuchung, die monatlich zirka fünf bis sieben Tage nach Einsetzen oder kurz nach dem Ende der Regelblutung durchgeführt werden soll, erfolgt nach einem bestimmten, sich immer wiederholenden Muster. Bei ertasteten Auffälligkeiten sollen Frauen einen Facharzt aufsuchen.
Ärztliche Krebsfrüherkennung
[Bearbeiten | Quelltext bearbeiten]Die klinische Untersuchung der Brust durch einen Arzt ist Bestandteil des gesetzlichen Krebs-Früherkennungsprogramms ab dem 30. Lebensjahr. Für die Aussagefähigkeit der ärztlichen Tastuntersuchung gilt im Prinzip dieselbe Einschränkung wie für die Selbstuntersuchung.
Brustkrebsfrüherkennung durch Blinde
[Bearbeiten | Quelltext bearbeiten]Blinde Menschen verfügen in der Regel über einen überdurchschnittlich trainierten Tastsinn. Diese besondere Fähigkeit wird für die Früherkennung von Brustkrebs genutzt. Im Rahmen des in Nordrhein-Westfalen angesiedelten Modellprojektes „Discovering hands“ (Entdeckende Hände) wurde der Ausbildungskurs der Medizinischen Tastuntersucherin geschaffen.
Bildgebende Verfahren
[Bearbeiten | Quelltext bearbeiten]
Die Röntgen-Mammographie ist einer S3-Leitlinie von 2010 zufolge zurzeit die einzige für die Erkennung von Brustkrebsvorstufen oder frühen Tumorstadien allgemein als wirksam anerkannte Methode.[91] Die Mamma-Kernspintomographie ist möglicherweise überlegen, jedoch für ein Massenscreening zu teuer.[92] In Deutschland wurde deshalb ein qualitätsgesichertes Mammographie-Screening-Programm auf der Grundlage der „Europäischen Leitlinien für die Qualitätssicherung des Mammographie-Screenings“ für Frauen von 50 bis 69 Jahren aufgebaut. Dazu wurde Deutschland in 94 Regionen aufgeteilt, für die jeweils eine Screening-Einheit verantwortlich ist.[93] In den USA gab es 2002 die Empfehlung, das Mammographiescreening bereits mit 40 Jahren zu beginnen.[88]
Durch Dreifachbefundung und weitere Diagnostik soll erreicht werden, dass möglichst wenige gutartige Mammatumoren biopsiert oder gar entfernt werden. Die EUREF-Richtlinie verlangt, dass in mindestens 50 % der genommenen Gewebeproben bösartige Tumoren nachgewiesen werden können; in manchen Untersuchungsprogrammen werden bis zu 80 % erreicht.[94]
CAD-Systeme (Computer-assisted Detection) können den Radiologen bei der Auswertung der Mammographien unterstützen. Solche Untersuchungen können in den USA und den Niederlanden von den Krankenkassen bezahlt werden. Nach bisher veröffentlichten Studien verbessern die bislang verfügbaren Geräte die Erkennungsrate jedoch nicht.[95] In den europäischen Screeningprogrammen wird daher die Doppelbefundung durch zwei Ärzte (und durch einen dritten bei Auffälligkeiten) bevorzugt.
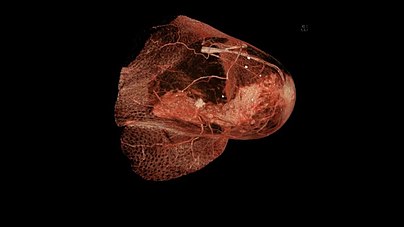
Die Mammographie ist bei Frauen mit dichtem Drüsengewebe in ihrer Aussagekraft begrenzt. Bei extrem dichtem Gewebe werden etwa 50 % der Brusttumoren mit der Mammographie nicht entdeckt. Dies betrifft in erster Linie jüngere Frauen, denen die Sonographie, im Einzelfall auch Kernspin-Mammographie, empfohlen wird. Nach systematischer Literaturrecherche bewertet der IGeL-Monitor (Initiator und Auftraggeber: MDS (Medizinischer Dienst des Spitzenverbandes Bund der Krankenkassen)) die Sonographie (Ultraschall) mit „unklar“, die Magnetresonanztomographie (MRT, Kernspin) mit „tendenziell negativ“. Die Wissenschaftler des IGeL-Monitors fanden in beiden Fällen keine Studien, die die Frage untersucht haben, ob die Untersuchungen Frauen tatsächlich davor bewahren können, an Brustkrebs zu sterben. Das gilt für die Untersuchungen zusätzlich zum Mammographie-Screening ebenso wie als Alternative zum Mammographie-Screening. Bei der MRT sind Schäden durch das Kontrastmittel möglich, das dabei gespritzt wird. Diese Bewertungen gelten für Frauen ab 40 Jahren, die kein erhöhtes Brustkrebs-Risiko haben.[96]
Brust-Computertomographie ist eine alternative Untersuchungsmethode, die sowohl mit als auch ohne Kontrastmittel möglich ist. Die Untersuchung verläuft kompressionsfrei. Da bei der Untersuchung nur der Brust-Bereich umfasst wird, soll nach Bedarf der Bereich der Achseln zusätzlich durch Sonographie untersucht werden. Die Strahlenbelastung liegt etwa im Bereich von der Mammographie.
Früherkennung durch Biomarker (Liquid Biopsy)
[Bearbeiten | Quelltext bearbeiten]Anfang 2019 wurde ein Liquid-Biopsy-Verfahren zur Brustkrebs-Frühdiagnostik durch die Universität Heidelberg veröffentlicht. Inzwischen hat die Staatsanwaltschaft Heidelberg hierzu Vorermittlungen aufgenommen. Uniklinikum und Spin-Off Heiscreen hatten den Test trotz fehlender Daten als „Meilenstein“ in der Brustkrebs-Frühdiagnostik bezeichnet. Finanzielle Verstrickungen von Ärzten, aber auch von Prominenten sollen die PR-Kampagne begünstigt haben.[97]
Auf Basis des innovativen Liquid-Biopsy-Verfahrens sei es möglich, Brustkrebs nicht-invasiv zu diagnostizieren. Das neue Verfahren erkenne eine Krebserkrankung anhand von Biomarkern aus dem Blut. Der Test könne bei Frauen aller Altersgruppen durchgeführt werden; besonders profitieren jüngere Frauen unter 50 Jahren und Frauen mit familiärer Hochrisikosituation für eine Brustkrebserkrankung, bei denen eine Mammographie beispielsweise aufgrund des dichten Brustdrüsengewebes wenig Aussage liefert oder aufgrund anderer Risikofaktoren herkömmliche bildgebende Verfahren kontraindiziert sind. Aktuelle Ergebnisse hätten bei 500 Brustkrebspatientinnen insgesamt eine Sensitivität von 75 Prozent gezeigt.[98] Die Arbeitsgemeinschaft Gynäkologische Onkologie (AGO) der Deutschen Krebsgesellschaft begrüßt ausdrücklich die Forschung zur Liquid-Biopsy-Technologie, warnt aber eindringlich vor einer verfrühten Anwendung des Testes. Eine wissenschaftliche Publikation liege noch nicht vor. Die klinischen Konsequenzen des Testes im Zusammenhang mit den Ergebnissen andere diagnostischer Verfahren, z. B. Mammographie und Sonographie müssen zunächst in Studien überprüft werden.[99]
Diagnose
[Bearbeiten | Quelltext bearbeiten]


Bei der Selbstuntersuchung oder bei der ärztlichen, klinischen Untersuchung kann ein neuer, unscharf begrenzter Tumor auffallen. Weitere Anzeichen sind Verhärtungen, Größen- und Umrissveränderungen der Brust im Seitenvergleich, verminderte Bewegung der Brust beim Heben der Arme, bleibende Hautrötung, Hauteinziehung oder Apfelsinenhaut (verdickte Haut mit eingezogenen Stellen), Einziehung oder Entzündung der Brustwarze, Absonderungen aus der Brustwarze. Knoten in der Achselhöhle können Lymphknoten-Metastasen entsprechen. Allgemeinsymptome bei weit fortgeschrittenen Erkrankungen sind u. a. Leistungsknick, ungewollter Gewichtsverlust oder Knochenschmerzen.
Ein lange Zeit unbehandeltes Mammakarzinom oder ein nicht kontrollierbares lokales Tumorrezidiv kann sich lymphangitisch oder subkutan infiltrierend soweit ausdehnen, dass die gesamte Brustwand panzerförmig ummauert erscheint; dieser Zustand wird als Cancer en cuirasse (Panzerkrebs) bezeichnet.[100]
Bildgebende Diagnostik
[Bearbeiten | Quelltext bearbeiten]Werden bei der Tast- oder Ultraschalluntersuchung Auffälligkeiten gefunden, folgt als nächste Untersuchung üblicherweise die Mammographie: Die Röntgenaufnahmen werden aus zwei Blickrichtungen (von der Seite und von oben) gemacht, bestimmte Veränderungen erfordern manchmal zusätzliche Aufnahmen. Die Galaktographie wird nur durchgeführt, wenn die Brustwarzen Sekret absondern. Als Ergänzung steht bei einer solchen Sekretion an einigen Zentren die Duktoskopie, eine Spiegelung der Milchgänge, zur Verfügung.
Umgekehrt werden mit der Mammographie entdeckte Veränderungen immer sonographisch weiter untersucht. Dabei werden gutartige Zysten erkannt. Die Kassenärztliche Bundesvereinigung schrieb 2003 hierfür Schallköpfe mit mindestens 5 MHz Frequenz vor.[101] Mittlerweile ist dieser Wert auf 7,5 MHz erhöht worden.[102]
Die Kernspintomographie der Brust (MR-Mammographie, MRT) wird zurzeit nur empfohlen für das invasive lobuläre Mammakarzinom zur Bestimmung der Resektions-Grenzen und allgemein bei Verdacht auf das Vorliegen mehrerer Tumorherde,[103] gegebenenfalls ist auch eine MRT-gesteuerte Biopsie möglich. Nach brusterhaltender Therapie kann die MRT eingesetzt werden, um zwischen narbigen Verdichtungen in der operierten Brust und neuem Tumorwachstum zu unterscheiden. Außerhalb der ambulanten Versorgung der gesetzlich krankenversicherten Patientinnen gibt es weitere Indikationen.
Die Positronen-Emissions-Tomographie ist derzeit keine Routinemethode, kann jedoch eingesetzt werden, um nach dem Primärtumor bzw. dessen Metastasen zu suchen, wenn dieser mit anderen Methoden nicht gefunden werden kann.
Knochenszintigramme, Computertomographien, Röntgenaufnahmen der Lunge, Sonographien der Leber und ggf. Kernspintomographien dienen dazu, nach Metastasen zu suchen, also die Ausbreitung der Erkrankung zu erkennen. Angesichts der Tatsache, dass die PET/CT bis auf die MRT-Hirn- und Brustuntersuchung genauer ist und zugleich auch andere Krebserkrankungen ausschließen kann, erscheint die PET/CT sinnvoller als Knochenszintigramme, Computertomographien, Röntgenaufnahmen der Lunge und Sonographien der Leber zusammen.
Bei der radiologischen Diagnostik kann zudem ein durch Exsudat entstandener Pleuraerguss, wie er beim Mammakarzinom auftreten kann, zuverlässiger als durch Perkussion erkannt werden.[104]
Gewebeentnahmen
[Bearbeiten | Quelltext bearbeiten]Wurde mit dem Ultraschall und der Mammographie ein Tumor diagnostiziert, wird dieser auf seine Gut- oder Bösartigkeit untersucht. Dazu werden jedem Tumor mittels Stanzbiopsie, in seltenen Fällen mittels Vakuumbiopsie, mehrere Gewebeproben entnommen und unter dem Mikroskop auf Krebszellen untersucht. Methode der Wahl für die Probenentnahme tastbarer und sonografisch sichtbarer Befunde ist die Stanzbiopsie, für im Kernspintomogramm sichtbare Befunde und Mikrokalzifikationen die stereotaktisch gestützte Vakuumbiopsie. Wurde der Tumor als bösartig erkannt, wird das Karzinom durch weitere Untersuchungen des entnommenen Gewebes näher bestimmt. Hierzu gehören der Status der Hormon- und HER2/neu-Rezeptoren sowie der Entartungsgrad.
Nach der Operation wird das aus der Brustdrüse entfernte Operationspräparat in der histologischen Untersuchung auf seine exakte Größe gemessen und das Gewebe auf weiteren Befall untersucht. Die entfernten Lymphknoten werden auf Metastasen geprüft. Die Größe des Karzinoms und die Anzahl der befallenen Lymphknoten sind für die TNM-Klassifikation, Prognose und weitere Behandlung von Bedeutung. Das Operationspräparat wird auch daraufhin vermessen, ob der Abstand zwischen dem Karzinom und dem verbliebenen, gesunden Gewebe ausreichend groß ist. Sollte dies nicht der Fall sein, kann eine Nachoperation nötig werden, damit ein angemessener Sicherheitsabstand zwischen gesundem und erkranktem Gewebe erreicht wird.
Genexpressionstests
[Bearbeiten | Quelltext bearbeiten]Mittlerweile gibt es eine Reihe Genexpressionstests für Patientinnen, die an frühem und hormonrezeptorpositivem Brustkrebs erkrankt sind. Sie untersuchen die Aktivitäten von verschiedenen Genen (Genexpression) in Gewebeproben eines Brustkrebstumors und helfen damit, diejenigen Patientinnen, die von einer adjuvanten Chemotherapie profitieren können und diejenigen Patientinnen, denen diese nebenwirkungsreiche Therapie erspart werden kann, voneinander zu unterscheiden. Die wichtigsten Genexpressionstests für Brustkrebs sind der EndoPredict, Oncotype DX und MammaPrint.
Klassifikation
[Bearbeiten | Quelltext bearbeiten]

Die Klassifikation eines Tumors ist dessen exakte Beschreibung auf der Grundlage der pathologischen Untersuchung einer Gewebeprobe oder des OP-Präparats und der entnommenen Lymphknoten.
Histologische Klassifikation
[Bearbeiten | Quelltext bearbeiten]Quelle:[105]
Der häufigste Tumortyp des Mammakarzinoms ist mit etwa 70–80 % ein Adenokarzinom ohne besondere Merkmale; dieser Tumortyp wird als invasives duktales Karzinom (IDC) bezeichnet. Seltener (in etwa 10–15 %) sind das invasive lobuläre Karzinom (ILC), das invasive tubuläre, muzinöse, medulläre, papilläre Karzinom (je etwa 2 %), gemischte und andere Tumortypen. Diese Tumortypen unterscheiden sich in ihrer klinischen Präsentation, den Befunden bei bildgebenden Untersuchungen, dem histologischen Ausbreitungsmuster und in der Prognose. Bei fast allen Tumortypen liegt auch eine nicht invasive (duktale oder lobuläre) Tumorkomponente vor, aus der sie hervorgegangen sind und die für die Größe der Operation mitentscheidend ist. Seltener geht das Mammakarzinom direkt aus gutartigen Erkrankungen hervor (von denen einige bei Mammatumor genannt sind, es handelt sich hier aber nicht um bösartige Tumorerkrankungen).
Als inflammatorisches Mammakarzinom bezeichnet man keinen histologischen Tumortyp, sondern eine sicht- und tastbare Veränderung, nämlich eine Rötung von mindestens einem Drittel der Brusthaut und Schwellung der Brust durch Infiltration der Lymphbahnen. Meist liegt ein lokal fortgeschrittener Befall der Brust und des umgebenden Lymphsystems vor.
Die nicht-invasiven Karzinome sind definiert als Karzinome innerhalb der Brustdrüsengänge (duktales Carcinoma in situ, DCIS) oder -läppchen (lobuläres Carcinoma in situ, LCIS bzw. Lobuläre Neoplasie, LN) ohne Stromainvasion. Eine Sonderstellung nimmt der Morbus Paget der Brustwarze (Mamille) ein, der auf einer nicht-invasiven Tumorausbreitung in die Mamillenhaut beruht und in der Regel mit einem intraduktalen Mammakarzinom, seltener auch mit einem invasiven Mammakarzinom assoziiert ist. Dieses Paget-Karzinom der Brustwarze kann klinisch mit einem Ekzem oder gutartigen Geschwür verwechselt werden.
Differenzierungsgrad
[Bearbeiten | Quelltext bearbeiten]Die histologischen Tumortypen werden anhand struktureller und zellulärer Eigenschaften sowie ihrer Kernteilungsrate unterteilt in drei Differenzierungsgrade (synonym Malignitätsgrad, englisch auch Grading). Die Einstufung des invasiven Karzinoms beruht auf den drei Kriterien Tubulusbildung (Ausbildung röhrenartiger Tumordrüsen), Kernpolymorphie (Vielgestaltigkeit der Zellkerne) und Mitoserate (Teilungsrate der Zellen) nach Elston und Ellis.[106] Je höher das Grading, desto ungünstiger ist das Verhalten der Tumorzellen. Man unterscheidet Tumoren mit Differenzierungsgrad 1, 2 oder 3 (G1 = gut differenziert, G2 = mäßig differenziert, G3 = gering differenziert).
TNM-Klassifikation
[Bearbeiten | Quelltext bearbeiten]Die TNM-Klassifikation beschreibt die Größe des Tumors (T), die Anzahl der befallenen Lymphknoten (N) und eine eventuelle Fernmetastasierung (M). Die tabellierte Kurzfassung der TNM-Klassifikation für Brustkrebs:
|
|
| ||||||||||||||||||||||||||||||||||||||
Stadieneinteilung
[Bearbeiten | Quelltext bearbeiten]Aus der TNM-Klassifikation (bzw. pTNM-Klassifikation, das „p“ steht für histologisch gesicherte Daten) des Mammakarzinoms ergibt sich die Stadiengruppierung nach UICC bzw. AJCC (TNM 6. Auflage. 2003) wie folgt:
| Stadium 0 | Tis | N0 | M0 |
| Stadium I | T1 | N0 | M0 |
| Stadium IIA | T0,T1 | N1 | M0 |
| T2 | N0 | M0 | |
| Stadium IIB | T2 | N1 | M0 |
| T3 | N0 | M0 | |
| Stadium IIIA | T0,T1,T2 | N2 | M0 |
| T3 | N1,N2 | M0 | |
| Stadium IIIB | T4 | N0,N1,N2 | M0 |
| Stadium IIIC | Jedes T | N3 | M0 |
| Stadium IV | Jedes T | Jedes N | M1 |
Hormonrezeptor- und HER2-Status
[Bearbeiten | Quelltext bearbeiten]Der Östrogenrezeptor- und Progesteronrezeptorstatus (ER- und PgR-Expression) wird ebenfalls histologisch, genauer immunhistologisch untersucht. Man bestimmt den Prozentsatz derjenigen Tumorzellen, an denen sich die Rezeptoren nachweisen lassen und errechnet aus Prozentsatz und der Färbeintensität einen 12-stufigen Immunreaktiven Score (IRS), oder den international gebräuchlicheren 8-stufigen Allred-Score.
| Färbeintensität (IS) | Positive Zellen (PP) | ||
|---|---|---|---|
| 0 | keine Reaktion | 0 | keine |
| 1 | schwache Reaktion | 1 | weniger als 10 % |
| 2 | mäßige Reaktion | 2 | zwischen 10 und 50 % |
| 3 | starke Reaktion | 3 | zwischen 51 und 80 % |
| 4 | mehr als 80 % | ||
| IRS | |
|---|---|
| 0–2 | negativ |
| 3–4 | schwach positiv |
| 6–8 | mäßig positiv |
| 9–12 | stark positiv |
Beim HER2-Rezeptor, der für die Entscheidung, ob eine Nachbehandlung mit Trastuzumab (auch in Kombination mit Pertuzumab und Docetaxel) sinnvoll ist, wird ein 4-stufiger Score angewandt, der sich nach der immunhistochemischen Färbeintensität richtet (ASCO-Empfehlung 2007[107]). Lassen sich keine Zellen anfärben, ist das Ergebnis negativ: Score 0. Auch der Score 1+ ist negativ, d. h. eine Behandlung mit Trastuzumab wäre ohne Effekt auf den Tumor. Bei einer mittleren Färbeintensität (Score 2) wird der Tumor mit dem FISH-Test nachuntersucht und anhand Vermehrung (Amplifikation) des HER2-Gens entschieden, ob es sich um einen HER2-positiven Tumor handelt.
| Positive Zellen | Membranfärbung | Färbeintensität | Score |
|---|---|---|---|
| keine | keine | keine | 0 |
| 1 % oder mehr | nicht komplett | schwach | 1+ |
| weniger als 10 % | vollständig | schwach bis mäßig | 1+ |
| 10 % oder mehr | vollständig | schwach bis mäßig | 2+ |
| 30 % oder weniger | vollständig | stark | 2+ |
| mehr als 30 % | vollständig | stark | 3+ |
Risikogruppen, Einteilung nach Ergebnissen der Konsensuskonferenzen in St. Gallen
[Bearbeiten | Quelltext bearbeiten]Die alle zwei Jahre in St. Gallen abgehaltene Konsensuskonferenz beschäftigt sich vor allem mit der adjuvanten Therapie. Um die Chemo- und Hormontherapie möglichst zielgerecht einsetzen zu können, werden der Empfehlung von 2007 folgend die operierten Patientinnen in drei Risiko-, besser Behandlungsgruppen eingeteilt:[108]
| Niedriges Risiko | Mittleres Risiko | Hohes Risiko | |
|---|---|---|---|
| Anzahl der befallenen Lymphknoten: |
keiner und alle folgenden Kriterien: | 1 bis 3 oder keiner, aber mindestens ein weiteres Kriterium: |
mehr als 4 oder 1 bis 3 und |
| Tumorgröße: | T1 (max. 2 cm) | T2 bis T4 (größer als 2 cm) | |
| Differenzierung: | G1 | G2 und G3 | |
| Tumoreinbruch: | Invasion in Gefäße | ||
| Hormonstatus: | ER/PR-positiv (Östrogen-/Progesteron-positiv) | ||
| HER2/neu-Status: | HER2/neu-negativ | HER2/neu-positiv | HER2/neu-positiv |
| Alter: | 35 Jahre und älter | oder jünger als 35 Jahre |
Molekulare Tumorklassifikation
[Bearbeiten | Quelltext bearbeiten]Anhand des Genexpressionsprofils, welches mit DNA-Microarrays aus dem Tumorgewebe gewonnen werden kann, kann man fünf verschiedene Hauptgruppen des Mammakarzinoms unterscheiden: Hormonrezeptorpositive Tumoren mit geringer bzw. höherer Aggressivität (genannt Luminal-A und Luminal-B, von lumen = Hohlraum der Milchgänge), HER2-positive Tumoren (erbB2-Phänotyp) und Hormonrezeptor- und HER2-negative Karzinome mit oder ohne Basalzell-Eigenschaften (basal-like und normal-like Phänotypen). Die zurzeit noch experimentelle molekulare Tumorklassifikation könnte in Zukunft eine bessere Abschätzung der Prognose und der voraussichtlichen Wirkung der adjuvanten Hormon- und Chemotherapie ermöglichen.[109]
Genexpressionsanalysen
[Bearbeiten | Quelltext bearbeiten]Eine zentrale Frage bei der Behandlung des operablen Mammakarzinoms ist die Frage, wie hoch das Risiko eines Wiederauftretens der Erkrankung (Rezidivrisiko) ist. Patientinnen mit hohem Rezidivrisiko sollten eine adjuvante Chemotherapie erhalten, während Patientinnen mit niedrigem Risiko die nebenwirkungsreiche Chemotherapie erspart bleiben sollte. Die in der Vergangenheit gehandhabte, auf rein klinischen Faktoren wie Tumorgröße, Menopausestatus, Alter etc. beruhende Abschätzung des Rezidivrisikos hat sich als ungenau erwiesen. Einige Patientinnen, die als „Niedrigrisiko“ klassifiziert wurden, erleiden trotzdem ein Rezidiv. Andererseits wird davon ausgegangen, dass viele Chemotherapien überflüssigerweise gegeben werden, d. h. viele Patientinnen wären auch ohne eine solche geheilt.[110]
Um eine genauere Vorhersage des Rezidivrisikos zu ermöglichen, wurden sogenannte Gensignaturen entwickelt, mit dem Ziel, das Risiko eines Wiederauftretens der Erkrankung genauer vorherzusagen. Dabei wird die Genexpression einer Reihe von Genen im Tumorgewebe gemessen und ein Punktwert (Risikoscore) berechnet, der das Risiko eines Rezidivs anzeigen soll. Ab einem gewissen Punktwert wird dann die Chemotherapie empfohlen.
Im Juli 2019 waren vier kommerzielle Genexpressionstests erhältlich. Alle vier Tests waren in klinischen Studien für Mammakarzinome im Frühstadium evaluiert worden.
| Oncotype DX (Genomic Health) |
Mammaprint (Agendia) |
EndoPredict (Myriad) |
ProSigna (Nanostring) | |
|---|---|---|---|---|
| Zahl der Gene | 21 | 70 | 11 | 50 |
| Tumor[A 1] | HR+, HER2- | HR+/-, HER2- | HR+, HER2- | HR+, HER2- |
| Menopausestatus[A 2] | prä und post | prä und post | prä und post | nur post |
| Nodalstatus[A 3] | N0 | N0, N+ | N0, N+ | N0, N+ |
| Evidenz | TAILORx-Studie[111] (9 Jahre prospektiv) |
MINDACT-Studie[112] (5 Jahre prospektiv)[110] |
prospektiv-retrospektive Daten aus verschiedenen Studien | prospektiv-retrospektive Daten aus verschiedenen Studien[110] |
- ↑ HR+/HR-: Hormonrezeptor-positiv/negativ, HER2-: HER2-negativ
- ↑ prämenopausal: Patientin befindet sich vor der Menopause, postmenopausal: Patientin befindet sich in bzw. nach der Menopause
- ↑ N0: kein Lymphknoten- (Nodal-)befall, N+: mit Lymphknotenbefall
Nach einer Entscheidung des Gemeinsamen Bundesausschusses (GBA) vom 20. Juni 2019 sollen die Kosten des Genexpressionstests Oncotype DX künftig durch die gesetzlichen Krankenkassen erstattet werden (Regelleistung).[110]
Therapie
[Bearbeiten | Quelltext bearbeiten]Zur Vereinheitlichung und Verbesserung der Krankenversorgung gibt es in Deutschland seit 2003 im Auftrag der Deutschen Krebsgesellschaft und der Deutschen Gesellschaft für Senologie von OnkoZert zertifizierte Brustzentren an Krankenhäusern[113] und seit 2004 ein Disease-Management-Programm für Brustkrebs, an dem sich auch niedergelassene Ärzte beteiligen können. Die gemeinsame Leitlinie der Stufe S3 der Deutschen Krebsgesellschaft und der medizinischen Fachgesellschaften ist für diese Programme die Orientierung zur Behandlung von Brustkrebs. Diese Leitlinie wird regelmäßig aktualisiert, zuletzt im Februar 2020.[103]
Die Strategie zur Brustkrebsbehandlung wird meist im Rahmen einer Tumorkonferenz geplant, an der sich Gynäkologen, internistische Onkologen, Radiologen, Strahlentherapeuten und Pathologen beteiligen. Die Einbindung der Patientin in die Entscheidungsfindung ist wie bei jeder eingreifenden medizinischen Maßnahme von großer Bedeutung (siehe informierte Einwilligung). Auch der deutsche Gesetzgeber spricht in der DMP-Richtlinie deutlich vom Status der aufgeklärten Patientin.[114]
Die Therapie der Brustkrebserkrankung soll im Frühstadium eine Heilung, beim metastasierten Karzinom eine Lebenszeitverlängerung und im Spätstadium eine Linderung der Krankheitsbeschwerden erreichen. Bei der Wahl der konkreten Therapie steht die Erhaltung der Lebensqualität im Vordergrund.[114][103] Darum wird neben den weiter oben beschriebenen Klassifikationen des Tumors auch die körperliche, psychosoziale und emotionale Situation der Patientin berücksichtigt. Eine „Standardtherapie“ gibt es nicht, die Berücksichtigung aller verschiedenen Faktoren führt zu einer individuellen Anpassung der Therapie an die Krankheit und an die jeweilige Patientin.[114][103]
Brustkrebs kann sich sehr schnell im Körper ausbreiten und wird daher schon in frühen Stadien mit einer systemischen (im ganzen Körper wirksamen) Therapie behandelt. Diese nach dem amerikanischen Chirurgen Bernard Fisher benannte „Fisher-Doktrin“ ist die Grundlage der Chemo- und Hormontherapie beim Brustkrebs.[115] Fast immer besteht die Behandlung heute aus einer Kombination verschiedener Therapieformen. Werden zusätzliche Maßnahmen vor einer Operation durchgeführt, werden sie als neoadjuvant bezeichnet, werden sie nach einer Operation eingesetzt, nennt man sie adjuvant.
Neoadjuvante Therapie
[Bearbeiten | Quelltext bearbeiten]In einigen Fällen wird eine Chemotherapie oder antihormonelle Therapie schon vor der chirurgischen Entfernung des Tumors durchgeführt.[116] Diese primäre, oder neoadjuvante Therapie hat einerseits das Ziel, den Tumor zu verkleinern, um eine vollständige Entfernung des Tumors oder sogar eine brusterhaltende Operation zu ermöglichen, andererseits kann an der mit den neoadjuvanten Verfahren erreichbaren Veränderung der Erfolg einer weiteren, adjuvanten Behandlung abgeschätzt werden. Standard ist die neoadjuvante Therapie beim inflammatorischen Karzinom und bei zunächst inoperablen (T4-)Tumoren. Die Chemotherapieschemata sind die gleichen wie bei der postoperativen Behandlung (siehe unten).
Operation
[Bearbeiten | Quelltext bearbeiten]Mit der Operation der Brustkrebserkrankung werden zwei Ziele verfolgt: Einerseits soll durch möglichst vollständige Entfernung der entarteten Zellen eine Ausbreitung (Metastasierung) der Tumorzellen in andere Körperregionen verhindert werden, sofern das noch nicht geschehen ist, andererseits soll ein Wiederauftreten der Krankheitszeichen an Ort und Stelle (ein Rezidiv) verhindert werden.
Brusterhaltende Chirurgie vs. Mastektomie
[Bearbeiten | Quelltext bearbeiten]






Eine brusterhaltende Therapie (BET) ist heute bei 60–70 % der Erkrankten möglich,[116] wenn die Relation zwischen der Tumorgröße und dem Brustvolumen günstig und der Tumor noch nicht in die Muskulatur oder Haut eingedrungen ist. Bei dieser Operation wird entweder der Tumor mit dem umliegenden Gewebe (Lumpektomie), ein größeres Segment oder ein ganzer Quadrant (Quadrantektomie) entfernt. Um ein kosmetisch ansprechendes Ergebnis zu erhalten, wird bei größerer Gewebeentfernung vor allem aus beiden unteren Quadranten eine sogenannte intramammäre Verschiebeplastik vorgenommen. Dabei wird die Brustdrüse ganz oder teilweise von Haut und Muskulatur gelöst und so verschoben, dass nach der Operation trotz des Gewebeverlustes eine ausgeglichene Brustform erhalten bleibt. Ist eine Verschiebeplastik nicht möglich, kann die Brust entweder direkt nach der Tumorentfernung oder nach Abschluss aller Behandlungen rekonstruiert werden.
Sollte eine Brusterhaltung nicht möglich sein, wird der gesamte Brustdrüsenkörper und ein Teil der darüber liegenden Haut entfernt (Ablatio, Mastektomie). Die Empfehlung zur Mastektomie wird ausgesprochen, wenn:
- der Tumor sehr groß ist (> 3 cm) oder den Brustmuskel infiltriert hat,
- ein inflammatorisches Karzinom diagnostiziert wurde,
- ein ausgedehnter Befall der Lymphgefäße der Brustdrüse nachgewiesen wurde,
- der Tumor ausgedehnte „Arme“ in die Milchgänge gebildet hat (Duktales in situ Karzinom),
- die gesamte Brustdrüse eine durch die Mammographie nachgewiesene Mikroverkalkung enthält,
- der Tumor trotz Nachoperation nicht mit einem ausreichenden Sicherheitsabstand zum gesunden Gewebe entfernt werden konnte,
- die Patientin dies wünscht. Manche Patientinnen entscheiden sich gegen die Möglichkeit zur brusterhaltenden Operation, um sich sicherer zu fühlen oder um die sonst notwendige Strahlentherapie zu vermeiden.
Die Empfehlung zur Mastektomie wird auch ausgesprochen, wenn ein multizentrisches (Tumorknoten in mehreren Quadranten) oder multifokales (mehrere Tumorknoten im selben Quadranten) Karzinom diagnostiziert wurde. Diese Empfehlung kann manchmal relativiert werden, wenn der Operateur alle Tumoren mit einem ausreichenden Sicherheitsabstand zum gesunden Gewebe entfernen kann.[119][120] Auch wenn eine Krebserkrankung schon in andere Organe metastasiert hat, kann der ursprüngliche Tumor schonender operiert werden, wenn das radikale chirurgische Vorgehen keinen Vorteil bringen würde.
Für die Versorgung von Frauen sowohl nach Brustamputation als auch nach brusterhaltender Operation (Chirurgie) oder auch nach Wiederaufbau mit unzureichendem kosmetischem Ergebnis werden Brustprothesen und Brustausgleichsteile aus Silikon eingesetzt. Frauen nach einer Brustoperation haben in der Regel Anspruch auf die Versorgung mit einer Brustprothese (auch Brustepithese genannt) bzw. einem Brustausgleichsteil, deren Kosten inkl. Beratung und Anpassung dann als medizinisches Hilfsmittel von den Krankenkassen übernommen wird. Als Halterung für die Prothese gibt es spezielle Prothesen-BHs und Prothesen-Badeanzüge mit eingearbeiteten Taschen, die zusammen mit dem Brustausgleich im Sanitätsfachgeschäft erhältlich sind.
Achsellymphknoten
[Bearbeiten | Quelltext bearbeiten]Die Lymphknoten der Achsel sind meist der erste Ort, an dem sich Metastasen bilden. Um diesen Befall zu erfassen, werden die Lymphknoten, zumindest einige von ihnen, bei der Operation oft mit entfernt.
Um die Folgeschäden (Lymphödem) so gering wie möglich zu halten, kann zunächst nur ein einzelner Lymphknoten entfernt und untersucht werden, wenn der Tumor in der Brust kleiner als 2 cm ist und die Achsellymphknoten nicht tastbar sind.[121] Dazu wird in die betreffende Brust ein Farbstoff oder ein Radionuklid injiziert, um den Lymphabfluss darzustellen. Der erste Lymphknoten, in dem das eingespritzte Material nachgewiesen werden kann, wird herausoperiert und untersucht. Nur wenn dieser sogenannte Wächterlymphknoten (sentinel node) von Tumorzellen befallen ist, werden weitere Lymphknoten der Achselhöhle ebenfalls entfernt (teilweise oder komplette Axilladissektion).
Nicht-invasive Tumorzerstörung
[Bearbeiten | Quelltext bearbeiten]2013 wurde in Rom erstmals ein Verfahren getestet, bei dem noninvasiv mittels Ultraschallwellen bei einer ambulanten Behandlung Tumorgewebe zerstört werden kann. Bei der anschließenden Operation konnten bei 10 von 12 Patientinnen mit Tumoren kleiner als 2 cm keine Tumorreste mehr gefunden werden.[122] Das Verfahren muss jedoch weiterhin getestet und optimiert werden.
Adjuvante Therapie
[Bearbeiten | Quelltext bearbeiten]Fast alle Patientinnen erhalten nach der Operation eine adjuvante (unterstützende) Behandlung.
Chemotherapie
[Bearbeiten | Quelltext bearbeiten]Nach der Operation folgt für viele Patientinnen mit höherem Rückfallrisiko eine Chemotherapie, um möglicherweise verbliebene Tumorzellen abzutöten. Die Notwendigkeit der Chemotherapie wird anhand des Tumortyps, des Stadiums und anderer Faktoren beurteilt. Wenn der Tumor hormonabhängig, kleiner als 2 cm und die Lymphknoten frei von Metastasen sind, kann in den meisten Fällen auf eine Chemotherapie verzichtet werden. Bei dieser Konstellation können mit einer antihormonellen Therapie ähnliche Ergebnisse erzielt werden (St. Gallen 2007).
Welche Chemotherapie verabreicht wird, hängt vom Zustand der Patientin und von der Klassifikation des Tumors ab, vor allem von der Risikogruppe nach der St.-Gallen-Empfehlung. Die Behandlung wird in mehreren Zyklen durchgeführt, beispielsweise insgesamt viermal im Abstand von drei Wochen oder sechsmal in Abstand von zwei Wochen. Der Zeitabstand zwischen den einzelnen Gaben soll dem Körper einerseits die Gelegenheit zur Regeneration geben, andererseits hofft man darauf, dass Mikrometastasen (ruhende Tumorzellen) bzw. Krebsstammzellen in den Erholungsphasen mit der Teilung beginnen und mit der erneuten Zuführung der Zytostatika zerstört werden können.
In der Regel werden die Zytostatika als Kombinationen eingesetzt. Die häufigsten Schemata sind zurzeit AC oder EC, FAC oder FEC. Wenn die Lymphknoten mit Metastasen befallen waren, wird eine Ergänzung der jeweiligen Kombination mit Taxanen (Paclitaxel und Docetaxel) empfohlen (St. Gallen, 2007). Das ältere CMF-Schema wird kaum noch verwendet. (A = Adriamycin, C = Cyclophosphamid, E = Epirubicin, F = Fluoruracil, M = Methotrexat, T = Taxane) Inzwischen werden Chemotherapien auch mit weiteren Therapien wie der zielgerichteten Antiangiogenese („Therapie des metastasierten Mammakarzinoms“, siehe unten) erfolgreich kombiniert.
Seit dem Juli 2019 werden durch die gesetzlichen Krankenkassen auch die Kosten eines Genexpressionstests übernommen, mit dem die Frage beantwortet werden kann, ob eine adjuvante Chemotherapie im Frühstadium eines operierten Mammakarzinoms erforderlich ist (→ Genexpressionsanalysen).
HER2/neu positive Tumoren
[Bearbeiten | Quelltext bearbeiten]Um das Risiko eines erneuten Auftretens der Erkrankung (Rezidiv) zu senken, wird bei HER2/neu positiven Tumoren in der Regel im Anschluss an die Chemotherapie ein Jahr lang die Behandlung mit dem HER2-Antikörper Trastuzumab durchgeführt („Antikörper-Therapie“, siehe unten), seltener auch ohne vorherige Chemotherapie.[123][124][125][126] Die Dauer und die Zusammensetzung der Chemotherapie wird vom Ausmaß der befallenen Lymphknoten mitbestimmt (St. Gallen 2007). Nach einer Trastuzumab Behandlung kann Neratinib für den gleichen Zweck eingesetzt werden.[127]
Bestrahlung
[Bearbeiten | Quelltext bearbeiten]Nach der brusterhaltenden Operation sollte eine Strahlentherapie der Brust erfolgen.[103] Sie senkt die Rezidivrate von 30 auf unter 5 %. Mikroskopisch kleine (nicht mit bloßem Auge erkennbare) Tumorreste können auch bei sorgfältigster Operation in der Brustdrüse verbleiben.
Auch nach einer Mastektomie wird zur Nachbestrahlung geraten, wenn der Tumor größer als 5 cm war (T3 oder T4), die Brustdrüse mehrere Tumoren enthielt oder der Tumor bereits in Haut oder Muskulatur eingedrungen war. Auch der Befall von Lymphknoten ist ein Anlass zur Nachbestrahlung der Brustwand, insbesondere bei mehr als drei befallenen Lymphknoten.
Das ehemalige Tumorgebiet soll bei Frauen unter 60 Jahren mit einer um 10–16 Gy höheren Dosis bestrahlt werden, damit sich an den Schnitträndern keine Rezidive ausbilden können.
Die Strahlentherapie beginnt zirka 4–6 Wochen nach der Operation und dauert sechs bis acht Wochen. Eine befürchtete Erhöhung koronarer Ereignisse als Langzeitfolge der Strahlenwirkung auf das Herz konnte nicht bestätigt werden, es gibt eine gewisse Risikoerhöhung, das absolute Risiko ist jedoch sehr gering und kann durch moderne Strahlentherapie eventuell weiter gesenkt werden.[128]
Antihormonelle Therapie
[Bearbeiten | Quelltext bearbeiten]Ist das Karzinom hormonsensitiv, wird zusätzlich eine Therapie mit Hormonantagonisten durchgeführt. Es gibt verschiedene, vom menopausalen Status der Frau und dem genauen Tumortyp abhängige Varianten.
Vor der Menopause
[Bearbeiten | Quelltext bearbeiten]Ende des 19. Jahrhunderts wurde ein möglicher Zusammenhang zwischen Brustkrebs und der Ovarialfunktion erkannt. Dies veranlasste Beatson 1895 eine „therapeutische Kastration“ vorzunehmen.[129] Eine chirurgische Ovariektomie oder radiotherapeutische Ausschaltung der Ovarfunktion wird nur noch selten vorgenommen. Studien zufolge genügt eine temporäre Ausschaltung der Hormonproduktion über zwei Jahre, die medikamentös erreicht werden kann.[116]
Bei Frauen, die noch die Periode haben, wird schon durch Chemotherapie die Hormonfunktion der Eierstöcke gestört.[130] Dieser Effekt richtet sich auch gegen die hormonabhängigen Tumorzellen und ist daher erwünscht. Frauen mit Kinderwunsch oder Frauen, denen das Risiko einer vorzeitigen Menopause zu groß ist,[131] können ihre Eierstöcke mit GnRH-Analoga (die die ovariale Produktion von Östrogen und Progesteron unterdrücken) vor der schädigenden Wirkung schützen und gleichzeitig die Hormonausschaltung bewirken. GnRH-Analoga werden in der Regel über zwei Jahre gegeben.[116]
Nach der Chemotherapie wird normalerweise ein Estrogen-Rezeptor-Modulator wie Tamoxifen, welcher die Anbindung des körpereigenen Östrogens an den Östrogen-Rezeptoren des Tumors verhindert, für 5 Jahre gegeben.[132] Aromatasehemmer sind vor der Menopause nicht angezeigt.
Nach der Menopause
[Bearbeiten | Quelltext bearbeiten]Ist die Patientin postmenopausal, erhält sie für in der Regel fünf Jahre entweder Tamoxifen oder einen Aromatasehemmer, welcher durch eine Enzymblockade die Bildung von Östrogen im Muskel- und Fettgewebe unterbindet. Neuere Studienergebnisse deuten an, dass die Aromatasehemmer wirksamer sind als das Tamoxifen, das heißt, die krankheitsfreie Überlebenszeit steigt an. In Studien wird der Aromatasehemmer manchmal sofort verwendet (upfront), in der Regelbehandlung erst nach zwei bis drei Jahren unter Tamoxifen (switch, deutsch ‚Wechsel‘), oder nach fünf Jahren (extended).[116] Die jeweiligen Nebenwirkungen der Substanzen müssen bei der Entscheidung berücksichtigt werden. Auf Grund der besseren Wirksamkeit sind Aromatasehemmer zu Therapiebeginn erste Wahl und werden entsprechend häufiger verordnet. Tamoxifen wird dagegen seit 2003 immer seltener verschrieben.[133] Eine weitere Möglichkeit besteht in der Gabe eines reinen Estrogen-Rezeptor-Antagonisten (Fulvestrant; Handelsname Faslodex), der von den Arzneimittelbehörden jedoch bisher nur bei fortgeschrittenem Brustkrebs zugelassen ist.[134]
Bei vielen Patientinnen mit hormonabhängigen Tumoren verliert Tamoxifen nach einigen Jahren seine Schutzwirkung (sogenannte Tamoxifenresistenz). Laborversuchen zufolge kann im Gegenteil sogar eine Beschleunigung des Zellwachstums eintreten.[135] Betreffende Frauen sollten besser mit anderen Substanzen behandelt werden. Es ist bislang aber noch nicht möglich, das Verhalten eines individuellen Tumors in dieser Beziehung vorauszusagen. Ein Hinweis könnte das gleichzeitige Auftreten einer HER2/neu- und AIB1-Expression an einem ER-positiven Tumor sein.[136]
Androgenrezeptorabhängige Tumortypen
[Bearbeiten | Quelltext bearbeiten]Die meisten Mamma-Karzinome besitzen auch Rezeptoren für das männliche Geschlechtshormon Testosteron und andere Androgene Hormone. Bei ER+ Tumortypen wird der Anteil der AR+ Tumoren mit über 80 % angegeben, bei den „dreifach-negativen“ Tumortypen (Triple-negative breast cancer, TNBC) wird der Anteil mit etwa 10–50 % geschätzt.
Abhängig vom Estrogenrezeptorstatus kann Testosteron eine wachstumshemmende Wirkung bei ER+ Tumoren oder eine wachstumstreibende Wirkung bei ER-/PR-Tumortypen entfalten. Der Androgenrezeptor reagiert teilweise auch mit anderen Androgenhormonen und Progestinen.
Speziell für AR+/ER-/PR-Tumortypen in lokal fortgeschrittenem oder metastasiertem Stadium wurde zwischen 2007 und 2012 die Behandlung mit dem Antiandrogen Bicalutamid in einer Phase II Studie mit gutem Erfolg erprobt.[137]
Da der Patentschutz von Bicalutamid (Casodex) ausgelaufen ist, wird inzwischen das neuere Enzalutamid für diesen Einsatzbereich getestet, bis jetzt sind jedoch nur in vitro Experimente bekannt.[138]
Historisch belegt ist ferner der Einsatz von Testosteron bei ER+ Tumortypen, die erzielten Ergebnisse waren in etwa vergleichbar mit Tamoxifen, jedoch mit stärkeren Nebenwirkungen verbunden. Ein ähnlicher Wirkungsmechanismus wird teilweise bei der experimentellen Behandlung mit Progestinen vermutet.
Antikörper
[Bearbeiten | Quelltext bearbeiten]Etwa ein Viertel aller Mammakarzinome weisen eine Überexpression des HER2/neu-Rezeptors auf. Der Nachweis dieses Rezeptors steht für einen aggressiven Krankheitsverlauf und eine ungünstige Prognose, ist aber auch Bedingung für die Behandlung (Krebsimmuntherapie) mit dem Antikörper Trastuzumab. Neben der alleinigen Verabreichung von Trastuzumab wird dieser auch in Kombination mit dem monoklonalen Antikörper Pertuzumab und dem Zytostatikum Docetaxel eingesetzt.[139]
1998 wurde der Wirkstoff (Handelsname: Herceptin) in den USA und 2000 in der Europäischen Union zunächst für Patientinnen mit metastasiertem Brustkrebs zugelassen. Trastuzumab ist ein monoklonaler Antikörper gegen den Wachstumsrezeptor HER2/neu auf der Zelloberfläche von Krebszellen. Studien ergaben, dass mit dieser sogenannten gezielten Krebstherapie (targeted therapy) das Risiko eines Rezidivs (Wiederauftretens) um etwa 50 % gemindert werden konnte. Viele klinische Studien zeigen, dass auch Frauen ohne Metastasen profitieren. Die HER2-Antikörpertherapie kann Rückfälle verhindern und so zur Heilung beitragen.[123][140][141][124][125] Seit 2006 ist Trastuzumab deshalb auch für die adjuvante Therapie zugelassen.
Therapie des metastasierten Mammakarzinoms
[Bearbeiten | Quelltext bearbeiten]Fernmetastasen verschlechtern die Prognose rapide, da in der Regel bei Vorliegen einer sichtbaren Fernmetastase multiple Mikrometastasen vorhanden sind. Deshalb richtet sich die Behandlung auf die Lebenszeitverlängerung und den Erhalt einer angemessenen Lebensqualität mit einer langfristigen Stabilisierung der körperlichen und psychischen Verfassung. Brustkrebs bildet ausgesprochen häufig Knochenmetastasen.[142]
Rezidive und Metastasen können operativ entfernt oder mit Strahlentherapie behandelt werden. Trotz der Nebenwirkungen kann unter Umständen auch mit der Verabreichung einer Chemo-, Hormon- oder durch eine gezielte Krebstherapie eine Erhöhung der Lebensqualität und eine Verlängerung der Zeit bis zum Fortschreiten der Erkrankung (Progressionsfreies Überleben) erreicht werden. Das zur Gruppe der Taxane gehörende Paclitaxel-Albumin (Handelsname: Abraxane) ist – in Monotherapie – indiziert für die Behandlung von metastasierendem Mammakarzinom bei erwachsenen Patienten, bei denen die Erstlinientherapie für metastasierende Krankheit fehlgeschlagen ist und für die eine standardmäßige Anthracyclin-enthaltende Therapie nicht angezeigt ist.
Zusätzlich zu den bei der adjuvanten Therapie eingesetzten Wirkstoffen kommt beim HER2/neu-positiven metastasierten Mammakarzinom auch der Tyrosinkinase-Inhibitor Lapatinib zum Einsatz. Metastasierte HER2/neu-negative Tumoren können seit 2007 mit dem Angiogenese-Hemmer Bevacizumab behandelt werden. Diese gezielte Krebstherapie kann in Kombination mit einer Chemotherapie aus Paclitaxel oder Docetaxel angewendet werden. Studien zu weiteren Kombinationsmöglichkeiten laufen zurzeit.[143] Durch die Antiangiogenese wird die vom Tumor ausgelöste Neubildung von Blutgefäßen verhindert. Infolgedessen wird der Tumor nicht mehr ausreichend versorgt und die Tumorzellen sollen dadurch zugrunde gehen.
Eribulin (Handelsname: Halaven) ist ein nichttaxanbasiertes, hochwirksames neues Zytostatikum (Zulassung in den USA im November 2010; in Europa im März 2011), das in Monotherapie für die Therapie von stark vorbehandelten Patientinnen mit lokal fortgeschrittenem oder metastasiertem Brustkrebs eingesetzt wird.[144]
Wenn der Krebs in seiner Ausbreitung so weit fortgeschritten ist, dass er nicht mehr zurückgedrängt werden kann, richtet sich die Behandlung vor allem auf die Beherrschung von Schmerzen und anderen Krankheitsbeschwerden. Zur Palliativmedizin gehört die psychosoziale Betreuung und eine Schmerzbehandlung, die schnell und vollständig erfolgen sollte und eine frühzeitige und ausreichende Gabe von Opiaten einschließt, siehe WHO-Stufenschema.
Nachsorge
[Bearbeiten | Quelltext bearbeiten]Die Nachsorge der behandelten Patienten dauert in der Regel fünf Jahre und richtet sich zumeist nach den Leitlinien der Deutschen Krebsgesellschaft. Auf Nebenwirkungen der Strahlentherapie (Lymphödem, Lungen- oder Herzprobleme), der Chemotherapie (Blutbildveränderungen, Organschäden) und der Hormontherapie (Thrombosen, Osteoporose) muss besonders geachtet werden. Neben der Befragung und klinischen Untersuchung soll in den ersten drei Jahren, da hier die meisten Rezidive auftreten, alle sechs Monate eine Mammographie angefertigt werden. Ab dem vierten Jahr erfolgt die Mammographie – ebenso wie bei der zweiten, gesunden Brust von Anfang an – jährlich. Gemäß S3-Leitlinie kehrt die Patientin nicht mehr zu einem zweijährigen Intervall oder in das Screening Programm zurück. Zur Verlaufskontrolle können in der Blutuntersuchung die Tumormarker CA 15-3 und CEA bestimmt werden, was allerdings nicht in den Richtlinien vorgesehen ist und meistens eher bei konkretem Verdacht der Fall ist. Es muss bei jeder einzelnen Patientin sehr sorgfältig abgewogen werden, ob die Nachsorge in der hier angegebenen Form tatsächlich durchgeführt werden soll; jede kleine nachgewiesene Veränderung kann eine erhebliche psychische Belastung nach sich ziehen, die wiederum die Lebensqualität entscheidend beeinflussen kann.
Hilfreich, als begleitende Heilmethode, für die Rehabilitation nach einer Brustkrebserkrankung und anschließender erfolgreicher Behandlung, ist zudem körperliche Aktivität.[145]
Für eine einheitliche Qualität bei der Nachbetreuung bieten die deutschen gesetzlichen Krankenkassen seit 2004 das Disease-Management-Programm „Brustkrebs“ an. Die teilnehmenden Ärzte orientieren sich bei der Therapie an den jeweils aktuellen Leitlinien zur Behandlung und Nachsorge des Brustkrebses. Eine Teilnahme ist bei allen Ärzten möglich, die sich diesen qualitätssichernden Programmen angeschlossen haben. Für die Patientinnen bedeutet die Teilnahme an diesem Programm eine Einschränkung der freien Arztwahl.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Entzündliche Brustleiden wie Abszesse wurden bereits in frühester Zeit mit dem Messer gespalten.[146] Die ersten Dokumentationen von Brustkrebserkrankungen stammen aus der Zeit von 2650 v. Chr. aus dem Alten Ägypten. Zu dieser Zeit wurden sie mit einem Brenneisen behandelt. Im Papyrus Edwin Smith (um 1600 v. Chr.) wurden acht Brustkrebserkrankungen beschrieben, auch die eines Mannes,[147] welche ebenfalls durch Kauterisation behandelt wurden. Der Papyrus Ebers enthält eine Beschreibung von Brustkrebs. Die Krebserkrankungen der Brust galten zur damaligen Zeit als nicht heilbar.[148][149][150]
Auch im Corpus Hippocraticum wurde der Fall eines Mammakarzinoms geschildert.[151] Von einer chirurgischen Behandlung tiefliegender Tumorerkrankungen wurde dort abgeraten, da nicht operierte Patienten länger lebten.[152]
Der griechische Arzt Galen sah Brustkrebs als Folge einer Säftestörung und damit als systemische Erkrankung, eine Krankheit des ganzen Organismus, an.[148][149] Als Mittel zur Behandlung wurden bis in das Mittelalter unterschiedlichste Rezepturen genutzt, um den als Ursache angesehenen eingedickten Körpersaft „Galle“ zu verflüssigen und abzuführen. Bestandteile waren, unter anderem, Blei- und Zinkkarbonat, Rosenöl und Hirschkot.[153] Die im Mittelalter durchgeführten Ätztherapien bei Carcinoma mammae oder dafür gehaltenen Brusterkrankungen wurden auch im 19. Jahrhundert noch durchgeführt, etwa mit Arsenik, Jod, Quecksilberpräpataten, Chlorzink[154] und Chlorkalipräparaten.[155]
Die erste Operation bei Brustkrebs soll Leonidas aus Alexandria um 100 n. Chr. durchgeführt haben. Zur Blutstillung und Entfernung von Tumorresten nutzte er ein Brenneisen.[153] Andreas Vesalius empfahl um 1543 bei Brustkrebs eine Entfernung der Brust (Mastektomie), bei welcher er jedoch eine Blutstillung mit Nähten der Kauterisation vorzog.[149]

Der französische Chirurg Jean-Louis Petit (1674–1750) legte das erste Konzept zur operativen Behandlung von Brustkrebs vor, welches jedoch erst 24 Jahre nach seinem Tode veröffentlicht wurde.[156] Sein Kollege Henry François Le Dran (1685–1770) meinte 1757, dass der Brustkrebs zumindest am Anfang lokaler Natur wäre. Erst wenn er sich seinen Weg in die Lymphbahnen geschaffen habe, sei die Prognose für die Patientin schlecht. Er entfernte daher die komplette Brust mitsamt den Lymphknoten der Achselhöhle.[156] Auch der schottische Chirurg Benjamin Bell (1749–1806) erkannte die Bedeutung einer Entfernung der Lymphknoten aus der Achselhöhle.[157]
Rudolf Virchow (1821–1902) konnte 1840 nachweisen, dass sich die Erkrankung aus den Epithelzellen entwickelt und sich entlang der Faszien und Lymphbahnen ausbreitet. Damit wandelte sich die Sicht vom Brustkrebs, welcher jetzt eher als lokale Erkrankung betrachtet wurde.[149][156]
Im Jahr 1867 stellte Charles H. Moore fest, dass die Ursache für ein Krebsrezidiv die unvollständige Entfernung des Primärtumors ist, und forderte daher bei Brustkrebs das benachbarte Gewebe (Haut, Lymphknoten, Fett, Pectoralismuskel) mitzuentfernen. Richard von Volkmann entfernte 1875 dementsprechend die Pectoralisfaszie mit.[158]
Diesem Konzept folgte auch William Stewart Halsted (1852–1922), der 1882 die erste radikale Mastektomie mit Entfernung der Faszie, der Brustmuskeln (Musculus pectoralis major, später auch in Anlehnung an eine von Willy Mayer vor der New Yorker Medizinischen Akademie vorgetragenen Methode den Musculus pectoralis minor[159]) und der Achsellymphknoten durchführte.[160] Für die damaligen Verhältnisse konnte damit eine lokale Tumorkontrolle mit einer 5-Jahres-Lokalrezidivrate von sechs Prozent erreicht werden.[161] Im deutschsprachigen Raum war Josef Rotter (1857–1924) Vorreiter dieser zum Standard gewordenen Methode, die er ab 1889 bei seinen Patientinnen durchführte.[162]
1874 beschrieb der englische Chirurg James Paget (1814–1899) eine ekzemartige Veränderung der Brustwarze mit angrenzendem duktalen Adenokarzinom, welche später als Morbus Paget bezeichnet wurde.[149]
Bis etwa 1884 glaubten manche Ärzte, dass Brustkrebs durch eine „Impfung“ mit Erysipelerregern erfolgreich behandelt werden könne.[155][163] Albert Schinzinger empfahl 1889 zur Behandlung inoperabler Mammakarzinom die Kastration.[164] Der schottische Chirurg George Thomas Beatson erkannte 1895, dass die Entfernung der Eierstöcke bei einer seiner Patientinnen den Brusttumor schrumpfen ließ.[148][149] 1897 wurde Brustkrebs erstmals bestrahlt.[153] Nachdem Hormone auch synthetisch hergestellt werden können, wurden auch endokrine Therapien[165] vermehrt eingesetzt.[129] Im Jahr 1927 wurde in Deutschland über die erste brusterhaltende Operation beim Mammakarzinom berichtet.[166]
1948 veröffentlichten David H. Patey und W. H. Dyson eine etwas weniger radikale Operationsmethode als Rotter und Halsted mit gleich guten Ergebnissen, bei welcher die Brustmuskeln erhalten bleiben konnten.[167] Sie wird heute noch als modifiziert-radikale Mastektomie nach Patey bezeichnet. Ein weiterer Rückgang der operativen Radikalität begann mit Robert McWhirter, der 1948 nach einfacher Mastektomie eine Strahlentherapie durchführte.[168] Einige Jahre nach der Entdeckung der Röntgenstrahlen wurden diese ab etwa 1900[169] auch zur Behandlung, von Brustkrebs eingesetzt, insbesondere zur (neoadjuvanten bzw. adjuvanten) Vor- oder Nachbestrahlung.[170][171]
Mit den Arbeiten von Bernhard und E. R. Fisher setzte sich in den 1960er Jahren die Auffassung durch, dass das Mammakarzinom schon im Frühstadium eine im Körper gestreute Erkrankung sein kann und die Lymphknoten keine Barriere gegen eine Ausbreitung im Körper darstellen. Vielmehr wurde der Befall der Lymphknoten als Indikator für eine systemische Ausbreitung angesehen. Die Lymphknotenentfernung hätte folglich nur prognostische und keine therapeutische Bedeutung.[172] Daher wurde das gängige Konzept der Operation und Strahlentherapie um eine anschließende Chemotherapie ergänzt, um auch Mikrometastasen zu vernichten.[173] Ab 1969 erfolgte die Chemotherapie als Kombination mehrerer Präparate mit Verbesserung der Wirksamkeit.[153]
Seit den 1970er Jahren werden Mammakarzinome zunehmend brusterhaltend operiert. Die Sentinel- oder auch Wächter-Lymphknoten-Entfernung erspart seit Ende des 20. Jahrhunderts oft die vollständige Entfernung der Lymphknoten aus der Achselhöhle. Damit wurde die operative Radikalität weiter reduziert.[156]
Eine Forschergruppe um den US-Amerikaner J. M. Hall entdeckte 1990 das, später BRCA1 benannte, Brustkrebs-Gen.[174] 1994 wurde mit BRCA2 ein zweites Brustkrebsgen erkannt.[175][176]
Die 1985 von der American Cancer Society gestartete Initiative Brustkrebsmonat Oktober findet wachsende Beachtung in den Industrieländern. 2011 wurde der BRA Day ins Leben gerufen.
Brustkrebszeichen in der Kunst
[Bearbeiten | Quelltext bearbeiten]In der medizinischen Fachliteratur wurde wiederholt über Brustkrebsanzeichen in historischen Bildern diskutiert. Im 16. Jahrhundert stellte Michelangelo in seinem berühmten Deckengemälde in der Sixtinischen Kapelle eine Frau dar, die an ihrer rechten Brust deutliche Veränderungen im Sinne einer Brustkrebserkrankung zeigt[177][178]. Die Abbildung findet sich in der ersten Szene des Deckengemäldes Die Sintflut aus dem Jahr 1508. Anzeichen wie ein sich andeutender Tumor, Größen- und Umrissveränderungen der Brust im Seitenvergleich, Hautrötung, Hauteinziehung oder Apfelsinenhaut finden sich auch beispielsweise in Werken von Raffael, Rembrandt van Rijn und Rubens.[179][180][181][182] Ob es sich bei den dargestellten Veränderungen allerdings tatsächlich um Brustkrebs handelt, lässt sich jedoch nicht beweisen und wurde daher auch angezweifelt.[183]
- Beispiele für Brustkrebszeichen in der Kunst
-
Michelangelo (1475–1564): Ausschnitt aus „Die Sintflut“
-
Raffael Sanzio (1483–1520): „Porträt einer jungen Frau“ („La Fornarina“)
-
Peter Paul Rubens (1577–1640): „Die drei Grazien“
-
Rembrandt van Rijn (1606–1669): „Bathseba mit Davids Brief“
-
Detail Michelangelo
-
Detail Raffael
-
Detail Rubens
-
Detail Rembrandt
Literatur
[Bearbeiten | Quelltext bearbeiten]Leitlinien
- Interdisziplinäre S3-Leitlinie für die Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. Version 4.1 – September 2018. AWMF-Registernummer: 32-045OL. Herausgeber: Leitlinienprogramm Onkologie der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF), Deutschen Krebsgesellschaft e. V. (DKG) und Deutschen Krebshilfe (DKH). Federführende Fachgesellschaften: Deutsche Gesellschaft für Gynäkologie und Geburtshilfe (DGGG) Langversion (PDF) Kurzfassung (PDF)
- AGO-Leitlinie (Arbeitsgemeinschaft Gynäkologische Onkologie): Empfehlungen gynäkologische Onkologie, Kommission Mamma Leitlinie 2018 (PDF)
- ESMO-Guidelines (European Society of Medical Oncology): E. Senkus, S. Kyriakides, S. Ohno, F. Penault-Llorca, P. Poortmans, E. Rutgers, S. Zackrisson, F. Cardoso on behalf of the ESMO Guidelines Committee: Primary breast cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. In: Annals of Oncology. Band 26, Supplement 5, 1. September 2015, S. v8–v30.
- NCI-Guidelines (National Cancer Institute, USA): Version für Patienten, Version für medizinisches Fachpersonal
- NCCN-Guideline (National Comprehensive Cancer Network, USA). William J Gradishar, Benjamin O Anderson, Ron Balassanian u. a.: NCCN Guidelines Insights Breast Cancer, Version 1.2017. Featured Updates to the NCCN Guidelines. In: Journal of the National Comprehensive Cancer Network. Band 15, Heft 4, 2017, S. 433–451.
Lehrbücher
- David J. Winchester, David P. Winchester, Clifford A. Hudis, and Larry Norton (Hrsg.): Breast Cancer (Atlas of Clinical Oncology). B.C. Decker, Hamilton, Ontario 2006, ISBN 1-55009-272-3 (eingeschränkte Vorschau in der Google-Buchsuche).
- Orlando Silva, Stefano Zurrida (Hrsg.): Brustkrebs: Diagnostik und Therapie. Urban & Fischer, München 2007, ISBN 978-3-437-24260-1 (eingeschränkte Vorschau in der Google-Buchsuche).
- Anne C. Regierer, Kurt Possinger: Mammakarzinom: Manual Diagnostik und Therapie. Deutscher Ärzte-Verlag, 2005, ISBN 3-7691-0487-0 (eingeschränkte Vorschau in der Google-Buchsuche).
- Manuela Eicher, Sara Marquard (Hrsg.): Brustkrebs. Lehrbuch für Breast Care Nurses, Pflegende und Gesundheitsberufe. Huber, Bern 2008, ISBN 978-3-456-84556-2.
Ratgeber
- Hermann Delbrück: Brustkrebs – Rat und Hilfe für Betroffene und Angehörige. 8. Auflage. Kohlhammer, Stuttgart 2009, ISBN 978-3-17-020469-0.
- Heinrich Schmidt-Matthiesen, Gunther Bastert, Diethelm Wallwiener (Hrsg.): Gynäkologische Onkologie. 7. Auflage. Schattauer, Stuttgart 2002, ISBN 3-7945-1974-4.
- Verschiedene Informationsbroschüren zum Thema „Brustkrebs“ der Deutschen Krebsgesellschaft. 2019 (krebsgesellschaft.de [PDF]).
- Clemens Unger: Metastasierendes Mammakarzinom: Patientinnen fragen – Ärzte antworten. Georg Thieme Verlag, Stuttgart 2004, ISBN 3-13-133561-0 (eingeschränkte Vorschau in der Google-Buchsuche).
- Marius Wunderle: Familiärer Brust- und Eierstockkrebs. Facharzt Sprechstunde. W. Zuckschwerdt, München 2019, ISBN 978-3-86371-244-0.
Dokumentationen
- Renate Zeun: Betroffen – Bilder einer Krebserkrankung. Verlag Volk und Gesundheit, Berlin 1990, ISBN 3-333-00380-5 (Renate Zeun studierte Fotografie, als sie an Brustkrebs erkrankte und operiert werden musste. Dieses Buch enthält ihre Diplom-Arbeit mit ihren eigenen Fotos ihrer Erkrankung und ihrem Umgang damit).
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Brustkrebs – Informationen bei Gesundheitsinformation.de (Online-Angebot des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen)
- Patientenleitlinien Brustkrebs. Website des Leitlinienprogrammes Onkologie.
- Brustkrebs/Mammakarzinom und Brustkrebs: Basis-Infos für Patientinnen und Angehörige. Website der Deutschen Krebsgesellschaft.
- Die blauen Ratgeber: Brustkrebs. (PDF; 2,9 MB) Stiftung Deutsche Krebshilfe, Stand 1/2019.
- Weibliche Sexualität bei Brustkrebs. (PDF; 0,7 MB) Krebsliga Schweiz.
- Brustkrebs (Mammakarzinom). Website des Krebsinformationsdienstes des Deutschen Krebsforschungszentrums.
- Brustkrebs (Mammakarzinom). Website des Zentrums für Krebsregisterdaten des Robert Koch-Instituts.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ M. A. Roubidoux: Breast cancer, male. In: Emedicine. Stand vom 24. September 2008.
- ↑ K. Rhiem, R. K. Schmutzler: Risikofaktoren und Prävention des Mammakarzinoms. In: Onkologe. Band 21, 2015, S. 202–210. doi:10.1007/s00761-014-2837-5
- ↑ a b c d e krebshilfe.de abgerufen am 10. Oktober 2019
- ↑ br.de abgerufen am 6. Februar 2021
- ↑ Melina Arnold, Eileen Morgan, Harriet Rumgay, Allini Mafra, Deependra Singh: Current and future burden of breast cancer: Global statistics for 2020 and 2040. In: The Breast. Band 66, ISSN 0960-9776, S. 15–23, doi:10.1016/j.breast.2022.08.010, PMID 36084384 (thebreastonline.com [abgerufen am 21. September 2022]).
- ↑ Alexander Katalinic, Carmen Bartel: Epidemiologie Mammakarzinom. Universität Lübeck, 2006. (krebsregister-sh.de ( vom 6. Oktober 2007 im Internet Archive; PDF))
- ↑ WHO/IARC: World Cancer Report. Lyon 2003 ( vom 1. Februar 2008 im Internet Archive)
- ↑ J. Eucker, P. Habbel, K. Possinger: Metastasiertes Mammakarzinom: Differenzierte, möglichst zielgerichtete medikamentöse Therapie. In: Onkologe, Band 19, 2013, S. 487–493. doi:10.1007/s00761-013-2450-z
- ↑ Brustkrebs bei Frauen häufigste Todesursache. In: Ärzte Zeitung, 1. September 2008.
- ↑ R. H. Johnson, F. L. Chien, A. Bleyer: Incidence of breast cancer with distant involvement among women in the United States, 1976 to 2009. In: JAMA. Band 309, Nummer 8, Februar 2013, S. 800–805, doi:10.1001/jama.2013.776. PMID 23443443.
- ↑ a b Zusammenstellung der Daten des Statistischen Bundesamtes Deutschland aus den Jahren 2003 bis 2006, Fachserie 12, Reihe 4, Datensatz: Todesursache Mammakarzinom (PDF)
- ↑ a b rme: Brustkrebs ist bei Männern anders. In: aerzteblatt.de. 15. Dezember 2014, abgerufen am 27. Dezember 2014.
- ↑ krebshilfe.de abgerufen am 10. Oktober 2019.
- ↑ Jael Backe: Brustkrebs beim Mann. In: Deutsches Ärzteblatt. Band 99, Nr. 17, 26. April 2002, S. A-1168 / B-970 / C-913 (aerzteblatt.de).
- ↑ Hui Miao, Helena M. Verkooijen, Kee-Seng Chia, Christine Bouchardy, Eero Pukkala, Siri Larønningen, Lene Mellemkjær, Kamila Czene, Mikael Hartma: Incidence and Outcome of Male Breast Cancer: An International Population-Based Study. In: Journal of Clinical Oncology, Band 29, 2011, S. 4381–4386, doi:10.1200/JCO.2011.36.8902.
- ↑ Breast Cancer in Men. In: NEJM. Abgerufen am 17. Dezember 2018 (englisch).
- ↑ brustkrebs-beim-mann.de Website des Netzwerkes.
- ↑ Brustkrebs beim Mann. krebsinformationsdienst.de
- ↑ Erblicher Brustkrebs – Wenn der Krebs in den Genen liegt. DKG, abgerufen am 8. März 2023.
- ↑ A. Antoniou, P. D. Pharoah, S. Narod u. a.: Average risks of breast and ovarian cancer associated with BRCA1 or BRCA2 mutations detected in case Series unselected for family history: a combined analysis of 22 studies. In: Am J Hum Genet. Band 72, 2003, S. 1117–1130. PMID 12677558.
- ↑ M. R. Stratton, N. Rahman: The emerging landscape of breast cancer susceptibility. In: Nature Genetics. Band 40, Nr. 1, 2008, S. 17–22. PMID 18163131.
- ↑ R. Schmutzler, A. Meindl: Das hereditäre Mammakarzinom: Genetik und Prävention. In: Aktuelle Empfehlungen zur Therapie primärer und fortgeschrittener Mammakarzinome. (Hrsg. C. Thomssen für die Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e. V.). Zuckschwerdt-Verlag, 2007, ISBN 978-3-88603-916-6.
- ↑ K. Hemminki, A. Försti, J. Lorenzo Bermejo: Surveying germline genomic landscape of breast cancer. In: Breast Cancer Res Treat. Band 113, 2009, S. 601–603. PMID 18297427.
- ↑ Familial breast cancer. In: The Lancet. Band 358, 2001, S. 1389–1399, zitiert nach Uta Wagenmann: Auf der Suche nach dem magischen Krebs-Gen. In: Freitag. 26. April 2002. (freitag.de)
- ↑ Katharina Schmutzler, Markus Löffler, Jürgen Windeler, Stefanie Thomas, Johannes Bruns, Thomas Rath: Familiärer Brust- und Eierstockkrebs: Von der Forschung zur Regelversorgung. In: Deutsches Ärzteblatt. Band 102, Nr. 50, 16. Dezember 2005, S. A-3486 / B-2948 / C-2461 (aerzteblatt.de).
- ↑ Internet, Behelfsquelle: Erblicher Brust- und Eierstockkrebs – Finanzierung für genetische Beratung österreichweit für die nächsten drei Jahre gesichert! Archiviert vom (nicht mehr online verfügbar) am 1. August 2012; abgerufen am 11. Oktober 2014.
- ↑ E. V. Jensen, H. I. Jacobson: Basic guides to the mechanism of estrogen action. In: Recent Progress in Hormon Research. Band 18, 1962, S. 387–414.
- ↑ Early Breast Cancer Trialists’ Collaborative Group: Tamoxifen for early breast cancer: An overview of the randomised trials. In: Lancet. Band 351, 1998, S. 1451–1467.
- ↑ B. Fisher, J. P. Costantino, D. L. Wickerham u. a.: Tamoxifen for prevention of breast cancer: Report of the National Surgical Adjuvant Breast and Bowel Project P-1 Study. In: Journal of the National Cancer Institute. Band 90, 1998, S. 1371–1388.
- ↑ Kala Visvanathan, Patricia Hurley, Elissa Bantug u. a.: Use of Pharmacologic Interventions for Breast Cancer Risk Reduction: American Society of Clinical Oncology Clinical Practice Guideline. In: Journal of Clinical Oncology. Band 31, 2013, S. 2942–2962.
- ↑ Nicola Siegmund-Schultze, Vera Zylka-Menhorn, Renate Leinmüller, Rüdiger Meyer: Hormontherapie und Brustkrebs: Ein Blick auf aktuelle Datenlage. In: Deutsches Ärzteblatt. Band 105, Nr. 6, 8. Februar 2008, S. A-260 / B-234 / C-230 (aerzteblatt.de).
- ↑ J. E. Rossouw, G. L. Anderson, R. L. Prentice, A. Z. LaCroix, C. Kooperberg, M. L. Stefanick, R. D. Jackson, S. A. Beresford, B. V. Howard, K. C. Johnson, J. M. Kotchen, J. Ockene; Writing Group for the Women’s Health Initiative Investigators.: Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women’s Health Initiative randomized controlled trial. In: JAMA. Band 288, Nr. 3, 2002, S. 321–333.
- ↑ J. Straszewski: Age at menarchy and breast cancer. In: Journal of the National Cancer Institute. Band 47, 1971, S. 935.
- ↑ D. Trichopoulos, B. MacMahon, P. Cole: Menopause and breast cancer risk. In: Journal of the National Cancer Institute. Band 48, 1972, S. 605.
- ↑ S. N. Dwivedi, P. Singh, N. Sareen, A. S. Bhadoria, U. Kapil: Reproductive factors and risk of breast cancer: A Review. In: Indian Journal of Cancer. Band 51, Nr. 4, 1. Oktober 2014, ISSN 0019-509X, S. 571, doi:10.4103/0019-509X.175345, PMID 26842199 (indianjcancer.com [abgerufen am 21. Dezember 2018]).
- ↑ U. Ackermann-Liebrich: Stillen als Prävention gegen Brustkrebs. ( vom 24. Oktober 2007 im Internet Archive) infomed.org, November/Dezember 2002. Nach einer Veröffentlichung in The Lancet, 260/2002, S. 187–195.
- ↑ V. Beral u. a.: Breast cancer and abortion: collaborative reanalysis of data from 53 epidemiological studies, including 83.000 women with breast cancer from 16 countries. In: The Lancet. 363/2004, S. 1007–1016. PMID 15051280.
- ↑ D. H. Brewster u. a.: Risk of breast cancer after miscarriage or induced abortion: a Scottish record linkage case-control study. In: J Epidemiol Community Health. 59/2005, S. 283–287. PMID 15767381.
- ↑ X. Paoletti, F. Clavel-Chapelon: Induced and spontaneous abortion and breast cancer risk: results from the E3N cohort study. In: Int J Cancer 106/2003, S. 270–276. PMID 12800205.
- ↑ G. K. Reeves u. a.: Breast cancer risk in relation to abortion: Results from the EPIC study. In: Int J Cancer. 119/2006, S. 1741–1745. PMID 16646050.
- ↑ M. K. Ramadhani, S. G. Elias u. a.: Innate left handedness and risk of breast cancer: case-cohort study. In: BMJ (Clinical research ed.). Band 331, Nummer 7521, Oktober 2005, S. 882–883, doi:10.1136/bmj.38572.440359.AE. PMID 16186135. PMC 1255796 (freier Volltext).
- ↑ Brustkrebs: Erhöhtes Risiko bei Linkshänderinnen. In: Spiegel Online. 26. September 2005, abgerufen am 27. Dezember 2014.
- ↑ Harald Frater: scinexx – Mehr Brustkrebs bei Linkshänderinnen: Zusammenhang zwischen Händigkeit und Krebshäufigkeit aufgedeckt – Krebs, Brustkrebs, Linkshänder – Kre. In: g-o.de. 26. September 2005, archiviert vom (nicht mehr online verfügbar); abgerufen am 27. Dezember 2014.
- ↑ a b c L. Titus-Ernstoff, P. A. Newcomb u. a.: Left-handedness in relation to breast cancer risk in postmenopausal women. In: Epidemiology (Cambridge, Mass.). Band 11, Nummer 2, März 2000, S. 181–184. PMID 11021617.
- ↑ L. Fritschi u. a.: Left-handedness and risk of breast cancer. In: Br J Cancer. 97, 2007, S. 686–687. PMID 17687338. PMC 2360366 (freier Volltext)
- ↑ D. Trichopoulos: Hypothesis: does breast cancer originate in utero. In: The Lancet. 335, 1990, S. 939–940. PMID 1970028.
- ↑ N. Geschwind, A. M. Galaburda: Cerebral lateralization. Biological mechanisms, associations, and pathology: I. A hypothesis and a program for research. In: Archives of neurology. Band 42, Nummer 5, Mai 1985, S. 428–459. PMID 3994562.
- ↑ V. Llaurens u. a.: Why are some people left-handed? An evolutionary perspective. In: Phil Trans R Soc B. 364, 2009, S. 881–894. doi:10.1098/rstb.2008.0235 PMID 19064347 (Review)
- ↑ a b c R. Roychoudhuri u. a.: Cancer and laterality: a study of the five major paired organs (UK). In: Cancer Causes & Control 17, 2006, S. 655–662. PMID 16633912.
- ↑ A. Ekbom u. a.: Epidemiologic correlates of breast cancer laterality (Sweden). In: Cancer Causes & Control. 5, 1994, S. 510–516. PMID 7827237.
- ↑ H. A. Weiss u. a.: Laterality of breast cancer in the United States. In: Cancer Causes & Control. 7, 1996, S. 539–543. PMID 8877052.
- ↑ C. I. Perkins u. a.: Association between breast cancer laterality and tumor location, United States, 1994–1998. In: Cancer Causes Control. 15, 2004, S. 637–645. PMID 15280621.
- ↑ M. T. Goodman u. a.: Comparative epidemiology of breast cancer among men and women in the US, 1996 to 2000. In: Cancer Causes Control. 17, 2006, S. 127–136. PMID 16425090.
- ↑ S. Dane u. a.: Asymmetries in breast cancer lateralization and both axillary lymph node number and metastatic involvement. In: Lymphology. 41, 2008, S. 75–79. PMID 18720914.
- ↑ a b O. Hallberg, O. Johansson: Sleep on the right side-Get cancer on the left? In: Pathophysiology. 17, 2010, S. 157–160. PMID 19647986.
- ↑ M. A. Kramer, S. Albrecht, R. A. Miller: Handedness and the laterality of breast cancer in women. In: Nursing research. Band 34, Nummer 6, Nov-Dez 1985, S. 333–337. PMID 2866491.
- ↑ Häufig gestellte Fragen. ( vom 9. März 2009 im Internet Archive) Abgerufen am 27. November 2009.
- ↑ E. Nekolla: Epidemiologie des strahleninduzierten Mammakarzinoms. Dissertation, LMU München, 2004.
- ↑ F. A. Mettler, A. C. Upton u. a.: Benefits versus risks from mammography: a critical reassessment. In: Cancer. Band 77, Nummer 5, März 1996, S. 903–909. PMID 8608482 (Review).
- ↑ P. Reynolds, S. Hurley u. a.: Active smoking, household passive smoking, and breast cancer: evidence from the California Teachers Study. In: Journal of the National Cancer Institute. Band 96, Nummer 1, Januar 2004, S. 29–37. PMID 14709736.
- ↑ P. Zubor, A. Gondova, J. Polivka Jr, P. Kasajova, K. Konieczka, J. Danko, O. Golubnitschaja: Breast cancer and Flammer syndrome: any symptoms in common for prediction, prevention and personalised medical approach? In: EPMA Journal. Band 8, Nr. 2, 10. Apr 2017, S. 129–140.
- ↑ M. Smollich, M. Götte u. a.: On the role of endothelin-converting enzyme-1 (ECE-1) and neprilysin in human breast cancer. In: Breast cancer research and treatment. Band 106, Nummer 3, Dezember 2007, S. 361–369, doi:10.1007/s10549-007-9516-9. PMID 17295044.
- ↑ B. M. Lynch, H. K. Neilson, C. M. Friedenreich: Physical activity and breast cancer prevention. In: Recent results in cancer research. Band 186, 2011, S. 13–42, doi:10.1007/978-3-642-04231-7_2. PMID 21113759. (Review).
- ↑ a b cancer.org: Detailed Guide: Breast Cancer – What Are the Risk Factors for Breast Cancer? ( vom 29. April 2009 im Internet Archive) abgerufen am 6. Mai 2008.
- ↑ a b Women’s Health Initiative, Gyne online, 4. Juni 2007 zitiert nach Brustkrebs-Risiko bei Übergewicht ( vom 11. Februar 2009 im Internet Archive)
- ↑ M. Gago-Dominguez, J. M. Yuan, C. L. Sun, H. P. Lee, M. C. Yu: Opposing effects of dietary n-3 and n-6 fatty acids on mammary carcinogenesis: The Singapore Chinese Health Study. In: British Journal of Cancer. Band 89, Nummer 9, November 2003, S. 1686–1692, doi:10.1038/sj.bjc.6601340. PMID 14583770. PMC 2394424 (freier Volltext).
- ↑ K. Wakai, K. Tamakoshi, C. Date, M. Fukui, S. Suzuki, Y. Lin, Y. Niwa, K. Nishio, H. Yatsuya, T. Kondo, S. Tokudome, A. Yamamoto, H. Toyoshima, A. Tamakoshi: Dietary intakes of fat and fatty acids and risk of breast cancer: a prospective study in Japan. In: Cancer Science. Band 96, Nummer 9, September 2005, S. 590–599, doi:10.1111/j.1349-7006.2005.00084.x. PMID 16128744.
- ↑ J. S. Zheng, X. J. Hu u. a.: Intake of fish and marine n-3 polyunsaturated fatty acids and risk of breast cancer: meta-analysis of data from 21 independent prospective cohort studies. In: BMJ (Clinical research ed.). Band 346, 2013, S. f3706. PMID 23814120. (Review).
- ↑ S. Rice, S. A. Whitehead: Phytoestrogens and breast cancer–promoters or protectors? In: Endocrine-related cancer. Band 13, Nummer 4, Dezember 2006, S. 995–1015, doi:10.1677/erc.1.01159. PMID 17158751. (Review).
- ↑ Phytoestrogens and Breast Cancer. Cornell University, Juli 2001; abgerufen am 25. November 2009.
- ↑ Crystal C. Douglas, Sarah A. Johnson, Bahram H. Arjmandi: Soy and its isoflavones: the truth behind the science in breast cancer. In: Anti-Cancer Agents in Medicinal Chemistry. Band 13, Nr. 8, Oktober 2013, ISSN 1875-5992, S. 1178–1187, doi:10.2174/18715206113139990320, PMID 23919747.
- ↑ Impact of Soy Foods on the Development of Breast Cancer and the Prognosis of Breast Cancer Patients. PMID 27161216.
- ↑ Shumin Qiu, Chongmin Jiang: Soy and isoflavones consumption and breast cancer survival and recurrence: a systematic review and meta-analysis. In: European Journal of Nutrition. Band 58, Nr. 8, Dezember 2019, ISSN 1436-6215, S. 3079–3090, doi:10.1007/s00394-018-1853-4, PMID 30382332.
- ↑ Yuxia Wei, Jun Lv, Yu Guo, Zheng Bian, Meng Gao: Soy intake and breast cancer risk: a prospective study of 300,000 Chinese women and a dose-response meta-analysis. In: European Journal of Epidemiology. Band 35, Nr. 6, Juni 2020, ISSN 1573-7284, S. 567–578, doi:10.1007/s10654-019-00585-4, PMID 31754945, PMC 7320952 (freier Volltext).
- ↑ Soja und Brustkrebs. Abgerufen am 4. März 2021.
- ↑ C. Aceves, B. Anguiano, G. Delgado: Is iodine a gatekeeper of the integrity of the mammary gland? In: Journal of Mammary Gland Biology and Neoplasia. Band 10, Nr. 2, April 2005, S. 189–196, doi:10.1007/s10911-005-5401-5, PMID 16025225.
- ↑ Sonnenmangel fördert Krebs! ( vom 30. September 2007 im Internet Archive; PDF; 2,0 MB) In: Medical Tribune, 42. Jg., Nr. 23, 8. Juni 2007, S. 21.
- ↑ J. M. Lappe u. a.: Vitamin D and calcium supplementation reduces cancer risk: results of a randomized trial. In: The American journal of clinical nutrition. 85/2007, S. 1586–1591. PMID 17556697.
- ↑ A. M. Misotti, P. Gnagnarella: Vitamin supplement consumption and breast cancer risk: a review. In: Ecancermedicalscience. Band 7, 2013, S. 365, doi:10.3332/ecancer.2013.365. PMID 24171049. PMC 3805144 (freier Volltext). (Review).
- ↑ A. A. Rose, C. Elser u. a.: Blood levels of vitamin D and early stage breast cancer prognosis: a systematic review and meta-analysis. In: Breast cancer research and treatment. Band 141, Nummer 3, Oktober 2013, S. 331–339, doi:10.1007/s10549-013-2713-9. PMID 24104883. (Review).
- ↑ F. Sperati, P. Vici u. a.: Vitamin D supplementation and breast cancer prevention: a systematic review and meta-analysis of randomized clinical trials. In: PloS one. Band 8, Nummer 7, 2013, S. e69269, doi:10.1371/journal.pone.0069269. PMID 23894438. PMC 3718745 (freier Volltext). (Review).
- ↑ M. S. Farvid, E. Cho u. a.: Dietary protein sources in early adulthood and breast cancer incidence: prospective cohort study. In: BMJ (Clinical research ed.). Band 348, 2014, S. g3437. PMID 24916719. PMC 4051890 (freier Volltext).
- ↑ Sarah F. Brennan, Jayne V. Woodside, Paula M. Lunny, Chris R. Cardwell, Marie M. Cantwell: Dietary fat and breast cancer mortality: A systematic review and meta-analysis. In: Critical Reviews in Food Science and Nutrition. Band 57, Nr. 10, 3. Juli 2017, ISSN 1549-7852, S. 1999–2008, doi:10.1080/10408398.2012.724481, PMID 25692500.
- ↑ Anthony B. Miller, Claus Wall, Cornelia J. Baines, Ping Sun, Teresa To: Twenty five year follow-up for breast cancer incidence and mortality of the Canadian National Breast Screening Study: randomised screening trial. In: BMJ (Clinical research ed.). Band 348, 11. Februar 2014, ISSN 1756-1833, S. g366, doi:10.1136/bmj.g366, PMID 24519768, PMC 3921437 (freier Volltext).
- ↑ E. J. Aiello, D. S. Buist u. a.: Rate of breast cancer diagnoses among postmenopausal women with self-reported breast symptoms. In: The Journal of the American Board of Family Practice / American Board of Family Practice. Band 17, Nummer 6, Nov-Dez 2004, S. 408–415. PMID 15575032.
- ↑ D. B. Thomas, D. L. Gao u. a.: Randomized trial of breast self-examination in Shanghai: final results. In: Journal of the National Cancer Institute. Band 94, Nummer 19, Oktober 2002, S. 1445–1457. PMID 12359854.
- ↑ J. P. Kösters, P. C. Gøtzsche: Regular self-examination or clinical examination for early detection of breast cancer. In: Cochrane Database Syst Rev. 2/2003, Art. CD003373. PMID 12804462.
- ↑ a b Agency for Healthcare Research and Quality: Screening for Breast Cancer. ( vom 5. Januar 2007 im Internet Archive) vom Februar 2002, abgerufen am 27. November 2009.
- ↑ Jolie Ringash: Preventive health care, 2001 update: screening mammography among women aged 40-49 years at average risk of breast cancer. ( vom 2. Januar 2007 im Internet Archive) Canadian Task Force on Preventive Health Care; abgerufen am 27. Dezember 2009.
- ↑ Silikonmodell zur Brustselbstuntersuchung. In: Constanze Schäfer, Ingo Donieth: Hilfsmittel und Medizinprodukte. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2003, ISBN 3-8047-1948-1.
- ↑ a b Patientenbroschüre zur AWMF-Leitlinie (077/001) „Brustkrebs-Früherkennung“ der Deutschen Krebsgesellschaft und der Deutschen Krebshilfe Früherkennung bei Brustkrebs – Eine Entscheidungshilfe für Frauen. (PDF; 360 kB) abgerufen am 12. November 2018.
- ↑ MR-Tomographie findet mehr Tumore. In: curado.de. 29. März 2007, archiviert vom (nicht mehr online verfügbar) am 9. November 2007; abgerufen am 27. Dezember 2014. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Mammographie-Screening-Programm. ( vom 4. September 2011 im Internet Archive) Vom 20. Januar 2011, abgerufen am 10. Januar 2012.
- ↑ S. Fabbri u. a.: Benign Breast Diseases in Breast Cancer Screening Programs in Italy 2000–2001. ( vom 31. Januar 2012 im Internet Archive; PDF; 155 kB) In: Tumori, 90, 2004, S. 547–549.
- ↑ P. Taylor, H. W. Potts: Computer Aids and Human Second Reading as Interventions in Screening Mammography. In: European Journal of Cancer. 44, 2008, S. 798–807. PMID 18353630.
- ↑ IGeL-Monitor, Bewertung der MRT der Brust zur Krebsfrüherkennung. und Ultraschall der Brust zur Krebsfrüherkennung. abgerufen am 19. Oktober 2018.
- ↑ Universität erstattet Anzeige nach Bluttest-PR. In: Süddeutsche Zeitung. 8. April 2019. Abgerufen am 14. April 2019.
- ↑ Pressemitteilung Universitätsklinikum Heidelberg, 21. Februar 2019. Abgerufen am 21. Februar 2019.
- ↑ Jens-Uwe Blohmer, Annette Hasenburg, Wolfgang Janni: Gemeinsame Stellungnahme zur Berichterstattung über neuen Bluttest zur Früherkennung bei Brustkrebs. (PDF) Arbeitsgemeinschaft Gynäkologische Onkologie e. V., 27. Februar 2019, ehemals im (nicht mehr online verfügbar); abgerufen am 8. März 2019. (Seite nicht mehr abrufbar. Suche in Webarchiven)
- ↑ J. Baltzer, H.-G. Meerpohl, J. Bahnsen: Praxis der gynäkologischen Onkologie – Praxis der Frauenheilkunde. 2. Auflage. Band 3, Georg Thieme Verlag, 2000, ISBN 3-13-109912-7, S. 296. (eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ Vereinbarung von Qualifikationsvoraussetzungen gemäß § 135 Abs. 2 SGB V zur Durchführungvon Untersuchungen in der Ultraschalldiagnostik. Stand 2003. In: dov-online.de. Abgerufen am 10. März 2022 (nur über Webcache von Google abrufbar).
- ↑ Vereinbarung von Qualitätssicherungsmaßnahmen nach § 135 Abs. 2 SGB V zur Ultraschalldiagnostik. (PDF) Stand 2021. Kassenärztliche Bundesvereinigung, S. 46, abgerufen am 10. März 2022.
- ↑ a b c d e S3-Leitlinie Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms der 2020. In: AWMF online
- ↑ Berthold Jany, Tobias Welte: Pleuraerguss des Erwachsenen – Ursachen, Diagnostik und Therapie. In: Deutsches Ärzteblatt. Band 116, Nr. 21, 2019, S. 377–385, hier: S. 379 und 383.
- ↑ S. Lakhani, I. O. Ellis, S. J. Schnitt, M. J. van de Vijver: WHO Classification of Tumours of the Breast, Fourth Edition. International Agency for Research on Cancer, Lyon 2012, ISBN 978-92-832-2433-4 (online).
- ↑ S3-Leitlinie Mammakarzinom. ( vom 18. Januar 2012 im Internet Archive; PDF; 1,67 MB) Deutsche Krebsgesellschaft S. 28–29, S. 185.
- ↑ A. C. Wolff, M. E. Hammond u. a.: American Society of Clinical Oncology/College of American Pathologists guideline recommendations for human epidermal growth factor receptor 2 testing in breast cancer. In: Journal of Clinical Oncology. Band 25, Nummer 1, Jan 2007, S. 118–145. (ascopubs.org). doi:10.1043/1543-2165(2007)131[18:ASOCCO]2.0.CO;2 (zurzeit nicht erreichbar). PMID 19548375.
- ↑ A. Goldhirsch, W. C. Wood u. a.: Progress and promise: highlights of the international expert consensus on the primary therapy of early breast cancer 2007. In: Annals of Oncology. Band 18, Nummer 7, Juli 2007, S. 1133–1144, doi:10.1093/annonc/mdm271. PMID 17675394. (Review).
- ↑ L. A. Carey, C. M. Perou u. a.: Race, breast cancer subtypes, and survival in the Carolina Breast Cancer Study. In: JAMA. Band 295, Nummer 21, Juni 2006, S. 2492–2502, doi:10.1001/jama.295.21.2492. PMID 16757721.
- ↑ a b c d Nadine Eckert: Mammakarzinom: Mehr Gewissheit für die Therapie. In: Dtsch Arztebl. Band 116, Nr. 29-30, 2019, S. A-1373 / B-1135 / C-1119 (online).
- ↑ J. A. Sparano, R. J. Gray, D. F. Makower, K. I. Pritchard, K. S. Albain, D. F. Hayes, C. E. Geyer Jr, E. C. Dees, M. P. Goetz, J. A. Olson Jr, T. Lively, S. S. Badve, T. J. Saphner, L. I. Wagner, T. J. Whelan, M. J. Ellis, S. Paik, W. C. Wood, P. M. Ravdin, M. M. Keane, H. L. Gomez-Moreno, P. S. Reddy, T. F. Goggins, I. A. Mayer, A. M. Brufsky, D. L. Toppmeyer, V. G. Kaklamani, J. L. Berenberg, J. Abrams, G. W. Sledge, Jr.: Adjuvant Chemotherapy Guided by a 21-Gene Expression Assay in Breast Cancer. In: N Engl J Med. Band 379, Nr. 2, 12. Juni 2018, S. 111–121, doi:10.1056/NEJMoa1804710, PMID 29860917 (englisch).
- ↑ F. Cardoso, L. J. van’t Veer, J. Bogaerts, L. Slaets, G. Viale, S. Delaloge, J. Y. Pierga, E. Brain, S. Causeret, M. DeLorenzi, A. M. Glas, V. Golfinopoulos, T. Goulioti, S. Knox, E. Matos, B. Meulemans, P. A. Neijenhuis, U. Nitz, R. Passalacqua, P. Ravdin, I. T. Rubio, M. Saghatchian, T. J. Smilde, C. Sotiriou, L. Stork, C. Straehle, G. Thomas, A. M. Thompson, J. M. van der Hoeven, P. Vuylsteke, R. Bernards, K. Tryfonidis, E. Rutgers, M. Piccart; MINDACT Investigators: 70-Gene Signature as an Aid to Treatment Decisions in Early-Stage Breast Cancer. In: N Engl J Med. Band 375, Nr. 8, 25. August 2016, S. 717–729, doi:10.1056/NEJMoa1602253, PMID 27557300 (englisch).
- ↑ Deutsche Krebsgesellschaft: Deutsche Krebsgesellschaft verleiht offiziell erstes „Zertifikat Brustzentrum“. ( vom 3. Dezember 2012 im Webarchiv archive.today) 21. Juli 2003.
- ↑ a b c „Anforderungen an strukturierte Behandlungsprogramme für Patientinnen mit Brustkrebs“, Anlage 3 zu §§ 28b bis 28 g der Risikostrukturausgleichs-Verordnung nach § 137f SGB Fünftes Buch (V).
- ↑ K. Travis: Bernard Fisher reflects on a half-century’s worth of breast cancer research. In: Journal of the National Cancer Institute. Band 97, Nummer 22, November 2005, S. 1636–1637, doi:10.1093/jnci/dji419. PMID 16288112.
- ↑ a b c d e Wolfgang Janni, Bernd Gerber, Harald Sommer, Michael Untch, Annette Krause, Darius Dian, Ingo Runnebaum, Brigitte Rack, Klaus Friese: Zertifizierte medizinische Fortbildung: Therapie des primären, invasiven Mammakarzinoms. In: Deutsches Ärzteblatt. Band 102, Nr. 41, 14. Oktober 2005, S. A-2795 / B-2360 / C-2226 (aerzteblatt.de).
- ↑ a b c V. Naraynsingh u. a.: Immediate breast reconstruction following segmentectomy using a latissimus dorsi 'myoadipose' flap through a single axillary incision: a case series. In: Cases Journal. 2, 2009, 8116. PMID 19830050 (Open Access, unter CC-by-3.0-Lizenz).
- ↑ a b S. Reefy u. a.: Oncological outcome and patient satisfaction with skin-sparing mastectomy and immediate breast reconstruction: a prospective observational study. In: BMC Cancer. Band 10, 2010, S. 171 doi:10.1186/1471-2407-10-171 (Open Access, unter CC-by-2.0).
- ↑ W. F. Hartsell u. a.: Should multicentric disease be an absolute contraindication to the use of breast-conserving therapy? In: Int J Radiat Oncol Biol Phys 30, 1994, S. 49–53. PMID 8083128.
- ↑ O. Gentilini, E. Botteri u. a.: Conservative surgery in patients with multifocal/multicentric breast cancer. In: Breast cancer research and treatment. Band 113, Nummer 3, Februar 2009, S. 577–583, doi:10.1007/s10549-008-9959-7. PMID 18330695.
- ↑ T. Kühn u. a.: Sentinel-Node-Biopsie beim Mammakarzinom. ( des vom 21. November 2008 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (PDF). In: Geburtsh Frauenheilk. Band 63, 2003, S. 835–840.
- ↑ Beatrice Cavallo Marincola, Luisa Di Mare, Federica Pediconi, Luca Bertaccini, Fabrizio Boni, Alessandro Napoli, Carlo Catalano: Clinical Experience in Noninvasive Treatment of Focal Breast Cancer with Magnetic Resonance Guided High Intensity Focused Ultrasound (MRgFUS) (PDF; 178 kB).
- ↑ a b E. H. Romond, E. A. Perez, J. Bryant u. a.: Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer. In: The New England Journal of Medicine. Band 353, Nummer 16, Oktober 2005, S. 1673–1684, doi:10.1056/NEJMoa052122. PMID 16236738.
- ↑ a b E. A. Perez, E. H. Romond u. a.: Updated results of the combinated analysis of NCCTG N9831 and NSABP B-31 adjuvant chemotherapy with/without trastuzumab in patients with HER2-positive breast cancer. In: J Clin Oncol 2007 ASCO Annual Meeting Proceeding. 25 (Suppl 18S): 2007, 6s (abstract 512).
- ↑ a b M. J. Piccart-Gebhart, M. Procter u. a.: Trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer. In: The New England Journal of Medicine. Band 353, Nummer 16, Oktober 2005, S. 1659–1672, doi:10.1056/NEJMoa052306. PMID 16236737.
- ↑ L. Gianni, A. Goldhirsch u. a.: Update of the HERA trial and the role of 1 year trastuzumab as adjuvant therapy for breast cancer. In: The Breast. Band 18, Suppl 1, 2009, S. S11 (abstract S25).
- ↑ Zusammenfassung der Merkmale des Arzneimittels (PDF; 441 kB) EPAR der EMA, abgerufen am 29. Oktober 2019.
- ↑ S. C. Darby, M. Ewertz u. a.: Risk of ischemic heart disease in women after radiotherapy for breast cancer. In: The New England Journal of Medicine. Band 368, Nummer 11, März 2013, S. 987–998, doi:10.1056/NEJMoa1209825. PMID 23484825.
- ↑ a b J. Kraus: Brustdrüse. 1973, S. 196.
- ↑ Sören von Otte, Michael Friedrich, Klaus Diedrich, Markus Kupka: Fertilitätserhalt bei onkologischen Patientinnen: Stand und Perspektiven. In: Deutsches Ärzteblatt. Band 103, Nr. 38, 22. September 2006, S. A-2479 / B-2149 / C-2073 (aerzteblatt.de).
- ↑ Medizin – Kommunikation: DGE: Hormonmangel schadet Gehirn. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften, Pressemitteilung vom 6. November 2007 beim Informationsdienst Wissenschaft (idw-online.de), abgerufen am 27. Dezember 2014.
- ↑ G. von Minckwitz: For The Breast Commission of the German Gynaecological Oncology Working Group (AGO). Evidence-based treatment of metastatic breast cancer – 2006 recommendations by the AGO Breast Commission. In: Eur J Cancer. Band 42, 2006, S. 2897–2908. PMID 17046240.
- ↑ 46 % mehr Brustkrebspatientinnen mit modernen Aromatasehemmern seit 2003 versorgt. ( des vom 27. August 2016 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Verein Deutsches Arzneiprüfungsinstitut, 13. November 2012.
- ↑ Faslodex. ( des vom 17. März 2018 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 46 kB) European Medicines Agency, März 2010.
- ↑ D. F. Hayes: Tamoxifen: Dr. Jekyll and Mr. Hyde? In: Journal of the National Cancer Institute. Band 96, Nummer 12, Juni 2004, S. 895–897. PMID 15199102.
- ↑ C. K. Osborne, V. Bardou, T. A. Hopp, G. C. Chamness, S. G. Hilsenbeck, S. A. Fuqua, J. Wong, D. C. Allred, G. M. Clark, R. Schiff: Role of the estrogen receptor coactivator AIB1 (SRC-3) and HER-2/neu in tamoxifen resistance in breast cancer. In: Journal of the National Cancer Institute. Band 95, Nummer 5, März 2003, S. 353–361. PMID 12618500.
- ↑ A. Gucalp, S. Tolaney u. a.: Phase II trial of bicalutamide in patients with androgen receptor-positive, estrogen receptor-negative metastatic Breast Cancer. In: Clinical cancer research. Band 19, Nummer 19, Oktober 2013, S. 5505–5512, doi:10.1158/1078-0432.CCR-12-3327. PMID 23965901. PMC 4086643 (freier Volltext).
- ↑ D. R. Cochrane, S. Bernales, B. M. Jacobsen, D. M. Cittelly, E. N. Howe, N. C. d Amato, N. S. Spoelstra, S. M. Edgerton, A. Jean, J. Guerrero, F. Gómez, S. Medicherla, I. E. Alfaro, E. McCullagh, P. Jedlicka, K. C. Torkko, A. D. Thor, A. D. Elias, A. A. Protter, J. K. Richer: Role of the Androgen Receptor in Breast Cancer and Preclinical Analysis of Enzalutamide. In: Breast Cancer Research. Band 16, Nr. 1, 2014, S. R7. doi:10.1186/bcr3599. PMC 3978822 (freier Volltext). PMID 24451109.
- ↑ Data From Omnitarg Clinical Program Presented at American Society of Clinical Oncology Meeting. Genentech, archiviert vom (nicht mehr online verfügbar) am 13. Juli 2014; abgerufen am 28. Juni 2014. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ D. Slamon, W. Eiermann, N. Robert u. a.: BCIRG 006: 2nd interim analysis phase III randomized trial comparing doxorubicin and cyclophosphamide followed by docetaxel (ACT) with doxorubicin and cyclophophamide followed by docetaxel and trastuzumab (ACTH) with docetraxel, carboplatin and trastuzumab (TCH) in HER2neu positive early breast cancer patients. In: Breast Cancer Res Treat. Band 100, Suppl 1, 2006, abstr 52.
- ↑ D. Slamon, W. Eiermann, N. Robert u. a.: Presentation at the 29th SABCS. San Antonio, Texas, USA, 14. bis 17. Dezember 2006.
- ↑ B. Krempien: Die Entstehung von Knochenschmerzen bei Knochenmetastasen und ihre Behandlung durch Bisphophonate. In: H. H. Bartsch, W. Hornstein (Hrsg.): Interdisziplinäre Schmerztherapie bei Tumorpatienten. Karger Publishers, 1998, ISBN 3-8055-6594-1. (eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ N. J. Robert, V. Diéras u. a.: RIBBON-1: randomized, double-blind, placebo-controlled, phase III trial of chemotherapy with or without bevacizumab for first-line treatment of human epidermal growth factor receptor 2-negative, locally recurrent or metastatic breast cancer. In: Journal of clinical oncology. Band 29, Nummer 10, April 2011, S. 1252–1260, doi:10.1200/JCO.2010.28.0982. PMID 21383283.
- ↑ J. Cortes, J. O’Shaughnessy u. a.: Eribulin monotherapy versus treatment of physician’s choice in patients with metastatic breast cancer (EMBRACE): a phase 3 open-label randomised study. In: Lancet. Band 377, Nummer 9769, März 2011, S. 914–923, doi:10.1016/S0140-6736(11)60070-6. PMID 21376385.
- ↑ Freerk T. Baumann, Klaus Schüle (Hrsg.): Bewegungstherapie und Sport bei Krebs: Leitfaden für die Praxis. 1. Auflage. Deutscher Ärzte-Verlag, 2008, ISBN 978-3-7691-0564-3, S. 274.
- ↑ J. Kraus: Brustdrüse. In: Franz Xaver Sailer, Friedrich Wilhelm Gierhake (Hrsg.): Chirurgie historisch gesehen. Anfang – Entwicklung – Differenzierung. Dustri-Verlag, Deisenhofen bei München 1973, ISBN 3-87185-021-7, S. 192–199, hier: S. 192.
- ↑ Sameh M. Arab: Medicine in Ancient Egypt 2. In: arabworldbooks.com. Abgerufen am 27. Dezember 2014.
- ↑ a b c A History of Breast Cancer. ( vom 30. Juli 2010 im Internet Archive).
- ↑ a b c d e f Orlando E. Silva, Stefano Zurrida: Brustkrebs: Diagnostik und Therapie. Elsevier, Urban & Fischer Verlag, 2007, ISBN 978-3-437-24260-1 (Volltext in der Google-Buchsuche).
- ↑ The History of Cancer. In: American Cancer Society. 9. März 2009, archiviert vom (nicht mehr online verfügbar) am 9. Oktober 2006; abgerufen am 26. März 2010.
- ↑ Corpus Hippocraticum: Epidemien 5,101.
- ↑ Corpus Hippocraticum: Aphorismen 6,38.
- ↑ a b c d Hermann Delbrück: Brustkrebs: Rat und Hilfe für Betroffene und Angehörige. W. Kohlhammer Verlag, 2008, ISBN 978-3-17-020469-0 (Volltext in der Google-Buchsuche).
- ↑ Vgl. etwa Josef Weinlechner: Vier Fälle von Carcinoma mammae mit Chlorzinkpaste behandelt. In: Wiener medizinische Presse. Nr. 13, 1876, S. 430 ff.
- ↑ a b J. Kraus: Brustdrüse. 1973, S. 195.
- ↑ a b c d Manfred Kaufmann, Ismail Jatoi, Jean Petit: Atlas der Brustchirurgie. Springer Verlag, 2007, ISBN 978-3-540-48881-1 (Volltext in der Google-Buchsuche).
- ↑ Benjamin Bell: Lehrbegriff der Wundarzneykunst. 3. Auflage. Band 6. Weidmann, 1809 (Volltext in der Google-Buchsuche).
- ↑ J. Kraus: Brustdrüse. 1973, S. 194.
- ↑ Vgl. J. Kraus: Brustdrüse. In: Franz Xaver Sailer, Friedrich Wilhelm Gierhake (Hrsg.): Chirurgie historisch gesehen. Anfang – Entwicklung – Differenzierung. Dustri-Verlag, Deisenhofen bei München 1973, ISBN 3-87185-021-7, S. 192–199, hier: S. 194–196.
- ↑ Vgl. auch William Stewart Halsted: Operation for cancer of the Breast. In: Ann. Surg. Band 20, 1894, S. 497 ff.
- ↑ William Stewart Halsted: The results of operations for the cure of cancer of the breast performed at the Johns Hopkins Hospital from June, 1889 to January, 1894. In: Ann Surg. Band 20, 1894, S. 497.
- ↑ Josef Rotter: Günstige Dauererfolge durch ein verbessertes Operationsverfahren der Mammakarzinome. In: Berliner klinische Wochenschrift. Band 33, 1896, S. 69.
- ↑ Vgl. Janicke, Albert Neisser: Exitus letalis nach Erysipelimpfung bei inoperablem Mamma-carcinom und mikroskopischem Befund des geimpften Carcinoms. In: Chirurgie. Band 25, 1884, S. 401 ff.
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin / Göttingen / Heidelberg 1960, S. 50.
- ↑ Vgl. etwa Henryk Nowakowski: Der gegenwärtige Stand der endokrinen Therapie in der Palliativbehandlung des metastasierenden Mamma-carcinoms der Frau. In: Der Chirurg. Band 39, 1968, S. 258 ff.
- ↑ J. Hirsch: Radiochirurgie des Brustkrebses. In: Deutsche Medizinische Wochenschrift Band 34, 1927, S. 1419–1421.
- ↑ D. H. Patey, W. H. Dyson: The prognosis of carcinoma of the breast in relation to the type of operation performed. In: British Journal of Cancer. Band 2, Nummer 1, März 1948, S. 7–13. PMID 18863724. PMC 2007539 (freier Volltext).
- ↑ R. McWhriter: Simple mastectomy and radiotherapy in the treatment of breast cancer. In: The British journal of radiology. Band 28, Nummer 327, März 1955, S. 128–139. PMID 14351717.
- ↑ Vgl. A. Clark: The effect of the Roentgen-rays in a case of chronic carcinom of the breast. In: British Medical Journal. Band 11, 1901, S. 1398 ff.
- ↑ J. Kraus: Brustdrüse. 1973, S. 196 f.
- ↑ Vgl. auch E. Munteau: Die praeoperative Röntgenbestrahlung des Mamma-carcinoms. Thieme, Stuttgart 1961.
- ↑ B. Fisher, E. R. Fisher: Transmigration of lymph nodes by tumor cells. In: Science. Band 152, Nummer 3727, Juni 1966, S. 1397–1398. PMID 5949244.
- ↑ Renate Leinmüller: Brustkrebs: Primäre Chemotherapie als prognostischer Marker. In: Deutsches Ärzteblatt. Band 95, Nr. 44, 30. Oktober 1998, S. A-2753 / B-2344 / C-2082 (aerzteblatt.de).
- ↑ Y. Miki, J. Swensen u. a.: A strong candidate for the breast and ovarian cancer susceptibility gene BRCA1. In: Science. Band 266, Nummer 5182, Oktober 1994, S. 66–71. PMID 7545954.
- ↑ R. Wooster, S. L. Neuhausen u. a.: Localization of a breast cancer susceptibility gene, BRCA2, to chromosome 13q12-13. In: Science. Band 265, Nummer 5181, September 1994, S. 2088–2090. PMID 8091231.
- ↑ Terea Wagner u. a.: Hereditärer Brust- und Eierstockkrebs. In: Detlev Ganten, Klaus Ruckpaul: Molekularmedizinische Grundlagen von hereditären Tumorerkrankungen. Birkhäuser, 2001, ISBN 3-540-67808-5, S. 257 Volltext in der Google-Buchsuche
- ↑ Sixtinische Kapelle: Michelangelo malte Frau mit Brustkrebs. In: Der Spiegel. 8. November 2024, ISSN 2195-1349 (spiegel.de [abgerufen am 8. November 2024]).
- ↑ Andreas G. Nerlich, Johann C. Dewaal, Antonio Perciaccante, Judith Wimmer, Simon T. Donell, Raffaella Bianucci: Did Michelangelo paint a young adult woman with breast cancer in “The Flood” (Sistine Chapel, Rome)? In: The Breast, Volume 78, 103823, December 2024. Editor-in-Chief: Fatima Cardoso, Lisbon, Portugal, Dezember 2024, abgerufen am 9. November 2024 (englisch).
- ↑ J. J. Grau, J. Estapé, M. Diaz-Padrón: Breast cancer in Rubens paintings. In: Breast cancer research and treatment. Band 68, Nummer 1, Juli 2001, S. 89–93. PMID 11678312.
- ↑ C. H. Espinel: The portrait of breast cancer and Raphael’s La Fornarina. In: Lancet. Band 360, Nummer 9350, 21.–28. Dez 2002, S. 2061–2063, doi:10.1016/S0140-6736(02)11997-0. PMID 12504417.
- ↑ P. A. Braithwaite, D. Shugg: Rembrandt’s Bathsheba: the dark shadow of the left breast. In: Annals of the Royal College of Surgeons of England. Band 65, Nummer 5, September 1983, S. 337–338. PMID 6351705. PMC 2494383 (freier Volltext).
- ↑ James Stuart Olson: Bathsheba’s Breast. JHU Press, 2005, ISBN 0-8018-8064-5 (Volltext in der Google-Buchsuche).
- ↑ A. Gross: An epidemic of breast cancer among models of famous artists. In: Breast cancer research and treatment. Band 84, Nummer 3, April 2004, S. 293, doi:10.1023/B:BREA.0000019965.21257.49. PMID 15026627.