Venlafaxin
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||
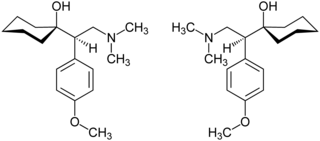
| (R)-Venlafaxin (links) und (S)-Venlafaxin (rechts) Enantiomere (1:1-Gemisch) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Venlafaxin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C17H27NO2 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes bis fast weißes, polymorphes Pulver (Hydrochlorid)[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 277,40 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt |
215–217 °C (Venlafaxin·Hydrochlorid)[2] | |||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Venlafaxin ist ein Arzneistoff, der bei der Behandlung von Depressionen und Angsterkrankungen verwendet wird. Chemisch handelt es sich um ein Phenylethylamin-Derivat, das als selektiver Serotonin-Noradrenalin-Wiederaufnahmehemmer seine Wirkung im Zentralnervensystem entfaltet.
Wirkprofil
[Bearbeiten | Quelltext bearbeiten]Venlafaxin vermindert die Wiederaufnahme (englisch: reuptake) von Serotonin und Noradrenalin in die präsynaptischen Vesikel an bestimmten Synapsen im Gehirn und ist ein selektiver Serotonin-Noradrenalin-Wiederaufnahmehemmer (SSNRI). Das dadurch vermehrte Angebot dieser Neurotransmitter im synaptischen Spalt soll die Linderung der depressiven Symptome bewirken.
Venlafaxin hemmt den Serotonin-Transporter mit etwa 30-facher Affinität im Vergleich zum Noradrenalin-Transporter und hemmt außerdem die Dopamin-Wiederaufnahme, wenn auch sehr schwach. In der Praxis bedeutet dies, dass Venlafaxin in niedrigen Dosierungen eher einem SSRI gleicht und seine noradrenerge Komponente erst ab höheren Dosierungen zum Tragen kommt.[4]
Innerhalb der SSNRI hat es also die größte Selektivität für Serotonin. Während Duloxetin eine 10-fach größere Selektivität für Serotonin im Verhältnis zu Noradrenalin zeigt, blockiert Milnacipran die Serotonin- und Noradrenalin-Wiederaufnahme etwa gleich stark.[5]
Die absolute Bioverfügbarkeit von Venlafaxin liegt bei lediglich 40 % bis 45 %, was an der erheblichen Metabolisierung in der Leber liegt. Venlafaxin wird primär über das CYP2D6 zum aktiven Metaboliten O-Desmethylvenlafaxin metabolisiert, in weit geringerem Umfang über das CYP3A4 zum weniger aktiven Nebenmetaboliten N-Desmethylvenlafaxin. Die Ausscheidung erfolgt vor allem über die Nieren (renal). Die Halbwertszeiten betragen 5 Stunden für Venlafaxin und 11 Stunden für O-Desmethylvenlafaxin.[6]
Die maximalen Plasmakonzentrationen von Venlafaxin und O-Desmethylvenlafaxin werden bei rasch freisetzenden Tabletten oder Kapseln innerhalb von 2 bzw. 3 Stunden und bei verzögert freisetzenden (retardierten) Formen innerhalb von 5,5 bzw. 9 Stunden erreicht.
Indikationen
[Bearbeiten | Quelltext bearbeiten]Venlafaxin-haltige Arzneimittel sind angezeigt zur Behandlung von Depressionen und Angsterkrankungen wie der generalisierten Angststörung, der sozialen Angststörung (soziale Phobie) und der Panikstörung (mit oder ohne Agoraphobie). Auch ist Venlafaxin angezeigt zur Erhaltungstherapie zur Verhinderung eines Rückfalls (Rezidivprophylaxe) oder des Wiederauftretens von neuen depressiven Erkrankungen. Weiterhin wird es im Rahmen des Off-Label-Use zur Behandlung der diabetischen Polyneuropathie eingesetzt. Auch im Rahmen einer ADHS-Behandlung kann es bei fehlgeschlagenen Versuchen mit anderen Stimulanzien, wie z. B. Methylphenidat, Erfolge erzielen, da es bei erhöhter Dosis ebenfalls eine stimulierende Wirkung entfaltet.[7]
Für Mädchen oder Jungen von 9 bis 18 Jahren mit mäßiger bis schwerer Depression – nicht aber mit unterschwelliger oder extrem starker Depression – ist nicht erwiesen, dass Venlafaxin oder ein anderes von 13 Antidepressiva besser wirkt als Placebos – mit Ausnahme von Fluoxetin, warnen Psychiater um Andrea Cipriani (Oxford-Universität) im „Lancet“ anhand der Befunde zu 5260 Probanden: Venlafaxin ging mit deutlich erhöhten Risiken für suizidale Gedanken und Handlungen einher. In einigen der 34 Studien wurden unliebsame Ergebnisse unterschlagen. Manche Hersteller verweigerten selbst die Übergabe anonymisierter Patientendaten.[8]
Unerwünschte Wirkungen
[Bearbeiten | Quelltext bearbeiten]Zu Beginn der Einnahme treten als Nebenwirkungen oft Magen-Darm-Beschwerden auf; es kommt häufig zu vermehrter Unruhe und diffusen Angstzuständen. Psychotische Reaktionen sind beschrieben, eventuell als Folge der dopaminergen Wirkung. Vermehrte (Nacht-)Schweißbildung, Blutdruckerhöhung und Herzbeschwerden sind ebenfalls möglich. Übelkeit ist, gerade zu Beginn der Behandlung, eine sehr häufige Nebenwirkung (mehr als 10 % der Patienten); unter anderem Erbrechen, Appetitlosigkeit, Verstopfung, Schwindel, Schlaflosigkeit, Nervosität, Zähneknirschen, Zittern und Sehstörungen sind häufig (1–10 % der Patienten). Weiterhin kann es zu Benommenheit und Müdigkeit kommen. Venlafaxin löst beim Mann sehr häufig sexuelle Funktionsstörungen aus (Ejakulationsschwierigkeiten) und kann die Libido vermindern.[9][10]
Suizidalität
Laut einer Analyse der US-Aufsichtsbehörde FDA von 2006, die alle Daten aus klinischen Studien mit Venlafaxin berücksichtigte (sowohl aus veröffentlichten als auch aus unveröffentlichten Untersuchungen), kann Venlafaxin bei unter 25-jährigen Anwendern die Suizidalität im Vergleich zur Einnahme von Scheinmedikamenten (Placebo) um den Faktor 5 steigern.[11] Eine placebokontrollierte US-amerikanische Metastudie aus dem Jahr 2012 mit 9185 Patienten konnte jedoch keinen Zusammenhang zwischen der Gabe von SSRI, hier Fluoxetin und Venlafaxin, und einem erhöhten Suizidrisiko finden. Die Studie kommt zu dem Ergebnis, dass die Annahmen der amerikanischen Gesundheitsbehörde FDA, die zu Warnhinweisen geführt hatten, falsch sind.[12][13]
Wegen des angeblichen besonderen Suizidrisikos und der im Vergleich zu anderen Antidepressiva höheren Toxizität sollte Venlafaxin nach Ansicht einiger Experten nicht mehr zur Erstbehandlung der Depression verwendet werden.[14] In Großbritannien wurde die Leitlinie zur Depressionsbehandlung überarbeitet, um den besonderen Risiken von Venlafaxin Rechnung zu tragen.[15] In Deutschland wurde über ein Stufenplanverfahren die Aufnahme eines entsprechenden Warnhinweises in die Produktinformation verpflichtend.[16]
Darreichungsformen
[Bearbeiten | Quelltext bearbeiten]Venlafaxin wird peroral verabreicht, es gibt Tabletten oder Kapseln zu 37,5 mg und 75 mg oder auch Retardformulierungen zu 37,5 mg, 75 mg, 150 mg, 225 mg und 300 mg, die den Arzneistoff verzögert abgeben. Wegen des gelegentlichen Auftretens der Magen-Darm-Beschwerden wird in Deutschland überwiegend die Retardform verordnet. Für die Herstellung der Arzneiformulierungen wird das Venlafaxin als Hydrochlorid eingesetzt.
Varianten
[Bearbeiten | Quelltext bearbeiten]Rechtzeitig vor dem Patentablauf von Venlafaxin versuchte der Hersteller Wyeth (inzwischen ein Pfizer-Unternehmen) eine Molekülvariante von Venlafaxin auf den Markt zu bringen und stellte im September 2007 einen EU-weiten (zentralen) Zulassungsantrag für Desvenlafaxin (das ist der aktive Metabolit O-Desmethylvenlafaxin). Die europäische Behörde hatte jedoch Bedenken, da die Wirksamkeit von Desvenlafaxin nicht überzeugend dargelegt werden konnte. Im Vergleich zur Muttersubstanz Venlafaxin schien Desvenlafaxin weniger wirksam zu sein sowie keinen Vorteil im Hinblick auf die Sicherheit und Verträglichkeit zu bieten. Außerdem erachtete das wissenschaftliche Gremium (Ausschuss für Humanarzneimittel, CHMP) die Daten zur Kurzzeit- und Langzeitwirkung von Desvenlafaxin als unzureichend. Wyeth zog daraufhin den Antrag zurück.[17]
14 Jahre später erhielt Neuraxpharm eine Zulassung für Desvenlafaxin für die Behandlung einer Major Depression bei Erwachsenen. Zum August 2022 wurde Desvenlafaxin unter dem Handelsnamen Desveneurax in Deutschland auf den Markt gebracht.[18]
In den USA ist Desvenlafaxin als Pristiq am Markt.[19]
Anwendung während der Schwangerschaft und Stillzeit
[Bearbeiten | Quelltext bearbeiten]Zur Anwendung von Venlafaxin in der Schwangerschaft liegen keine ausreichenden Daten vor.[20] Bei Neugeborenen, deren Mütter in den späten Stadien der Schwangerschaft Venlafaxin erhalten hatten, können verschiedene Anpassungsstörungen sofort oder kurz nach der Geburt auftreten, die mit neurologischen, gastrointestinalen und respiratorischen Symptomen einhergehen,[21] darunter Schwierigkeiten beim Saugen und Schlafen, Zittern, angespannte oder übermäßig entspannte Muskulatur, Erbrechen, Reizbarkeit und ständiges Weinen.[20] Aus epidemiologischen Studien gibt es Hinweise darauf, dass die Einnahme von SSRI in der Schwangerschaft das Risiko für das Auftreten einer persistierenden pulmonalen Hypertonie beim Neugeborenen möglicherweise erhöhen kann.[20] Falls ein Neugeborenes irgendeines dieser Symptome aufweist, muss der Arzt kontaktiert werden.
Venlafaxin und sein Stoffwechselprodukt Desmethylvenlafaxin gehen in die Muttermilch über. Bei gestillten Kindern wurde in einigen Fällen über Schreien, Reizbarkeit und unnormales Schlafverhalten berichtet.[20] Aktuell scheint bei mütterlicher Monotherapie mit Venlafaxin Stillen bei guter Beobachtung des Kindes akzeptabel.[21] Die Entscheidung für oder gegen das Stillen muss individuell getroffen werden, ebenso wie die Einnahme in der Schwangerschaft.[21]
Wechselwirkungen mit anderen Arzneimitteln
[Bearbeiten | Quelltext bearbeiten]Venlafaxin ist ein Substrat des Cytochrom P450 2D6 und kann (durch eine im Vergleich mit anderen Antidepressiva allerdings nur leicht hemmende Wirkung auf dieses Enzym[22]) die Verstoffwechslung von anderen Stoffen verlangsamen, was zu Vergiftungen führen kann.[23] Venlafaxin ist unterschiedlich wirksam bei Patienten mit unterschiedlichen Cytochrom-P450-Varianten.[24] Unter Behandlung mit Venlafaxin kann, wie bei anderen serotonergen Wirkstoffen, ein potenziell lebensbedrohlicher Zustand, das so genannte Serotonin-Syndrom auftreten. Dies ist insbesondere dann der Fall, wenn andere Substanzen eingenommen werden, die das serotonerge Neurotransmittersystem beeinflussen können. Dazu gehören zum Beispiel Johanniskraut, Lithium, Triptane, Serotonin-Wiederaufnahmehemmer (SSRI), Sibutramin und Tramadol. Venlafaxin darf nicht gemeinsam mit irreversiblen und sollte nicht gemeinsam mit reversiblen Monoaminooxidase-Hemmern (MAO-Hemmern) eingenommen werden. Bei einem Medikationswechsel ist ein ausreichend langes therapiefreies Intervall einzuhalten. Auch die gleichzeitige Anwendung von Venlafaxin mit CYP3A4-Inhibitoren, wie Atazanavir, Clarithromycin, Indinavir, Itraconazol, Voriconazol, Posaconazol, Ketoconazol, Nelfinavir, Ritonavir, Saquinavir und Telithromycin, kann den Venlafaxinspiegel erhöhen.
Venlafaxin kann die Bioverfügbarkeit (gemessen als Area under the curve, AUC) von Haloperidol, Risperidon und Metoprolol erhöhen. Die AUC von Indinavir ist bei gleichzeitiger Einnahme von Venlafaxin vermindert. Die klinische Relevanz dieser Interaktionen ist nicht bekannt.[20]
Absetzsyndrom
[Bearbeiten | Quelltext bearbeiten]Wegen des möglichen Auftretens eines Absetzsyndroms wird empfohlen, die Behandlung ausschleichend zu beenden, das heißt, die Dosis von Venlafaxin schrittweise herabzusetzen und den Patienten zu überwachen. Die Frequenz der Symptome ist abhängig von der Dosis, der Behandlungsdauer und vom individuellen Patienten. Im Zusammenhang mit abruptem Absetzen, Dosisreduktion oder Ausschleichen der Behandlung wurde über folgende Symptome berichtet: Appetitlosigkeit, Angstgefühle, Bewegungsdrang (Agitiertheit), Verwirrung, Durchfall (Diarrhoe), Benommenheit, Mundtrockenheit, Müdigkeit, Kopfschmerzen, Hypomanie, Schlaflosigkeit oder andere Schlafstörungen, Nervosität, Parästhesie, Schläfrigkeit, Schwitzen, Schwindel, Übelkeit, Erbrechen, Zittern (Tremor), Albträume, Schwäche, Hyperakusis, Geschmacksveränderungen, verzerrtes Sehen, Verwirrtheit (Konfusion), Ich-Störungen (Depersonalisation), Ohrgeräusche (Tinnitus), Empfindungsstörungen wie vor allem „Brain zaps“, Wahnideen und verzerrte Wahrnehmung.
Die Mehrzahl der Absetzreaktionen seien laut Herstellerangaben nicht schwerwiegend und klingen spontan ab, in der Regel innerhalb von zwei Wochen nach dem Absetzen von Venlafaxin. In einzelnen Fällen können sie zwei bis drei Monate oder auch länger anhalten.[25]
Stereoisomerie
[Bearbeiten | Quelltext bearbeiten]Venlafaxin ist chiral und enthält ein Stereozentrum. Es gibt somit zwei Enantiomere, die (R)-Form und die (S)-Form. Die Handelspräparate enthalten den Arzneistoff als Racemat[26] (1:1-Gemisch der Enantiomere), wobei aus grundsätzlichen Überlegungen die Verwendung des besser und zugleich meist nebenwirkungsärmer wirksamen Enantiomers (Eutomer) zu bevorzugen wäre.[27]
Herstellung
[Bearbeiten | Quelltext bearbeiten]Zur Synthese von racemischem Venlafaxin geht man von Cyclohexanon und 4-Methoxyphenylacetonitril aus.[28]
Die durch Deprotonierung des Nitrils in der α-Stellung und einer aldolartigen Reaktion wird der Nitrilalkohol erhalten. Die katalytische Hydrierung liefert den Aminoalkohol. Der Wirkstoff wird schließlich durch eine Dimethylierung in einer Eschweiler-Clarke-Reaktion erhalten.

Struktur-Wirkungsbeziehungen
[Bearbeiten | Quelltext bearbeiten]Ein originelles Analogon ist das (R)-Sila-Venlafaxin, welches keine Aktivität mehr am SERT aufweist, sie am NAT bewahrt und antiemetisch wirkt.[29]
Handelsnamen
[Bearbeiten | Quelltext bearbeiten]Efectin (A, PL), Efexor (CH, DK, ES, FI, IT, NL, S, UK), Effexor (CDN, F, USA), Trevilor retard (D), zahlreiche Generika
Umweltrelevanz
[Bearbeiten | Quelltext bearbeiten]Venlafaxin ist eine der Leitsubstanzen der Schweizer Kontrollliste für die Einschätzung der Klärleistung in der 4. Reinigungsstufe.[30]
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Bewertung. infomed Pharma-Kritik, 19. Juli 1996
- Fachinfo und Patienteninfo aller Produkte resp. Handelsnamen im Compendium.ch
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Europäische Arzneibuch-Kommission (Hrsg.): Europäische Pharmakopöe 5. Ausgabe. Band 5.0–5.8, 2006.
- ↑ a b Eintrag zu Venlafaxin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 11. November 2014.
- ↑ a b Datenblatt Venlafaxine hydrochloride bei Sigma-Aldrich, abgerufen am 25. April 2011 (PDF).
- ↑ Stephen Stahl et al.: SNRIs: The Pharmacology, Clinical Efficacy, and Tolerability in Comparison with Other Classes of Antidepressants. CNS Spectr. 2005; 10 (9): 732 – 47.
- ↑ C Moret, M Charveron, JP Finberg, JP Couzinier, M Briley: Biochemical profile of midalcipran (F 2207), 1-phenyl-1-diethyl-aminocarbonyl-2-aminomethyl-cyclopropane (Z) hydrochloride, a potential fourth generation antidepressant drug. In: Neuropharmacology. 24. Jahrgang, Nr. 12, 1985, S. 1211–9, doi:10.1016/0028-3908(85)90157-1, PMID 3005901.
- ↑ E. Mutschler, G. Geisslinger, Heyo K. Kroemer, P. Ruth, M. Schäfer-Korting: Arzneimittelwirkungen. Lehrbuch der Pharmakologie und Toxikologie. 9. Auflage. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart 2008, ISBN 3-8047-1952-X.
- ↑ Therapie neuropathischer Schmerzen, Stand 2008. (PDF; 180 kB) Deutsche Gesellschaft für Neurologie
- ↑ Andrea Cipriani, Xinyu Zhou u. a.: Comparative efficacy and tolerability of antidepressants for major depressive disorder in children and adolescents: a network meta-analysis. In: The Lancet, 2016, doi:10.1016/S0140-6736(16)30385-3.
- ↑ A. L. Montejo, G. Llorca, J. A. Izquierdo, F. Rico-Villademoros: Incidence of sexual dysfunction associated with antidepressant agents: a prospective multicenter study of 1022 outpatients. Spanish Working Group for the Study of Psychotropic-Related Sexual Dysfunction. In: The Journal of clinical psychiatry, Band 62 Suppl 3, 2001, S. 10–21, PMID 11229449.
- ↑ U. Werneke, S. Northey, D. Bhugra: Antidepressants and sexual dysfunction. In: Acta Psychiatrica Scandinavica, 114, 2006, S. 384, doi:10.1111/j.1600-0447.2006.00890.x.
- ↑ Relationship between Antidepressant Drugs and Suicidality in Adults. Clinical Review. (PDF; 2 MB): FDA, 5. Dezember 2006.
- ↑ Robert D. Gibbons, C. Hendricks Brown, Kwan Hur, John M. Davis, J. John Mann: Suicidal thoughts and behavior with antidepressant treatment reanalysis of the randomized placebo-controlled studies of fluoxetine and venlafaxine.
- ↑ Suizidgefahr bei Jugendlichen: Entwarnung für Antidepressiva. Süddeutsche.de
- ↑ A. Cipriani, J. R Geddes, C. Barbui: Venlafaxine for major depression. In: BMJ. 334, 2007, S. 215, doi:10.1136/bmj.39098.457720.BE.
- ↑ NICE – Consultation: Amendment to clinical guideline on depression (clinical guideline 23) ( vom 30. April 2007 im Internet Archive).
- ↑ Antidepressiva: Suizidalität junge Erwachsene.Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM)
- ↑ Wyeth Europa Ltd withdraws its marketing authorisation application for Ellefore, EMA Pressemitteilung, 15. Oktober 2008.
- ↑ Apotheke Adhoc: Desvenlafaxin: Grünes Licht nach 14 Jahren. Abgerufen am 12. August 2022 (deutsch).
- ↑ Pristiq. FDA.
- ↑ a b c d e Trevilor retard 37,5 / 75 / 150 mg. Deutsche Fachinformation, Stand: Mai 2022.
- ↑ a b c Pharmakovigilanz- und Beratungszentrum für Embryonaltoxikologie. Institut für Klinische Pharmakologie und Toxikologie, Charité-Universitätsmedizin. Abgerufen am 13. August 2022.
- ↑ Torsten Kratz, Albert Diefenbacher: Psychopharmakotherapie im Alter. Vermeidung von Arzneimittelinteraktionen und Polypharmazie. In: Deutsches Ärzteblatt. Band 116, Heft 29 f. (22. Juli) 2019, S. 508–517, S. 509.
- ↑ Cytochrome P450 Drug Interaction Table. (PDF; 278 kB) Indiana University:
- ↑ D. E. McAlpine, J. M. Biernacka, D. A. Mrazek, D. J. O’Kane, S. R. Stevens, L. J. Langman, V. L. Courson, J. Bhagia, T. P. Moyer: Effect of cytochrome P450 enzyme polymorphisms on pharmacokinetics of venlafaxine. In: Therapeutic Drug Monitoring, Band 33, Nummer 1, Februar 2011, S. 14–20, doi:10.1097/FTD.0b013e3181fcf94d. PMID 21099743.
- ↑ Efexor. Fachinformation des Arzneimittel-Kompendium der Schweiz, Stand der Informationen: August 2013.
- ↑ ROTE LISTE. Verlag Rote Liste Service, Frankfurt am Main 2017, ISBN 978-3-946057-10-9, S. 225.
- ↑ Everhardus Ariëns: Stereochemistry, a basis for sophisticated nonsense in pharmacokinetics and clinical pharmacology. In: European Journal of Clinical Pharmacology, 26, 1984, S. 663–668, doi:10.1007/BF00541922.
- ↑ Axel Kleemann, Jürgen Engel, Bernd Kutscher, Dietmar Reichert: Pharmaceutical Substances. 4. Auflage. 2 Bände erschienen. Thieme-Verlag, Stuttgart 2000, ISBN 978-1-58890-031-9; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.
- ↑ Graham A. Showell, Matthew J. Barnes, Jürgen O. Daiss et al.: (R)-Sila-venlafaxine: A selective noradrenaline reuptake inhibitor for the treatment of emesis. In: Bioorganic & Medicinal Chemistry Letters. 16. Jahrgang, Nr. 9, 1. Mai 2006, S. 2555–2558, doi:10.1016/j.bmcl.2005.12.062, PMID 16513343.
- ↑ Die Publikationsplattform des Bundesrechts - Verordnung des UVEK zur Überprüfung des Reinigungseffekts von Massnahmen zur Elimination von organischen Spurenstoffen bei Abwasserreinigungsanlagen, Stand 1. Dezember 2016, abgerufen am 21. Juli 2024