Amylnitrit
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Amylnitrit | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C5H11NO2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 117,15 g·mol−1 | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Siedepunkt | ||||||||||||||||||||||
| Dampfdruck |
65 hPa (20 °C)[1] | |||||||||||||||||||||
| Brechungsindex |
1,3918 (20 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Amylnitrit ist eine Bezeichnung für Ester des aliphatischen Alkohols Amylalkohol mit Salpetriger Säure. Die Begriffsverwendung ist aber häufig ungenau und nicht an eine konkrete chemische Struktur gebunden.
Amylnitrit gehört chemisch zur Gruppe der Alkylester der Salpetrigen Säure (Alkylnitrite) wie Ethylnitrit, Propylnitrit, Isopropylnitrit, 1-Butylnitrit oder Isobutylnitrit.
Begriffsdefinition
[Bearbeiten | Quelltext bearbeiten]Amylnitrit bezeichnet strenggenommen nur den von n-Pentanol ausgehenden n-Pentylester der Salpetrigen Säure. Alle anderen Pentylester, die von den verzweigten Pentanolen ausgehen – insbesondere (3-Methylbutyl)-nitrit – werden chemisch korrekt als iso-Amylnitrite bezeichnet, jedoch wird Isoamylnitrit häufig auch als Gruppenname, der den n-Pentylester einschließt, verwendet. Auch eine synonyme Verwendung von „Isoamylnitrit“ und „Amylnitrit“ findet statt.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Der französische Chemiker Antoine-Jérôme Balard (1802–1876) stellte 1844 erstmals Amylnitrit her. 1859 beobachtete J. Guthrie, dass sich beim Einatmen der Amylnitrit-Dämpfe der Puls beschleunigt und Gesichtsröte eintritt. Benjamin Ward Richardson (1828–1896) testete die Wirkung an Fröschen und stellte dabei eine Vasodilatation der Mesenterialgefäße (Arteria mesenterica superior beziehungsweise Arteria mesenterica inferior) fest. Arthur Graham Gamgee (1841–1893) konnte eine blutdrucksenkende Wirkung an Säugetieren nachweisen. Nach diesen Erkenntnissen wurde Amylnitrit 1867 durch den Pharmakologen Thomas Lauder Brunton (1844–1916)[5] in die Angina-pectoris-Therapie eingeführt. Den Wirkungsmechanismus klärte erst 1931 Corneille Heymans (1892–1968) auf.[6]
Isomere und Eigenschaften
[Bearbeiten | Quelltext bearbeiten]| Strukturisomere | ||||
| Name | n-Amylnitrit | 3-Methylbutylnitrit | Isoamylnitrit (Isomerengemisch) | |
| Andere Namen |
n-Pentylnitrit |
3-Methyl-1-nitrosooxybutan |
Isopentylnitrit | |
| Strukturformel | 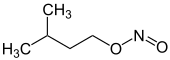
|

| ||
| CAS-Nummer | 463-04-7 | 110-46-3 | 8017-89-8 | |
| EG-Nummer | 207-332-7 | 203-770-8 | ||
| ECHA-Infocard | 100.006.667 | 100.003.429 | ||
| PubChem | 10026 | 8053 | 24687 | |
| ChemSpider | 9632[7] | 7762[8] | ||
| ZVG-Nummer | 510045[9] | 496177[3] | ||
| Wikidata | Q412350 | Q27888090 | Q54086381 | |
3-Methylbutylnitrit ist eine blassgelbe, leichtbewegliche Flüssigkeit mit einer Dichte von 0,87 g·cm−3 (20 °C)[1] und einem Siedepunkt von 98–99 °C. Die Verbindung ist unbegrenzt mischbar mit den meisten organischen Lösungsmitteln, aber wenig löslich in Wasser, wird aber (besonders in Gegenwart von Basen oder Säuren) leicht verseift. Sie besitzt einen charakteristischen, süßlich-dumpfen Geruch.
Darstellung
[Bearbeiten | Quelltext bearbeiten]Im Labor lässt sich Isoamylnitrit durch Reaktion von iso-Amylalkohol, Natriumnitrit und konzentrierter Salzsäure mit anschließender Destillation darstellen.[10]
Wirkung und Verwendung
[Bearbeiten | Quelltext bearbeiten]Amylnitrit wurde ursprünglich zur temporären Erweiterung der Herzkranzgefäße bei der Angina pectoris und zur Senkung des Blutdrucks medizinisch genutzt. Wegen seiner kurzen Wirkdauer wird heute dafür verdünntes Nitroglycerin (Handelsname Nitrolingual) genutzt. Eine durch Amylnitrit herbeigeführte Methämoglobinämie hilft bei der Behandlung einer Cyanid-Intoxikation, da das Methämoglobin dabei zu verträglicherem Cyanomethämoglobin reagiert; heute ist diese Methode aber nicht mehr das Mittel der Wahl.
Aufgrund einer nach Inhalation rasch einsetzenden psychotropen und aphrodisierenden Wirkung wird Amylnitrit missbräuchlich in Form sogenannter „Poppers“ verwendet (siehe Abschnitt Rechtslage).
Organische Nitrite sind NO-Donatoren. In den Endothelzellen von Blutgefäßen wirkt das Stickstoffmonoxid NO durch Second-Messenger-Mechanismen muskelrelaxierend und somit gefäßerweiternd. Da die venösen Blutgefäße durch bessere enzymatische Ausstattung stärker auf NO-Donatoren reagieren, kommt es im normalen Dosisbereich zunächst zu verstärkter Durchblutung und verbesserter Sauerstoffversorgung (Rötung im Gesichtsbereich, medizinisch „Flush“). Überdosierung kann zu akutem Blutdruckabfall, im Extremfall zum Schock führen, wenn durch die Gefäßerweiterung im Körper die Blutversorgung des Gehirns nicht mehr gewährleistet werden kann.
Mutagene, toxische oder immunsuppressive Eigenschaften wurden nicht nachgewiesen. Nitrithaltige Medikamente sind grundsätzlich verschreibungspflichtig. Bei niedrigem Blutdruck ist die Verwendung von Amylnitrit kontraindiziert. Durch Kontakt von flüssigem Amylnitrit mit Schleimhäuten und Augen kann es zu Reizungen und Verätzungen kommen.
In der präparativen organischen Chemie wird Amylnitrit als Nitrosierungsmittel gebraucht. Davon zu unterscheiden ist Amylnitrat, welches wie auch andere Nitrate beispielsweise als Zündbeschleuniger für Dieselkraftstoffe verwendet wird.
Ebenfalls findet es Verwendung in der Synthese von Azoverbindungen, wie beispielsweise 4-(2-Pyridylazo)resorcin. Die Diazotierung des 2-Aminopyridin findet hierbei, auf Grund der Instabilität des Diazoniumsalzes in wässriger Umgebung, in wasserfreiem Medium statt, wobei das Amylnitrit das ansonsten übliche Natriumnitrit ersetzt.[11]
Kontraindikation
[Bearbeiten | Quelltext bearbeiten]Die gleichzeitige Einnahme von nitrathaltigen Medikamenten wie Nitrolingual-Spray oder NO-Donatoren mit PDE-5-Hemmern (z. B. Sildenafil, Tadalafil oder Vardenafil) ist kontraindiziert. Durch die kombinierte Wirkung auf den Blutdruck droht ein akuter lebensbedrohlicher Blutdruckabfall.
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Unerwünschte Wirkungen können Schwindel, Benommenheit, Herzrasen, Blutdruckabfall bis zum lebensbedrohlichen Kreislaufkollaps, eingeschränkte Artikulationsfähigkeit, Kopfschmerzen, Übelkeit, Orientierungslosigkeit, Hautrötung und Hitzewallungen sein. Es kann zu Steigerungen des Hirndruckes und des Augeninnendruckes kommen. Es wird weiterhin von gelb eingefärbter visueller Wahrnehmung direkt nach dem Konsum berichtet.
Gegenmaßnahmen bei Überdosierung
[Bearbeiten | Quelltext bearbeiten]Symptomorientierte Notfallbehandlung wegen der Herz-Kreislauf-bezogenen Symptome: Bewegen der Extremitäten, Kopf tief lagern, tief ein- und ausatmen (Ziel: Venenrückfluss fördern). Adrenalin ist nicht das Mittel der Wahl, da es die Schocksymptome (Schwäche, Ruhelosigkeit, Schwitzen, Blässe, Übelkeit und Erbrechen, Harn- und Stuhlinkontinenz) verschärft.
Bezüglich einer möglichen Dyspnoe (Atemnot) ist das Antidot Methylenblau als Injektion das Mittel der Wahl, da hierdurch der Abbau des Methämoglobins, das die Dyspnoe verursacht und durch das die Nitrit-Intoxikation entsteht, beschleunigt wird. Bei gleichzeitiger Behandlung von Cyanidintoxikation ist vor dem Verabreichen des Methylenblau eine iatrogene Methämoglobinämie, die wiederum die gefährliche Cyanid-Verstoffwechselung umgehen soll, zu beachten.
Sucht
[Bearbeiten | Quelltext bearbeiten]Eine physische Sucht ist nicht bekannt; die Ausbildung einer psychischen Sucht wird für möglich gehalten und soll sich in Unlust an Sex ohne Amylnitrit äußern.
Rechtslage
[Bearbeiten | Quelltext bearbeiten]Amylnitrit unterliegt keinen betäubungsmittelrechtlichen Regelungen, so dass der Besitz legal ist. Jedoch sind Herstellung und Inverkehrbringen ohne Erlaubnis für die Anwendung an Mensch oder Tier in vielen Ländern verboten, da Amylnitrit als pharmakologisch wirksame Substanz unter die Definition arzneimittelrechtlicher Vorschriften (in der EU etwa der Richtlinien 2001/82/EG und 2001/83/EG[12]) fällt und durch solche geregelt wird.[13]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Datenblatt Isopentylnitrit bei Merck, abgerufen am 24. Mai 2018.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-312.
- ↑ a b c Eintrag zu Pentylnitrit in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Eintrag zu Pentyl nitrite im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Barbara I. Tshisuaka: Brunton, Sir Thomas Lauder. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 217.
- ↑ Wolf-Dieter Müller-Jahncke, Christoph Friedrich, Ulrich Meyer: Arzneimittelgeschichte. 2., überarb. und erw. Auflage. Wiss. Verl.-Ges, Stuttgart 2005, ISBN 978-3-8047-2113-5, S. 161.
- ↑ Eintrag zu n-Pentyl nitrite in der ChemSpider-Datenbank der Royal Society of Chemistry, abgerufen am 20. Mai 2018.
- ↑ Eintrag zu Iso-Amyl nitrite in der ChemSpider-Datenbank der Royal Society of Chemistry, abgerufen am 20. Mai 2018.
- ↑ Eintrag zu Pentylnitrit in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Mai 2018. (JavaScript erforderlich)
- ↑ L. Gattermann, H. Wieland: Die Praxis des organischen Chemikers, 29. Auflage. Walter de Gruyter & Co., 1941, S. 147–148.
- ↑ F.H. Pollard, P. Hanson, W.J. Geary: 4-(2-Pyridylazo)-resorcinol as a possible analytical reagent for the colorimetric estimation of cobalt, lead and uranium. In: Analytica Chimica Acta 20, 1959, S. 26–31, doi:10.1016/0003-2670(59)80004-0.
- ↑ Artikel 1 Nr. 2 (b) der Richtlinien 2001/82/EG und 2001/83/EG, umgesetzt in Deutschland in § 2 Abs. 1 des Arzneimittelgesetzes.
- ↑ Für Deutschland siehe auch: Erwin Deutsch, Rudolf Ratzel, Hans-Dieter Lippert: Kommentar zum Arzneimittelgesetz (AMG). 3. Auflage. Gabler Wissenschaftsverlage, 2010, ISBN 978-3-642-01454-3, S. 64–66 (eingeschränkte Vorschau in der Google-Buchsuche).
- ATC-V03
- Feuergefährlicher Stoff
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 40
- Gesundheitsschädlicher Stoff bei Verschlucken
- Gesundheitsschädlicher Stoff bei Einatmen
- Synthetische psychotrope Substanz
- Arzneistoff
- Antidot
- Kraftstoffzusatz
- Dissoziativum
- Psychotroper Wirkstoff
- Salpetrige-Säure-Verbindung
- Pentylester